жааХжЄШЏЙЩЗнгаЯоЙЋЫОЙигкЩюлкЪабЧЛдСњЩњЮяПЦММЙЩЗнгаЯоЙЋЫО
2024ФъАыФъЖШГжајЖНЕМИњзйБЈИц
жааХжЄШЏЙЩЗнгаЯоЙЋЫОЃЈвдЯТМђГЦЁАжааХжЄШЏЁБЛђЁАБЃМіШЫЁБЃЉзїЮЊЩюлкЪабЧЛдСњЩњЮяПЦММЙЩЗнгаЯоЙЋЫОЃЈвдЯТМђГЦЁАбЧЛдСњЁБЛђЁАЙЋЫОЁБЛђЁАЩЯЪаЙЋЫОЁБЃЉЪзДЮЙЋПЊЗЂааЙЩЦБВЂдкПЦДДАхЩЯЪаЕФБЃМіШЫЁЃИљОнЁЖжЄШЏЗЂааЩЯЪаБЃМівЕЮёЙмРэАьЗЈЁЗЁЂЁЖЩЯКЃжЄШЏНЛвзЫљПЦДДАхЙЩЦБЩЯЪаЙцдђЁЗЕШЯрЙиЙцЖЈЃЌжааХжЄШЏТФааГжајЖНЕМжАд№ЃЌВЂГіОпБОАыФъЖШГжајЖНЕМИњзйБЈИцЁЃ
вЛЁЂГжајЖНЕМЙЄзїИХЪі
1ЁЂБЃМіШЫжЦЖЈСЫГжајЖНЕМЙЄзїжЦЖШЃЌжЦЖЈСЫЯргІЕФЙЄзїМЦЛЎЃЌУїШЗСЫЯжГЁМьВщЕФЙЄзївЊЧѓЁЃ
ЁЂБЃМіШЫвбгыЙЋЫОЧЉЖЉБЃМіавщЃЌИУавщвбУїШЗСЫЫЋЗНдкГжајЖНЕМЦкМфЕФШЈРћвхЮёЃЌВЂБЈЩЯКЃжЄШЏНЛвзЫљБИАИЁЃ
3ЁЂБОГжајЖНЕМЦкМфЃЌБЃМіШЫЭЈЙ§гыЙЋЫОЕФШеГЃЙЕЭЈЁЂЯжГЁЛиЗУЕШЗНЪНПЊеЙГжајЖНЕМЙЄзїЃЌВЂгк2024Фъ
дТ
ШеЁЂ2024Фъ
дТ
ШеЖдЙЋЫОФММЏзЪН№ЪЙгУЕШЧщПіНјааСЫЯжГЁМьВщЁЃ
ЁЂБОГжајЖНЕМЦкМфЃЌБЃМіШЫИљОнЯрЙиЗЈЙцКЭЙцЗЖадЮФМўЕФвЊЧѓТФааГжајЖНЕМжАд№ЃЌОпЬхФкШнАќРЈЃК
ЃЈ1ЃЉВщдФЙЋЫОеТГЬЁЂШ§ЛсвщЪТЙцдђЕШЙЋЫОжЮРэжЦЖШЁЂШ§ЛсЛсвщВФСЯЃЛ
ЃЈ2ЃЉВщдФЙЋЫОВЦЮёЙмРэЁЂЛсМЦКЫЫуКЭФкВПЩѓМЦЕШФкВППижЦжЦЖШЃЛЃЈ
ЃЉВщдФЙЋЫОгыПиЙЩЙЩЖЋЁЂЪЕМЪПижЦШЫМАЦфЙиСЊЗНЕФзЪН№ЭљРДУїЯИМАЯрЙиФкВПЩѓвщЮФМўЁЂаХЯЂХћТЖЮФМўЃЛ
ЃЈ4ЃЉВщдФЙЋЫОФММЏзЪН№ЙмРэЯрЙижЦЖШЁЂФММЏзЪН№ЪЙгУаХЯЂХћТЖЮФМўКЭОіВпГЬађЮФМўЁЂФММЏзЪН№зЈЛЇвјааЖдеЫЕЅЁЂФММЏзЪН№ЪЙгУУїЯИеЫЁЂ2024ФъАыФъЖШФММЏзЪН№ДцЗХгыЪЕМЪЪЙгУЧщПіЕФзЈЯюБЈИцЃЛЃЈ
ЃЉЖдЙЋЫОИпМЖЙмРэШЫдБНјааЗУЬИЃЛ
ЃЈ6ЃЉЖдЙЋЫОМАЦфПиЙЩЙЩЖЋЁЂЪЕМЪПижЦШЫЁЂЖЪТЁЂМрЪТЁЂИпМЖЙмРэШЫдБНјааЙЋПЊаХЯЂВщбЏЃЛ
ЃЈ7ЃЉВщбЏЙЋЫОЙЋИцЕФИїЯюГаХЕВЂКЫВщГаХЕТФааЧщПіЃЛ
ЃЈ8ЃЉЭЈЙ§ЙЋПЊЭјТчМьЫїЕШЗНЪНЙизЂгыЗЂааШЫЯрЙиЕФУНЬхБЈЕРЧщПіЁЃ
ЖўЁЂБЃМіЛњЙЙКЭБЃМіДњБэШЫЗЂЯжЕФЮЪЬтМАећИФЧщПі
ЛљгкЧАЪіБЃМіШЫПЊеЙЕФГжајЖНЕМЙЄзїЃЌБОГжајЖНЕМЦкМфЃЌБЃМіШЫКЭБЃМіДњБэШЫЮДЗЂЯжЙЋЫОДцдкжиДѓЮЪЬтЁЃ
Ш§ЁЂжиДѓЗчЯеЪТЯю
БОГжајЖНЕМЦкМфЃЌЙЋЫОжївЊЕФЗчЯеЪТЯюШчЯТЃК
ЃЈвЛЃЉММЪѕЗчЯе
1ЁЂаТВњЦЗПЊЗЂЗчЯе
ЬхЭтеяЖЯаавЕЪЧММЪѕУмМЏаЭаавЕЃЌЦфбаЗЂКЭЩњВњЪЧвЛжжЖрбЇПЦИпЖШЯрЛЅЩјЭИЁЂжЊЪЖУмМЏЁЂММЪѕКЌСПИпЕФЛюЖЏЃЌЖдММЪѕДДаТКЭВњЦЗбаЗЂФмСІвЊЧѓНЯИпЁЃЬхЭтеяЖЯСьгђММЪѕИќаТНЯПьЁЂЯИЗжЪаГЁНЯЖрЃЌВњЦЗжжРрПьЫйдіМгЕФЭЌЪБЃЌЭЌРрЯюФПЕФММЪѕЗНЗЈвВдкЬцДњЙ§ГЬжаЁЃЙЋЫОдкаТВњЦЗбаЗЂЙ§ГЬжаПЩФмУцСйвђбаЗЂММЪѕТЗЯпГіЯжЦЋВюЁЂбаЗЂНјГЬЛКТ§ЖјЕМжТбаЗЂЪЇАмЕФЗчЯеЃЌЭЌЪБвВПЩФмГіЯждкбаВњЦЗЖЈЮЛЦЋВюЕМжТВњЦЗЩЬвЕМлжЕНЯЕЭЕФЗчЯеЃЌНјЖјЖдЙЋЫОЕФЪаГЁОКељСІдьГЩВЛРћгАЯьЁЃ
2ЁЂММЪѕШЫВХСїЪЇЗчЯе
ЬхЭтеяЖЯаавЕЪЧММЪѕУмМЏаЭаавЕЃЌгЕгаЮШЖЈЁЂИпЫижЪЕФПЦММШЫВХЖгЮщЖдЙЋЫОЕФЗЂеЙжСЙиживЊЁЃЫцОМУКЭвНСЦСьгђЕФХюВЊЗЂеЙЃЌЬхЭтеяЖЯСьгђаавЕШЫВХМлжЕШе
вцЭЙЯдЃЌЕЋаавЕВЛЖЯМгОчЕФШЫВХОКељПЩФмЕМжТММЪѕШЫВХСїЪЇЃЌДгЖјгАЯьЙЋЫОЕФГжајДДаТФмСІЃЌЖдЙЋЫОЕФГЄдЖЗЂеЙдьГЩВЛРћгАЯьЁЃ
3ЁЂММЪѕИќаТМАВњЦЗЩ§МЖЗчЯеЙЋЫОЫљДІЕФЬхЭтеяЖЯаавЕОпгаЖрбЇПЦШкКЯЁЂПЦММКЌСПИпЁЂЖдШЫдБЫижЪвЊЧѓИпЁЂбаЗЂМАВњЦЗзЂВсжмЦкНЯГЄЁЂММЪѕИќаТЛЛДњНЯПьЕШЬиЕуЁЃЙЋЫОашвЊЭЈЙ§ГжајЕФВњЦЗбаЗЂЃЌВЛЖЯЬсЩ§дгаВњЦЗЕФММЪѕЫЎЦНЃЌТњзужеЖЫПЭЛЇЕФашЧѓЁЃ
ЕЋЮДРДШєЙЋЫОВЛФмМАЪБИњзйЁЂеЦЮеВЂе§ШЗЗжЮіаТММЪѕЁЂаТВФСЯЛђаТЙЄвеЖдаавЕЕФгАЯьВЂВЩШЁЧЁЕБгІЖдДыЪЉЃЌЮоЗЈМАЪБЭъГЩдгаВњЦЗЕФЩ§МЖЛЛДњЃЌЛђепПЦбагыЩњВњВЛФмТњзуЪаГЁЕФвЊЧѓЃЌНЋЖдЮДРДЙЋЫОвЕМЈдіГЄМАГжајгЏРћФмСІВњЩњВЛРћгАЯьЁЃ
ЃЈЖўЃЉОгЊЗчЯе
1ЁЂОЯњЩЬЙмРэЗчЯе
ЙЋЫОдкздВњВњЦЗЯњЪлЛЗНкВЩШЁЁАОЯњЮЊжїЁЂжБЯњЮЊИЈЁБЕФЯњЪлФЃЪНЁЃЙЋЫОЪкШЈОЯњЩЬдкжИЖЈЧјгђЛђжеЖЫНјааЯњЪлЃЌГ§вЕЮёКЯзїЭтЃЌИїОЯњЩЬдкШЫЁЂВЦЁЂЮяЕШЗНУцОљЖРСЂгкЙЋЫОЁЃЙЋЫОжЦЖЈСЫбЯИёЕФОЯњЩЬЙмРэжЦЖШЃЌвЊЧѓОЯњЩЬАДееЙњМвЗЈТЩЗЈЙцЁЂЯрЙиеўВпКЯЗЈОгЊЁЃЫцзХЙЋЫОЕФПьЫйЗЂеЙЃЌЖдОЯњЩЬЕФХрбЕЙмРэЁЂзщжЏЙмРэвдМАЗчЯеЙмРэЕФФбЖШвВНЋМгДѓЁЃШєЙЋЫОВЛФмМАЪБЬсИпЖдОЯњЩЬЕФЙмРэФмСІЃЌвЛЕЉОЯњЩЬГіЯжздЩэЙмРэЛьТвЁЂЮЅЗЈЮЅЙцЕШааЮЊЃЌПЩФмЕМжТЙЋЫОВњЦЗЯњЪлГіЯжЯТЛЌЃЌЖдЙЋЫОЕФЪаГЁЭЦЙуВњЩњВЛРћгАЯьЁЃ
2ЁЂВњЦЗМлИёЯТНЕЕФЗчЯе
ЬхЭтеяЖЯЪдМСЕФЖЈМлФЃЪНЃЌвЛАузлКЯПМТЧИУВњЦЗдкЧјгђЪаГЁОЮяМлВПУХХњзМЕФМьбщЯюФПЪеЗбЫЎЦНЁЂздЩэбаЗЂЭЖШыЁЂЩњВњГЩБОЁЂВњЦЗЪаГЁОКељЧщПіЕШвђЫизлКЯШЗЖЈЁЃ
ЫцзХЮвЙњвНСЦжЦЖШИФИяЕФНјвЛВНЩюЛЏЃЌЙњМвЖдЬхЭтеяЖЯЪдМСМлИёЕФЙмРэЮДРДПЩФмНЋШеЧїбЯИёЃЌЙЋЫОВњЦЗЯњЪлМлИёПЩФмЪмЕНвНБЃеўВпЁЂеаЭЖБъеўВпЃЈЬиБ№ЪЧМЏВЩеўВпЃЉЁЂвНдКВЩЙКЙцЖЈЕШеўВпвђЫиЕФгАЯьЃЛЭЌЪБЃЌЭЌРраТВњЦЗЕФЭЦГіЕМжТаавЕ
ОКељМгОчЁЂММЪѕИяаТЕШЪаГЁвђЫивВПЩФмЕМжТЙЋЫОВњЦЗЕФМлИёЯТНЕЃЌНјЖјЖдЙЋЫОУЋРћТЪЫЎЦНКЭЪеШыЫЎЦНдьГЩВЛРћгАЯьЁЃ
3ЁЂдВФСЯНјПкЗчЯеЮЊБЃеЯВњЦЗЕФжЪСПКЭадФмЕФЮШЖЈадЃЌЙЋЫОгУгкЩњВњЬхЭтеяЖЯЪдМСЕФВПЗждСЯвдМАгУгкЩњВњЬхЭтеяЖЯвЧЦїЕФВПЗжВПМўжївЊВЩгУНјПкдВФСЯЁЃШєЪмЙњМЪУГвзФІВСЕШвђЫигАЯьЃЌЯрЙиЙЉгІЩЬВЛФмМАЪБЁЂБЃжЪЁЂБЃСПЕФЙЉгІКЯИёЕФдВФСЯЃЌЛђепЮДРДЙиМќНјПкдВФСЯЕФМлИёЛђЛуТЪЗЂЩњжиДѓВЛРћБфЛЏЃЌНЋгАЯьЙЋЫОНЛЛѕжЪСПКЭГЩБОЫЎЦНЃЌЖдЙЋЫОЕФе§ГЃЩњВњОгЊдьГЩВЛРћгАЯьЁЃ
4ЁЂСЊЖЏЯњЪлЗчЯеСЊЖЏЯњЪлеўВпЯТЃЌШчЙћОЯњЩЬЯђЙЋЫОВЩЙКЪдМСЕФН№ЖюОљЕЭгкдЄЦкЃЌЕМжТЪдМСЯњЪлЪеШыдіГЄЛКТ§ЃЌЛђЬхЭтеяЖЯЪаГЁММЪѕЕќДњЫйЖШМгПьЃЌЕМжТЙЋЫОвЧЦїдкИпЫйИќаТЛЛДњЯТЪдМСгУСПдіГЄЗІСІЃЌдђЙЋЫОНЋУцСйЮоЗЈЪеЛивЧЦїГЩБОМАОгЊвЕМЈЯТЛЌЕФЗчЯеЁЃДЫЭтЃЌЫфШЛСЊЖЏЯњЪлеўВпЪЧФПЧАЬхЭтеяЖЯаавЕЭЈааЕФЯњЪлФЃЪНЃЌЧвЦфКЯЙцадЁЂКЯРэадвбБЛаавЕФкЦѓвЕЖрДЮТлжЄЃЌЕЋЫцзХЙњМвеўВпЕФНјвЛВНБфЛЏЃЌСЊЖЏЯњЪлПЩФмУцСйЬєеНЃЌЙЋЫОЯжгаЯњЪлеўВпПЩФмвђДЫЗЂЩњИФБфЁЃЙЋЫОНЋВЛЖЯИњзйЙњМвеўВпЕФНтЖСЃЌгыЭЌаавЕЦѓвЕЙВЭЌЬНЫїаТЕФЗћКЯаавЕЬиЕуЕФЯњЪлФЃЪНЃЌМАЪБЕїећОгЊВпТдЁЃ
5ЁЂДњРэвЕЮёБфЖЏЗчЯеЙЋЫОвЕЮёАќРЈБДПЫТќЁЂБЬЕЯЁЂЮжЗвЕШЖрИіЙњЭтвНСЦЦїаЕВњЦЗЕФДњРэЯњЪлЁЃЙЋЫОгыЩЯЪіЙњЭтвНСЦЦїаЕЩњВњЩЬЧЉЖЉЕФДњРэавщгааЇЦквЛАуЮЊвЛФъЃЌЦкТњКѓашвЊжиаТЧЉЖЉЁЃЬШШєЙЋЫОгыЩЯЪіЦЗХЦЩњВњЩЬЕФДњРэЙиЯЕвђЪаГЁЛЗОГБфЛЏЛђЦфЫћдвђжежЙЃЌНЋЖдЙЋЫОЕФОгЊвЕМЈВњЩњВЛРћгАЯьЁЃ
6ЁЂПЙдПЙЬхЭтЙКЗчЯеПЙдПЙЬхЪЧУтвпеяЖЯЪдМСЕФКЫаФдСЯжЎвЛЃЌЙЋЫОгУгкЩњВњЬхЭтеяЖЯЪдМСЕФПЙдПЙЬхжївЊЭЈЙ§ЖдЭтВЩЙКЛёЕУЁЃШєЩЯгЮПЙдПЙЬхаавЕВњЩњжиДѓБфЛЏЃЌЕМжТПЙдПЙ
ЬхГіЯжМлИёЗЂЩњДѓЗљВЈЖЏЁЂЙЉИјЖЬШБЛђжЪСПЯТНЕЃЌНЋгАЯьЙЋЫОВњЦЗЕФЩњВњГЩБОЁЂВњФмвдМАВњЦЗжЪСПЃЌДгЖјЖдЙЋЫОЕФе§ГЃЩњВњОгЊдьГЩВЛРћгАЯьЁЃ
ЃЈШ§ЃЉеўВпЗчЯе
1ЁЂаТВњЦЗзЂВсЗчЯедкЮвЙњЃЌЯрЙивНСЦЦїаЕЗЈТЩЗЈЙцвЊЧѓЃЌаТВњЦЗбаЗЂГЩЙІКѓЃЌЛЙБиаыОЙ§зЂВсМьбщЁЂСйДВЦРМлЁЂВњЦЗзЂВсЛђВњЦЗБИАИЁЂзЂВсжЪСПЙмРэЬхЯЕКЫВщЁЂЩњВњаэПЩЛђЩњВњБИАИЕШНзЖЮЃЌВХФмЛёЕУЯргІвЉЦЗМрЖНЙмРэВПУХАфЗЂЕФвНСЦЦїаЕзЂВсжЄЛђБИАИЦОжЄЁЂвНСЦЦїаЕЩњВњаэПЩжЄЛђЩњВњБИАИЦОжЄЃЌШЁЕУЪаГЁзМШыаэПЩЁЃЙњЭтЪаГЁЖдвНСЦЦїаЕвВжЦЖЈСЫбЯИёЕФМрЙмжЦЖШЃЌЙЋЫОВњЦЗНјШыЙњЭтЪаГЁвВвЊТњзуЕБЕиЯргІЗЈТЩЗЈЙцЕФвЊЧѓЁЃ
ЕЋгЩгкВЛЭЌЙњМвКЭЕиЧјЕФВњЦЗзЂВсГЬађЁЂвЊЧѓКЭжмЦкДцдкВювьЃЌВПЗжЙњМвКЭЕиЧјЖдНјПквНСЦЦїаЕзМШыУХМїНЯИпЃЌзЂВсжмЦкНЯГЄЁЃШєЮДРДЙњФкЭтВњЦЗзМШыБъзМЗЂЩњжиДѓБфЛЏЃЌЛђЙЋЫОаТВњЦЗЮоЗЈДяЕНЯргІзМШыБъзМЃЌдђНЋЖдЙЋЫОВњЦЗЯњЪлдьГЩВЛРћгАЯьЁЃ
2ЁЂеўВпБфЛЏЗчЯе
ЮЊБЃжЄвНСЦаавЕЕФНЁПЕЗЂеЙЃЌИїМЖвЉЦЗМрЖНЙмРэВПУХвдМАЦфЫћЯрЙиМрЙмВПУХГжајЭъЩЦаавЕЗЈТЩЗЈЙцЃЌМгЧПвНСЦЦїаЕВњЦЗдкжЪСППижЦЁЂЙЉЛѕзЪжЪЁЂВЩЙКеаБъЕШЗНУцЕФМрЙмЁЃШчЙћЙЋЫОЮДРДдкОгЊВпТдЩЯЮДФмИљОнЙњМввНСЦаавЕМрЙмеўВпЗНУцЕФБфЛЏНјааЯргІЕФЕїећКЭЪЪгІЃЌНЋПЩФмЖдЙЋЫООгЊВњЩњВЛРћгАЯьЁЃ
ЭЌЪБЃЌзд2009ФъЁЖжаЙВжабыЙњЮёдКЙигкЩюЛЏвНвЉЮРЩњЬхжЦИФИяЕФвтМћЁЗЗЂВМвдРДЃЌвНСЦЮРЩњаавЕИФИяВЛЖЯЩюЛЏЃЌ2016ФъвдРДТНајЭЦГіЁАСНЦБжЦЁБЁЂМЏжаВЩЙКЕШИФИяДыЪЉЁЃ
дкЬхЭтеяЖЯСьгђЃЌЁАСНЦБжЦЁБЁЂМЏжаВЩЙКЕШДыЪЉвбдкВПЗжЕиЧјЪЕЪЉЃЌЙЋЫОдЄМЦЫцзХвНСЦЮРЩњЬхжЦИФИяЕФЭЦНјЃЌЁАСНЦБжЦЁБЁЂМЏжаВЩЙКЕШДыЪЉНЋЛсж№ВНЭЦЙуЁЃШчЙћЙЋЫОВЛФмЫГгІвНСЦИФИяЕФЗНЯђЃЌМАЪБжЦЖЈЯрЙигІЖдДыЪЉЃЌЖдОЯњЩЬЯЕЭГНјаагХЛЏЃЌГжајБЃГжбаЗЂЭЖШыгыВњЦЗДДаТЃЌПЩФмЛсУцСйОгЊвЕМЈЯТЛЌЕФЗчЯеЁЃ
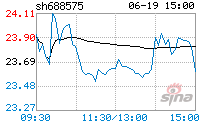
ЃЈЫФЃЉЙЋдЪМлжЕБфЖЏЗчЯеНижС2024Фъ6дТФЉЃЌЙЋЫОГжгадЦПЕМЏЭХгаЯоЙЋЫОЃЈ02325.HKЃЉHЙЩ687.75ЭђЙЩЁЃИУЭЖзЪЕФН№ШкзЪВњЙРжЕБфЖЏВњЩњНЯДѓЕФЙЋдЪМлжЕБфЖЏЃЌЙЋдЪМлжЕБфЖЏЖдБЈИцЦкРћШѓзмЖюЕФгАЯьЮЊШЫУёБв-1,012.78ЭђдЊЁЃШчЙћКѓЦкдЦПЕМЏЭХЙЩМлГіЯжДѓЗљВЈЖЏЃЌЙЋЫОЫљГжН№ШкзЪВњПЩФмДцдкНЯДѓН№ЖюЕФЙЋдЪМлжЕБфЖЏЗчЯеЃЌДгЖјЖдЙЋЫОЕФЙщЪєгкФИЙЋЫОЫљгаепОЛРћШѓдьГЩНЯДѓЕФгАЯьЁЃ
ЫФЁЂжиДѓЮЅЙцЪТЯюЛљгкЧАЪіБЃМіШЫПЊеЙЕФГжајЖНЕМЙЄзїЃЌБОГжајЖНЕМЦкМфЃЌБЃМіШЫЮДЗЂЯжЙЋЫОДцдкжиДѓЮЅЙцЪТЯюЁЃ
ЮхЁЂжївЊВЦЮёжИБъЕФБфЖЏдвђМАКЯРэад2024Фъ1-6дТЃЌЙЋЫОжївЊВЦЮёЪ§ОнМАжИБъШчЯТЫљЪОЃК
ЕЅЮЛЃКдЊ
жївЊЛсМЦЪ§Он
| жївЊЛсМЦЪ§Он | БОБЈИцЦкЃЈ1Ѓ6дТЃЉ | ЩЯФъЭЌЦк | БОБЈИцЦкБШЩЯФъЭЌЦкдіМѕЃЈ%ЃЉ |
| гЊвЕЪеШы | 960,029,208.32 | 1,074,967,509.03 | -10.69 |
| ЙщЪєгкЩЯЪаЙЋЫОЙЩЖЋЕФОЛРћШѓ | 173,028,557.51 | 141,533,046.55 | 22.25 |
| ЙщЪєгкЩЯЪаЙЋЫОЙЩЖЋЕФПлГ§ЗЧОГЃадЫ№вцЕФОЛРћШѓ | 161,319,313.93 | 128,179,757.26 | 25.85 |
| ОгЊЛюЖЏВњЩњЕФЯжН№СїСПОЛЖю | 140,632,406.99 | -545,492,966.93 | ВЛЪЪгУ |
| жївЊЛсМЦЪ§Он | БОБЈИцЦкФЉ | ЩЯФъЖШФЉ | БОБЈИцЦкФЉБШЩЯФъЖШФЉдіМѕЃЈ%ЃЉ |
| ЙщЪєгкЩЯЪаЙЋЫОЙЩЖЋЕФОЛзЪВњ | 2,596,302,567.81 | 2,559,840,879.62 | 1.42 |
| змзЪВњ | 4,040,538,974.27 | 3,806,083,365.13 | 6.16 |
| жївЊВЦЮёжИБъ | БОБЈИцЦкЃЈ1Ѓ6дТЃЉ | ЩЯФъЭЌЦк | БОБЈИцЦкБШЩЯФъЭЌЦкдіМѕЃЈ%ЃЉ |
| ЛљБОУПЙЩЪевцЃЈдЊЃЏЙЩЃЉ | 0.30 | 0.25 | 20.00 |
| ЯЁЪЭУПЙЩЪевцЃЈдЊЃЏЙЩЃЉ | 0.30 | 0.25 | 20.00 |
| ПлГ§ЗЧОГЃадЫ№вцКѓЕФЛљБОУПЙЩЪевцЃЈдЊЃЏЙЩЃЉ | 0.28 | 0.23 | 21.74 |
| МгШЈЦНОљОЛзЪВњЪевцТЪЃЈ%ЃЉ | 6.52 | 5.68 | діМг0.84ИіАйЗжЕу |
| ПлГ§ЗЧОГЃадЫ№вцКѓЕФМгШЈЦНОљОЛзЪВњЪевцТЪЃЈ%ЃЉ | 6.08 | 5.14 | діМг0.94ИіАйЗжЕу |
| баЗЂЭЖШыеМгЊвЕЪеШыЕФБШР§ЃЈ%ЃЉ | 16.19 | 13.29 | діМг2.90ИіАйЗжЕу |
1ЁЂгЊвЕЪеШыНЯЩЯФъЭЌЦкЯТНЕЃЌжївЊЯЕБЈИцЦкФкаТЙквЕЮёНЯЩЯФъЭЌЦкДѓЗљЯТНЕЫљжТЃЌБЈИцЦкФкЙЋЫОЗЧаТЙкздВњвЕЮёШдБЃГжНЯПьдіГЄЁЃ
2ЁЂЙщЪєгкФИЙЋЫОЫљгаепЕФОЛРћШѓЁЂЙщЪєгкФИЙЋЫОЫљгаепЕФПлГ§ЗЧОГЃадЫ№вцЕФОЛРћШѓЁЂЛљБОУПЙЩЪевцЁЂПлГ§ЗЧОГЃадЫ№вцКѓЕФЛљБОУПЙЩЪевцЗжБ№ЩЯЩ§
22.25%ЁЂ25.85%ЁЂ20.00%ЁЂ21.74%ЃЌМгШЈЦНОљОЛзЪВњЪевцТЪЭЌБШдіМг0.84ИіАйЗжЕуЃЌвдЩЯжИБъБфЖЏжївЊЯЕБЈИцЦкФкЙЋЫОЗЧаТЙкздВњвЕЮёгЊвЕЪеШыЭЌБШдіГЄНЯПьЃЌвдМАЪеШыНсЙЙБфЛЏв§Ц№ЕФУЋРћТЪЬсИпЃЌЕМжТБОБЈИцЦкУЋРћЖюНЯЩЯФъЭЌЦкдіМгЁЃ
3ЁЂОгЊЛюЖЏВњЩњЕФЯжН№СїСПОЛЖюдіМгЃЌжївЊЯЕБОБЈИцЦкЯњЪлЩЬЦЗЪеЕНЕФЯжН№діМгвдМАжЇИЖЕФЫАЗбКЭЦфЫћжЇГіМѕЩйЫљжТЁЃ
СљЁЂКЫаФОКељСІЕФБфЛЏЧщПі
ЃЈвЛЃЉКЫаФОКељСІЗжЮі
1ЁЂЗсИЛЕФЬхЭтеяЖЯММЪѕЦНЬЈ
ЙЋЫОзд2013ФъжСНёзЈзЂгкДХЮЂСЃпЙрЄѕЅЛЏбЇЗЂЙтЦНЬЈЕФНЈЩшЃЌГЩЙІбаЗЂГіЭъЩЦЕФДХЮЂСЃпЙрЄѕЅЛЏбЇЗЂЙтЦНЬЈЃЌГЩЮЊЙњФкНЯдчЪЕЯжДХЮЂСЃпЙрЄѕЅЛЏбЇЗЂЙтУтвпЗжЮівЧМАХфЬзЪдМСВњвЕЛЏЕФЦѓвЕЁЃФПЧАЃЌдквЧЦїЁЂЪдМСДХжщЁЂМЄЗЂвКЁЂЕзЮяЁЂаЁЗжзгБъМЧММЪѕЕШКЫаФСьгђОљОпгазЈРћЃЌВњЦЗадФмЮШЖЈадИпЃЌГЩЙІНјШыСЫЙњФкИпЖЫУтвпМьВтВњЦЗЪаГЁЁЃЭЌЪБЃЌЭЈЙ§зджїбаЗЂЁЂЭтВПВЂЙКЕШЗНЪНЃЌвбНЈСЂСЫгЕгазджїжЊЪЖВњШЈЕФЩњЛЏеяЖЯЁЂЛЏбЇЗЂЙтЁЂУтвпгЁМЃЁЂУИСЊУтвпЁЂНКЬхН№ВуЮіЁЂМфНгУтвпгЋЙтСљДѓЦНЬЈЃЌвбГЩЮЊЙњФкСьЯШЕФЪЕбщЪвзлКЯНтОіЗНАИЬсЙЉЩЬЁЃ
2ЁЂЭъЩЦЧвЖРЬиЕФСйДВеяЖЯВњЦЗВЫЕЅ
еяЖЯЪдМСЗНУцЃЌЙЋЫОЪдМСВњЦЗКИЧЪѕЧААЫЯюЁЂМззДЯйЁЂжзСіБъМЧЮяЕШжЪСПЮШЖЈЕФГЃЙцМьВтЯюФПЃЌЛЙгЕгаздЩэУтвпадМВВЁЁЂЩњжГНЁПЕЁЂКєЮќЕРВЁдЬхЁЂЬЧФђВЁЕШгХЪЦЭЛГіЕФЬиЩЋМьВтЯюФПЁЃ
3ЁЂЙњФкСьЯШЕФЬхЭтеяЖЯВњЦЗбаЗЂФмСІКЭГЩЙћзЊЛЏФмСІ
ЙЋЫОгЕгавЛжЇММЪѕИВИЧШЋУцЁЂКЫаФСІСПЭЛГіЕФММЪѕбаЗЂЖгЮщЃЌгЕгааавЕСьЯШЕФГЩЙћзЊЛЏФмСІЁЃбаЗЂШЫдБзЈвЕЩцМАвНбЇМьбщЁЂЩњЮяММЪѕгыМьВтЁЂЩњЮяЙЄГЬЁЂУт
впбЇгыЗжзгЩњЮябЇЁЂЩњЮяЛЏбЇЁЂгаЛњЛЏбЇгыКЯГЩЁЂЛЏбЇЗжЮіММЪѕЁЂвНСЦЦїаЕЙЄГЬЁЂЛњаЕЁЂМЦЫуЛњЁЂЕчзгЁЂздЖЏЛЏПижЦЁЂЙтбЇЁЂСїЬхЕШИїСьгђЁЃЙЋЫОбаЗЂСьЕМЭХЖгЩюИћЬхЭтеяЖЯбаЗЂСьгђЖрФъЃЌОпгааавЕСьЯШЕФДДаТбаЗЂФмСІЃЌЙЋЫОвЧЦїбаЗЂзмМраЄг§ОЂШйЛёЁА2019ФъЖШжаЙњЬхЭтеяЖЯВњвЕСьОќШЫЮяЁБЁЂЙЋЫОЪдМСбаЗЂзмМрЧЎДПиЈШйЛёЁА2021ФъЖШжаЙњЬхЭтеяЖЯВњвЕСьОќШЫЮяЁБЁЂЙЋЫОЖЪТГЄКњћdЛдШйЛёЁА2022ФъЖШжаЙњЬхЭтеяЖЯВњвЕСьОќШЫЮяЁБЁЂЙЋЫОИБЖЪТГЄЁЂзмОРэЫЮгРВЈШйЛёЁА2023ФъЖШжаЙњЬхЭтеяЖЯВњвЕСьОќШЫЮяЁБЁЃ
4ЁЂЭъЩЦЕФбаЗЂЬхЯЕКЭЗсИЛЕФММЪѕДЂБИдкЬхЭтеяЖЯВњЦЗбаЗЂЩЯЃЌЙЋЫОгЕгаЭъЩЦЕФбаЗЂМмЙЙвдМАЗсИЛЕФбаЗЂОбщЃЌФмЙЛГЩЪьЁЂгааЇЕиНјааВњЦЗбаЗЂЁЃЭЌЪБЃЌЙЋЫОгЕгаЗсИЛЕФММЪѕДЂБИЃЌЯжгаЛЏбЇЗЂЙтММЪѕЦНЬЈЬсЩ§ЗНУцЃЌдкбаЪдМСЯюФПЗсИЛЃЛдкаТаЭММЪѕЗНУцЃЌЙЋЫОврНјааЛљгкЮЂСїПиММЪѕЕФЬхЭтеяЖЯвЧЦїКЭЪдМСЁЂЗжзгеяЖЯММЪѕвдМАЛљвђВтађЕШаТаЭММЪѕСьгђПЊеЙЙЅМсбаЗЂЁЃ
5ЁЂгХжЪПЭЛЇШЯПЩЕФЦЗХЦгХЪЦгЩгкЖрФъРДГжајЯђжЊУћвНдКЬсЙЉадФмгХСМЁЂЦЗжЪЮШЖЈЕФВњЦЗЃЌЙЋЫОвбдквНСЦаавЕФкаЮГЩСМКУЕФПкБЎМАЦЗХЦгХЪЦЁЃЙЋЫОЦОНшЛЏбЇЗЂЙтЕШЬхЭтеяЖЯВњЦЗдкжеЖЫвНдКЬхЯЕФкаЮГЩЕФЦЗХЦжЊУћЖШКЭКУЦРЖШЃЌНјвЛВНЬсЩ§СЫВњЦЗЕФЪаГЁеМгаТЪЁЃЙЋЫОВњЦЗжЪСПКЭадФмЪмЕНИпЖЫМьВтЪаГЁПЭЛЇЕФЙуЗКШЯПЩЃЌдкЙњФкУтвпеяЖЯСьгђОпгаНЯКУЕФПкБЎМАгАЯьСІЃЌаЮГЩСЫНЯЧПЕФЦЗХЦгХЪЦЁЃ
6ЁЂНЁШЋЕФЙЋЫОжЪСПЬхЯЕгыЮШЖЈЕФВњЦЗжЪСПЙЋЫОАДееЙњМвЯрЙиЗЈТЩЗЈЙцвдМАISO9001ЁЂISO13485ЁЂХЗУЫCEЕШжЪСПЬхЯЕЕФвЊЧѓНЈСЂСЫЭъБИЕФжЪСПЙмРэЬхЯЕЃЌДгВњЦЗЩшМЦЁЂВњЦЗбщжЄЁЂЙЉгІЩЬЙмРэЁЂЮяСЯЙмРэЁЂЩњВњЙ§ГЬЙмРэЁЂГЩЦЗМьбщЁЂВњЦЗГіГЇЕШЛЗНкОљв§ШыжЪСППижЦСїГЬЁЃЙЋЫОНЈСЂСЫЭъБИЕФжЪСПЙмРэжЦЖШЃЌЭЈЙ§жЦЖШЛЏЁЂЙцЗЖЛЏЁЂСїГЬЛЏЕФЙмРэЃЌгааЇЪЕЯжСЫВњЦЗЕФжЪСППижЦЁЃФПЧАЃЌЙЋЫОжЪСПЬхЯЕНЈЩшДяЕНЙњМЪБъзМЃЌжївЊВњЦЗвбЭЈЙ§ISO9001ШЯжЄЁЂISO13485ШЯжЄвдМАХЗУЫCEШЯжЄЃЌВЂШЁЕУСЫЁЖжаЙњжЪСПГЯаХЦѓвЕЁЗЕШШйгўЁЃ
7ЁЂЗсИЛЕФЪаГЁОбщгыЭъЩЦЕФгЊЯњЭјТчЙЋЫОДгЪТЬхЭтеяЖЯВњЦЗЕФЯњЪлвЕЮёГЄДяЪЎгрФъЃЌОпгаНЯЧПЕФЪаГЁУєШёЖШЁЂЪаГЁЭЦЙуФмСІвдМАЗсИЛЕФЬхЭтеяЖЯВњЦЗЯњЪлОбщЁЃОЙ§ЪЎгрФъЕФЗЂеЙЃЌЙЋЫОНЈСЂСЫЭъЩЦЕФгЊЯњЭјТчЃЌОЯњЧјгђИВИЧШЋЙњГ§ЬЈЭхЁЂАФУХЭтЕФЫљгаЕиЧјЃЛКЃЭтвЕЮёИВИЧУРжоЁЂХЗжоЁЂбЧжоЁЂЗЧжо110ЖрИіЙњМвКЭЕиЧјЁЃГЩЪьЕФгЊЯњЭјТчФмЙЛЪЙЙЋЫОИќКУЕФСЫНтжеЖЫПЭЛЇЕФашЧѓЃЌФмЙЛМАЪБЗДРЁВњЦЗгХЛЏвтМћЃЌМгПьЙЋЫОЖдВњЦЗЕФИќаТЫйЖШЃЌИќМгЬљКЯЪаГЁЖдгкВњЦЗЕФвЊЧѓЃЌНјвЛВНЬсЩ§жеЖЫгУЛЇЖдгкЙЋЫОВњЦЗЕФШЯПЩГЬЖШЃЌМЋДѓЕФЬсИпСЫЙЋЫОЕФЦЗХЦжЊУћЖШЃЌвВЪЙЙЋЫОгЊвЕЪеШыНќФъРДПьЫйЬсЩ§ЃЌЬсИпСЫЙЋЫОЕФКЫаФОКељСІЁЃ
ЃЈЖўЃЉБЈИцЦкФкЗЂЩњЕФЕМжТЙЋЫОКЫаФОКељСІЪмЕНбЯжигАЯьЕФЪТМўЁЂгАЯьЗжЮіМАгІЖдДыЪЉ
БОГжајЖНЕМЦкМфЃЌБЃМіШЫЭЈЙ§ВщдФЭЌаавЕЩЯЪаЙЋЫОМАЪаГЁаХЯЂЃЌВщдФЙЋЫОеаЙЩЫЕУїЪщЁЂЖЈЦкБЈИцМАЦфЫћаХЯЂХћТЖЮФМўЃЌЖдЙЋЫОИпМЖЙмРэШЫдБНјааЗУЬИЕШЃЌЮДЗЂЯжЙЋЫОЕФКЫаФОКељСІЗЂЩњжиДѓВЛРћБфЛЏЁЃ
ЦпЁЂбаЗЂжЇГіБфЛЏМАбаЗЂНјеЙ
ЃЈвЛЃЉбаЗЂжЇГіБфЛЏЧщПі
ЕЅЮЛЃКдЊ
ПЦФП
| ПЦФП | БОЦкЪ§ | ЩЯЦкЪ§ | БфЛЏЗљЖШЃЈ%ЃЉ |
| ЗбгУЛЏбаЗЂЭЖШы | 154,271,310.80 | 137,428,296.74 | 12.26 |
| зЪБОЛЏбаЗЂЭЖШы | 1,143,503.50 | 5,428,213.31 | -78.93 |
| баЗЂЭЖШыКЯМЦ | 155,414,814.30 | 142,856,510.05 | 8.79 |
| баЗЂЭЖШызмЖюеМгЊвЕЪеШыБШР§ЃЈ%ЃЉ | 16.19 | 13.29 | діМг2.90ИіАйЗжЕу |
| баЗЂЭЖШызЪБОЛЏЕФБШжиЃЈ%ЃЉ | 0.74 | 3.80 | МѕЩй3.06ИіАйЗжЕу |
ЃЈЖўЃЉбаЗЂНјеЙ
БЈИцЦкФкЃЌЙЋЫОаТдіЛёЕУЙњФквНСЦЦїаЕВњЦЗзЂВсжЄ/БИАИЦОжЄ
ЯюЃЛаТдіХЗУЫCEШЯжЄ
ЯюЃЌЦфжаIVDRclassAРр
ЯюЁЂIVDRclassBРр
ЯюЃЌIVDRclassCРр
ЯюЁЃаТдіЪкШЈОГФкЭтзЈРћ
ЯюЃЌаТдіШэМўжјзїШЈжЄЪщ
ЯюЁЃ
АЫЁЂаТдівЕЮёНјеЙЪЧЗёгыЧАЦкаХЯЂХћТЖвЛжТЃЈШчгаЃЉБОГжајЖНЕМЦкМфЃЌБЃМіШЫЭЈЙ§ВщдФЙЋЫОеаЙЩЫЕУїЪщЁЂЖЈЦкБЈИцМАЦфЫћаХЯЂХћТЖЮФМўЃЌЖдЙЋЫОИпМЖЙмРэШЫдБНјааЗУЬИЃЌЛљгкЧАЪіКЫВщГЬађЃЌБЃМіШЫЮДЗЂЯжЙЋЫОДцдкаТдівЕЮёЁЃ
ОХЁЂФММЏзЪН№ЕФЪЙгУЧщПіМАЪЧЗёКЯЙцБОГжајЖНЕМЦкМфЃЌБЃМіШЫВщдФСЫЙЋЫОФММЏзЪН№ЙмРэЪЙгУжЦЖШЁЂФММЏзЪН№зЈЛЇвјааЖдеЫЕЅКЭФММЏзЪН№ЪЙгУУїЯИеЫЃЌВЂЖдДѓЖюФММЏзЪН№жЇИЖНјааЦОжЄГщВщЃЌВщдФФММЏзЪН№ЪЙгУаХЯЂХћТЖЮФМўКЭОіВпГЬађЮФМўЃЌЪЕЕиВщПДФММЏзЪН№ЭЖзЪЯюФПЯжГЁЃЌСЫНтЯюФПНЈЩшНјЖШМАзЪН№ЪЙгУНјЖШЃЌШЁЕУЩЯЪаЙЋЫОГіОпЕФФММЏзЪН№ЪЙгУЧщПіБЈИцЃЌЖдЙЋЫОИпМЖЙмРэШЫдБНјааЗУЬИЁЃ
2024Фъ4дТ18ШеЃЌЙЋЫОейПЊЕкШ§НьЖЪТЛсЕкЖўЪЎвЛДЮЛсвщЁЂЕкШ§НьМрЪТЛсЕкЖўЪЎДЮЛсвщЃЌЩѓвщЭЈЙ§СЫЁЖЙигкВПЗжФМЭЖЯюФПбгЦкЕФвщАИЁЗЃЌЭЌвтЙЋЫОНЋЪзДЮЙЋПЊЗЂааФММЏзЪН№ЭЖзЪЯюФПжЎЁАбаЗЂжааФЩ§МЖМАВњФмРЉГфЯюФПЁБДяЕНдЄЖЈПЩЪЙгУзДЬЌЕФШеЦкбгГЄжС2025Фъ6дТ30ШеЃЌВЂгк2024Фъ4дТ20ШеНјааСЫЙЋИцЁЃ
ЛљгкЧАЪіКЫВщГЬађЃЌБЃМіШЫШЯЮЊЃКБОГжајЖНЕМЦкМфЃЌЙЋЫОвбНЈСЂФММЏзЪН№ЙмРэжЦЖШВЂгшвджДааЃЌФММЏзЪН№ЪЙгУвбТФааСЫБивЊЕФОіВпГЬађКЭаХЯЂХћТЖГЬађЃЌЛљгкЧАЪіМьВщЮДЗЂЯжЮЅЙцЪЙгУФММЏзЪН№ЕФЧщаЮЁЃ
ЪЎЁЂПиЙЩЙЩЖЋЁЂЪЕМЪПижЦШЫЁЂЖЪТЁЂМрЪТКЭИпМЖЙмРэШЫдБЕФГжЙЩЁЂжЪбКЁЂЖГНсМАМѕГжЧщПі
2024ФъЩЯАыФъЖШЃЌЙЋЫОПиЙЩЙЩЖЋЁЂЪЕМЪПижЦШЫЮДЗЂЩњМѕГжааЮЊЃЌЙЋЫОЯжШЮМАБЈИцЦкФкРыШЮЖЪТЁЂМрЪТЁЂИпМЖЙмРэШЫдБКЭКЫаФММЪѕШЫдБГжЙЩБфЖЏЧщПіШчЯТЃК
аеУћ
| аеУћ | жАЮё | ЦкГѕГжЙЩЪ§ | ЦкФЉГжЙЩЪ§ | БЈИцЦкФкЙЩЗндіМѕБфЖЏСП | діМѕБфЖЏдвђ |
| СЮСЂЩњ | ЖЪТЁЂВЦЮёзмМр | 0 | 82,966 | 82,966 | ЖўМЖЪаГЁЙЩЗндіГж |
Г§ДЫжЎЭтЃЌ2024Фъ1-6дТЃЌЙЋЫОПиЙЩЙЩЖЋЁЂЪЕМЪПижЦШЫЁЂЖЪТЁЂМрЪТКЭИпМЖЙмРэШЫдБГжгаЙЋЫОЙЩЪ§ЮДЗЂЩњдіМѕБфЖЏЁЃ
НижС2024Фъ6дТ30ШеЃЌЙЋЫОПиЙЩЙЩЖЋЁЂЪЕМЪПижЦШЫЁЂЖЪТЁЂМрЪТКЭИпМЖЙмРэШЫдБГжгаЕФЙЩЗнОљВЛДцдкжЪбКЁЂЖГНсМАМѕГжЕФЧщаЮЁЃ
ЪЎвЛЁЂБЃМіЛњЙЙШЯЮЊгІЕБЗЂБэвтМћЕФЦфЫћЪТЯю
ЛљгкЧАЪіБЃМіШЫПЊеЙЕФГжајЖНЕМЙЄзїЃЌБОГжајЖНЕМЦкМфЃЌБЃМіШЫЮДЗЂЯжгІЕБЗЂБэвтМћЕФЦфЫћЪТЯюЁЃ
ЃЈБОвГЮое§ЮФЃЌЮЊЁЖжааХжЄШЏЙЩЗнгаЯоЙЋЫОЙигкЩюлкЪабЧЛдСњЩњЮяПЦММЙЩЗнгаЯоЙЋЫО2024ФъАыФъЖШГжајЖНЕМИњзйБЈИцЁЗжЎЧЉеТвГЃЉ
БЃМіДњБэШЫЃК
ЫябзСж
| ЫябзСж | ЭѕЖА |
жааХжЄШЏЙЩЗнгаЯоЙЋЫО
ФъдТШе