���еأ�����֤ȯ������ ֤ȯ���룺300558 ֤ȯ��ƣ�����ҩҵ
����ҩҵ�ɷ�����˾��ҵ��ǹ�������A�ɹ�Ʊ�����ļ�
�������֮�ظ�����
��������
��������������
����ҩҵ�ɷ�����˾2020��ǹ�������A�ɹ�Ʊ�����ļ�
��������Ļظ�����
�й�֤ȯ�ල����ίԱ�
�����2020��5��18�ճ��ߵġ��й�֤�������������Ŀ���һ�η������֪ͨ�顷��200621�ţ�����ơ��������������Ϥ�������˶Է�����������������������������ʵ���ֻظ����£�������ˡ������ر�˵�������ظ������еļ�ƻ����ʵ�������Ԥ������ͬ�����ظ����������������º��壺
| ��������������� | ���� |
| ������Ļش� | ���� |
| �н�����˲���� | ���塢�Ӵ� |
Ŀ ¼
���������1�� ...... 4
���������2�� ...... 16
���������3�� ...... 21
���������4�� ...... 27
���������5�� ...... 60
���������6�� ...... 75
���������7�� ...... 86
���������8�� ...... 90
���������9�� ...... 101
���������10�� ...... 105
���������1�����ڹɷ���Ѻ���뷢���˽����Ѻ��ԭ�����ԡ���Ѻ�ʽ������;��Լ������Ȩʵ�����Ρ��عɹɶ���ʵ�ʿ����˵IJ���״�����峥�������ɼ۱䶯������������¶�Ƿ���ڽϴ��ƽ�ַ��գ��Ƿ���ܵ���ʵ�ʿ����˷���������Լ��عɹɶ���ʵ�ʿ�����ά�ֿ���Ȩ�ȶ��Ե���ش�ʩ���뱣����������ʦ���к˲鲢���������
�ظ���
һ���عɹɶ���ʵ�ʿ����˹ɷ���Ѻ��ԭ�����ԡ���Ѻ�ʽ������;��Լ������Ȩʵ�����Ρ�����״�����峥�������ɼ۱䶯�����
��һ���عɹɶ���ʵ�ʿ����˹ɷ���Ѻ���������
���ݷ������ṩ�Ĺɶ����ᡢ��Ȩ��Ѻ����ļ����й�֤ȯ�Ǽǽ����������ι�˾��2020��6��3�ճ��ߵġ�֤ȯ��Ѻ��˾��������ϸ����������2020��6��3�գ������˿عɹɶ���ʵ�ʿ�������Ѻ��˾�ɷݵ�����������£�
| �عɹɶ�/ʵ�ʿ��������� | �ֹ��������ɣ� | �ֹɱ��� | ����Ѻ�ɷ��������ɣ� | ��Ѻ���� |
| ����Ͷ�� | 80,064,000 | 19.97% | 24,178,000 | 30.20% |
| ����Ͷ�� | 20,649,578 | 5.15% | 15,667,996 | 75.88% |
| ������ | 1,022,184 | 0.25% | ���� | ���� |
| �ϼ� | 101,735,762 | 25.37% | 39,845,996 | 39.17% |
����2020��6��3�գ������˿عɹɶ���ʵ�ʿ��������ֹ�˾�ɷݺϼƱ���Ѻ39,845,996�ɣ�ռ����й�˾�ɷ�������39.17%��ռ��˾�ܹɱ���9.94%��
�������ɷ���Ѻ��ԭ�����ԡ���Ѻ�ʽ������;��Լ������Ȩʵ�����θ��ݷ������ṩ�ġ���Ʊ��Ѻʽ�ع�����ҵ��Э�顷������Ʊ��Ѻʽ�ع����ͻ������顷������Ʊ��Ѻʽ�ع�����Э���顷������Ʊ����Ȩת�ü��ع���ͬ�����Լ������˿عɹɶ���ʵ�ʿ����˳��ߵ�����˵��������2020��6��3�գ������˿عɹɶ���ʵ�ʿ�������Ѻ��˾�ɷݵľ���������£�
| ��� | ������ | ��ѺȨ�� | ��Ѻ�������ɣ� | ��ʼ������Ԫ�� | ��Ѻ���� | ��Ѻԭ���ʽ���; | ��Ȩʵ������ |
| 1 | ���� Ͷ�� | ���Ž�Ͷ֤ȯ�ɷ�����˾ | 7,500,000ע1 | 150,000,000 | 2019.1.22-2021.1.21 | ����ǰ�ڽ�ǰ�ڽ����ʽ���;Ϊ��ȨͶ�ʣ�����ȨͶ�� | 1����Լ����Ԥ���ߣ�180%����Լ����ƽ���ߣ�160%�� 2���Գ�����ΥԼ��Ϊ��Ȩʵ�ֵ�������Ҫ��������1���������ṩ��١���թ��Ϣ���ṩ�IJ��ϡ���Ϣ���ش���������©����2����ͬ����ǰ����������ȷ��ʾ�������ж�����������ծ��3��������δ��ʱ�������֤ȯ����������������ߵ������ӳ���Ѻ���֤ȯ�����ڻ��������۹ɷ�Ϊ���۵��������4��������ʵ��������;Υ��Υ�桢Υ��Э��Լ�����漰������������ҵ����5��������δ�����ѺȨ�˵����ŵ���Ҫ��δ��Լ���ṩ�ʽ���;ʹ��֤�����ϣ���Υ���ʽ���Э��Լ���ģ���6�����ɡ��������桢���Ź��¼������淶���ļ����ܻ�����ֹ�����Ƴ����˲μӹ�Ʊ��Ѻ�ع����ģ���7���������ڼ�ĸ�Ϣ�գ�������δ��Լ����ʱ���֧���ڼ���Ϣ����8�����ڹ����ջ����ڹ����գ�������δ��Լ�����й��ؽ��ף���9����ѺȨ�˸���Э |
| 2 | 4,853,000 | 68,550,000 | 2019.6.25-2021.11.30 | ����ǰ����Ѻ������������;Ϊ��ĿͶ�ʣ� |
| ��� | ������ | ��ѺȨ�� | ��Ѻ�������ɣ� | ��ʼ������Ԫ�� | ��Ѻ���� | ��Ѻԭ���ʽ���; | ��Ȩʵ������ |
| ��Լ��Ҫ���������ǰ���ػ��ȡ��ѺȨ����Ϊ��������Լ���ϴ�ʩ��������δ��ָ�����ڽ��й��ؽ����ȡ��Լ���ϴ�ʩ����10���������ԭ���³�ʼ������ʧ�ܣ���11���������ԭ���¹��ؽ�����ʧ�ܣ���12��������Υ��Э��������뱣֤�����13��������Υ��Э��Լ������������ | |||||||
| 3 | �������Ͷ��������˾ | 1,700,000 | 30,000,000 | 2019.12.30-2020.12.30 | ����ǰ�����ʡ����ڿ���Ͷ�ʺϻ��˲ιɹ�˾��Ӫ | 1����ij1�������գ�T�գ����̺���ռ��ָ��a��180%����ѺȨ����Ȩ��T+1��������ǰ֪ͨ����������Ӧ����ı�֤��������ר��������Ѻ��Ĺ�Ʊʹ��T�շ��ռ��ָ��a��180%�����������δ��T+2������������15:00ǰ������ר��������֤�������Ѻ����Ĺ�Ʊ��ʹ��T�շ��ռ��ָ��a��180%�ģ���ѺȨ����ȨҪ��������������ա�֪ͨ�顷���µ������������ǰ�ع���Ĺ�Ʊ����Ȩ����/����ݡ��������С���20�ŵ�һ�ʽ����С������˵�ָ����������ȫ����Ѻ��Ʊ�������õļۿ������ר��������֧���ع��ۿ����������Ӧ֧��������У��� 2����ij1�������գ�T�գ����̺���ռ��ָ��a��160%����ѺȨ����ȨҪ��������������ա�֪ͨ�顷���µ������������ǰ�ع���Ĺ�Ʊ����Ȩ����ѺȨ��Ҫ���������ǰ�ع���Ĺ�ƱȨ��ʱ����ɾ� | |
| 4 | 4,000,000 | 70,000,000 | 2020.1.9-2021.1.9 |
| ��� | ������ | ��ѺȨ�� | ��Ѻ�������ɣ� | ��ʼ������Ԫ�� | ��Ѻ���� | ��Ѻԭ���ʽ���; | ��Ȩʵ������ |
| ���������С���20�ŵ�һ�ʽ����С������˵�ָ����������ȫ����Ѻ��Ʊ�������õļۿ������ר��������֧���ع��ۿ����������Ӧ֧��������У��� | |||||||
| 5 | ����֤ȯ�ɷ�����˾ | 6,125,000 | 87,500,000 | 2020.5.7-2021.5.7 | ����ǰ����Ѻ�������й�˾Ͷ�� | 1��Ԥ���ߣ�200%��ƽ���ߣ�180%�� 2���Գ�����ΥԼ��Ϊ��Ȩʵ�ֵ�������Ҫ��������1����Լ���Ļع������գ��������ԭ��δ����ɹ��ؽ���δ��ͨ���������ȷ�ʽ�˽�ծ��2����Լ���ϱ�������ƽ���ߺ�����ѺȨ��֪ͨ�����˽�����ǰ���صĹ��ؽ����գ��������ԭ��δ����ɹ��ؽ���δ��ͨ���������ȷ�ʽ�˽�ծ��3��������Ѻ��Ʊ��ST��*ST�����������˱���ܻ�����ȡ��������ȴ�ʩ�������˱���ֹ�����Ʋ����Ʊ��Ѻʽ�ع�����ҵ������δ��Լ֧����Ϣ�����ع��ڼ������ѺȨ��Ҫ����������ڸ��������ε�������δ��ָ�������ڸ�����������Σ�����ѺȨ��֪ͨ�����˽�����ǰ���صĹ��ؽ����գ��������ԭ��δ����ɹ��ؽ���δ��ͨ���������ȷ�ʽ�˽�ծ�� | |
| 6 | ���� Ͷ�� | �й����ʽ��ڹɷ�����˾ | 6,099,998 | 201,000,000 ע2 | 2016.12.26-2020.12.24 | �ʲ���Ԫ���� | 1��Ԥ���ߣ�160%������ߣ�140%�� 2���������ΥԼ�����������ڹ���Э��һ�¼����ڹ��صģ�������ͬ����ѺȨ���������걨ΥԼ���ã�������Э�����ʮ���������ʮ�����Ĺ涨����ȫ�� |
| 7 | 1,000,000 | 2017.6.1-2020.12.24 | |||||
| 8 | 600,000 | 2018.8.9-2020.12.24 | |||||
| 9 | 400,000 | 2018.8.23-2020.12.24 |
| ��� | ������ | ��ѺȨ�� | ��Ѻ�������ɣ� | ��ʼ������Ԫ�� | ��Ѻ���� | ��Ѻԭ���ʽ���; | ��Ȩʵ������ |
| 10 | 6,399,998 | 185,900,000 ע3 | 2017.2.22-2020.12.24 | ���߲��ֱ��֤ȯ���Գ�����ΥԼ��Ϊ��Ȩʵ�ֵ�������Ҫ��������1�������˰�Լ����ȡ��Լ���ϴ�ʩ����뱣֤��ϲ���Ľ�����Լ����������Ԥ����Ԥ���ߣ���������ΥԼ��������2�������ڼ䣬�����˿�����ѺȨ�����벿�ֽ����Ѻ�������뱣֤����в��ֽ����Ѻ��Ľ�����Լ���ϱ�����ȥ��ʼ����Լ���ϱ������ڵ���10%����������ΥԼ������ | |||
| 11 | 768,000 | 2018.8.9-2020.12.24 | |||||
| 12 | 400,000 | 2018.8.23-2020.12.24 |
ע1����ʼ��Ѻ�ɷ�����Ϊ1,585��ɣ���2020��3�½����Ѻ835��ɡ�ע:2������2020��6��3�գ����ʱ������Ϊ154,677,708.21Ԫ��ע3������2020��6��3�գ����ʱ������Ϊ114,984,144.76Ԫ��
����2020��6��3�գ������˿عɹɶ���ʵ�ʿ����������ɷ���Ѻ��ԭ���ʽ���;��ҪΪ����1��������Ʊ��Ѻ���ʡ��黹ǰ�ڽ���2������Ͷ�ʺϻ������ڹ�ȨͶ�ʡ��ιɹ�˾�ճ���Ӫ����3���ʲ���Ԫ���õȣ�δ�漰��ת�÷����˹ɷ�ת�û����Ȩת��ΪĿ�ĵ����Σ�ǰ���ɷ���Ѻ��ԭ������������˿عɹɶ���ʵ�ʿ����������ɷ���Ѻ���Э����������У�δ������ѺȨ����ʹ��Ȩ�����Ρ�
�������عɹɶ���ʵ�ʿ����˵IJ���״�����峥����
1���عɹɶ��IJ���״�����峥����
��1������Ͷ�ʵIJ���״�����峥����
���ݿ���Ͷ���ṩ�IJ����������˿عɹɶ�����Ͷ�����һ��һ�ڵ���Ҫ�����������£�
��λ����Ԫ
| ��Ŀ | 2019��/2019��12��31�� | 2020��1-4��/2020��4��30�� |
| ���ʲ� | 35,673.04 | 42,494.09 |
| �ܸ�ծ | 34,355.00 | 41,355.00 |
| ������Ȩ�� | 1,318.04 | 1,139.09 |
����Ͷ��ϵ������ʵ�ʿ����˵ijֹ�ƽ̨�������з����˹ɷݼ����ֲιɹ�˾��Ȩ�⣬δʵ�ʿ�չ��Ӫҵ��
����Ͷ�ʾ��н�ǿ�ij�ծ����������ԭ�����£�
1������Ͷ�ʵ�ʵ�ʿ����˶���������״������
��ͨ������Ͷ�ʳ��з����˵Ĺɷ��⣬��������ֱ�ӻ�ͨ������ƽ̨��ӳ��з����˵Ĺɷݣ�ӵ�з�����������ʵ���ʲ���������ҵ�Ĺ�Ȩ/�ϻ�ݶ����״�����ã�����ܹ��ڱ�Ҫʱͨ���ʲ����ñ��֡����д���ȶ��ַ�ʽΪ����Ͷ���ṩ�ʽ�֧�֡�
2������Ͷ���Գ��н϶�δ��Ѻ�ķ����˹ɷ�
����2020��6��3�գ�����Ͷ������Ѻ24,178,000�ɷ����˹ɷݣ�����2020��4��30�����̼�94.23Ԫ/�ɣ�ǰ��Ȩ�����㣬�õ���Ѻ�ɷݶ�Ӧ��ֵռ����������ֵ��6.03%�������ϵ͡�����Ͷ�ʳ��е�55,886,000�ɷ����˹ɷ���δ��Ѻ��ռ����з����˹ɷ�������69.80%������2020��4��30�����̼�94.23Ԫ/�ɣ�ǰ��Ȩ�����㣬�õ�δ��Ѻ�ɷݶ�Ӧ����ֵΪ52.66��Ԫ�����Ը��ڿ���Ͷ���Ѱ����ɷ���Ѻ�����ʱ�Ϣ�����н�ǿ���ʽ���������
3�������˳����ķֺ�����
2017��2019���ڼ䣬������ÿ��ȷֱ�����ֽ����6,015��Ԫ����˰����4,411��Ԫ����˰����7,619��Ԫ����˰��������Ͷ���ܹ��Է����˻���ȶ��ķֺ����档���ݿ���Ͷ���ṩ�ġ���ҵ���ñ��桷������Ͷ�ʵ�����״�����ã�������ʧ�ż�¼����δ�峥ծ��δ�����������ע��ĸ�ծ������ѯ�����й����й��������������й�ִ����Ϣ������������Ͷ�ʲ����ڱ�����ʧ�ű�ִ�������������Ρ�
��2������Ͷ�ʵIJ���״�����峥����
���ݱ���Ͷ���ṩ�IJ����������˿عɹɶ�����Ͷ�����һ��һ�ڵ���Ҫ�����������£�
��λ����Ԫ
| ��Ŀ | 2019��/2019��12��31�� | 2020��1-4��/2020��4��30�� |
| ���ʲ� | 56,042.84 | 38,913.65 |
| �ܸ�ծ | 54,668.02 | 37,679.44 |
| ������Ȩ�� | 1,374.82 | 1,234.21 |
����Ͷ��ϵ�����˵�Ա���ֹ�ƽ̨�������з����˵Ĺɷ��⣬δʵ�ʿ�չ��Ӫҵ��
����Ͷ�ʾ��н�ǿ�ij�ծ����������ԭ�����£�
1������Ͷ�ʵ�ʵ�ʿ����˶���������״������
��ͨ������Ͷ�ʳ��з����˵Ĺɷ��⣬��������ֱ�ӻ�ͨ������ƽ̨��ӳ��з����˵Ĺɷݣ�ӵ�з�����������ʵ���ʲ���������ҵ�Ĺ�Ȩ/�ϻ�ݶ����״�����ã�����ܹ��ڱ�Ҫʱͨ���ʲ����ñ��֡����д���ȶ��ַ�ʽΪ����Ͷ���ṩ�ʽ�֧�֡�
2������Ͷ���Գ��в���δ��Ѻ�ķ����˹ɷ�
����2020��6��3�գ�����Ͷ������Ѻ15,667,996�ɷ����˹ɷݣ�����2020��4��30�����̼�94.23Ԫ/�ɣ�ǰ��Ȩ�����㣬�õ���Ѻ�ɷݶ�Ӧ��ֵռ����������ֵ��3.91%�������ϵ͡�����Ͷ�ʳ��е�4,981,582�ɷ����˹ɷ���δ��
Ѻ��ռ����з����˹ɷ�������24.12%������2020��4��30�����̼�94.23Ԫ/�ɣ�ǰ��Ȩ�����㣬�õ�δ��Ѻ�ɷݶ�Ӧ����ֵΪ4.69��Ԫ���Ը��ڱ���Ͷ���Ѱ����ɷ���Ѻ�����ʱ�Ϣ�����н�ǿ���ʽ���������
3�������˳����ķֺ�����2017��2019���ڼ䣬������ÿ��ȷֱ�����ֽ����6,015��Ԫ����˰����4,411��Ԫ����˰����7,619��Ԫ����˰��������Ͷ���ܹ��Է����˻���ȶ��ķֺ����档
���ݱ���Ͷ���ṩ�ġ���ҵ���ñ��桷������Ͷ�ʵ�����״�����ã�������ʧ�ż�¼����δ�峥ծ��δ�����������ע��ĸ�ծ������ѯ�����й����й��������������й�ִ����Ϣ������������Ͷ�ʲ����ڱ�����ʧ�ű�ִ�������������Ρ�
2��ʵ�ʿ����˵IJ���״�����峥����
����2020��6��3�գ�������ֱ�ӻ��ӿ��Ʒ�����101,735,762�ɹɷݣ�ռ��˾�ܹɱ���25.37%����������Ѻ�ɷ�����39,845,996�ɣ�δ��Ѻ�ɷ�����61,889,766�ɣ�δ��Ѻ�ɷ�����ռ������ֱ�ӻ��ӿ��Ʒ����˹ɷ�������
60.83%������2020��4��30�����̼�94.23Ԫ/�ɣ�ǰ��Ȩ�����㣬�õ�δ��Ѻ�ɷݶ�Ӧ����ֵΪ58.32��Ԫ�����Ը��ڿ���Ͷ�ʡ�����Ͷ���Ѱ����ɷ���Ѻ�����ʱ�Ϣ��
�����з����˹ɷ��⣬��������ӵ�з�����������ʵ���ʲ���������ҵ�Ĺ�Ȩ/�ϻ�ݶ����ܹ�ͨ���ʲ����ñ��֡����д���ȶ��ַ�ʽ�����ʽ��룬��ծ������Խ�ǿ��
���ݷ�����ʵ�ʿ����˶������ġ��������ñ��桷������ߵ�����˵������������������״��������״�����ã�������ʧ�ż�¼��������ڵ����Ρ�
����ѯ�����й����й��������������й�ִ����Ϣ����������������������δ�˽���ش����ϡ��ٲã�Ҳ�����ڱ�����ʧ�ű�ִ�������������Ρ�
���ϣ���������������ظ�����֮�գ������˿عɹɶ���ʵ�ʿ����˵IJ���
״��������״�����ã����н�ǿ��ծ���峥������
���ģ������˹ɼ۱䶯���
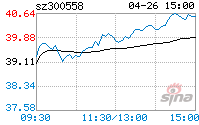
2017��1��1����2020��4��30���ڼ䣬�����˵Ĺɼ۱䶯������£�
������Դ��WIND
����ͼ�ɼ�����2017��1��1����2020��4��30���ڼ䣬�����˹ɼ�Ʊ�ijɽ�����Ϊ55.38Ԫ/�ɣ�ǰ��Ȩ�������Ը���Ŀǰ�ɷ���Ѻ��Ԥ������ƽ���ߣ�ƽ�ַ��սϵ͡�
�����Ƿ���ڽϴ��ƽ�ַ��գ��Ƿ���ܵ���ʵ�ʿ����˷���������Լ��عɹɶ���ʵ�ʿ�����ά�ֿ���Ȩ�ȶ��Ե���ش�ʩ
��һ�������ڽϴ�ƽ�ַ��գ����ᵼ��ʵ�ʿ����˷������
��������������ظ�����֮�գ�����Ͷ�ʡ�����Ͷ�ʹɷ���Ѻ��Ԥ����ƽ�������£�
| ��� | ������ | ��ѺȨ�� | ��Ѻ�������ɣ� | Ԥ���ߣ�Ԫ�� | ƽ���ߣ�Ԫ�� |
| 1 | ���� Ͷ�� | ���Ž�Ͷ֤ȯ�ɷ�����˾ | 7,500,000 | 38.58 | 34.29 |
| 2 | 4,853,000 | 33.76 | 30.01 |
| ��� | ������ | ��ѺȨ�� | ��Ѻ�������ɣ� | Ԥ���ߣ�Ԫ�� | ƽ���ߣ�Ԫ�� |
| 3 | �������Ͷ��������˾ע | 1,700,000 | 33.34 | 29.64 | |
| 4 | 4,000,000 | 33.12 | 29.44 | ||
| 5 | ����֤ȯ�ɷ�����˾ | 6,125,000 | 30.43 | 27.39 | |
| 6 | ���� Ͷ�� | �й����ʽ��ڹɷ�����˾ | 6,099,998 | 33.36 | 29.19 |
| 7 | 1,000,000 | ||||
| 8 | 600,000 | ||||
| 9 | 400,000 | ||||
| 10 | 6,399,998 | 26.54 | 23.22 | ||
| 11 | 768,000 | ||||
| 12 | 400,000 |
ע���ñʹɷ���Ѻ��Ԥ���ߡ�ƽ����ϵ���ݽ���2020��3��21�գ������������С���23�ŵ�һ�ʽ����й�Ʊ����Ȩת�ü��ع���ͬ��Լ�������һ�λع���۽���ʱ�㣩����Ͷ��Ӧ֧���Ļع��������ȷ����
2020��1��1����2020��4��30���ڼ䣬�����˹�Ʊ�ɽ�����Ϊ79.65Ԫ/�ɣ�ǰ��Ȩ�����ϱ��еĹɷ���Ѻƽ�����뷢���˶����г��ɼ����������Խϴ�İ�ȫ�ռ䡣��ˣ����ݷ����˵�ǰ�ɼ����������Ͷ�ʡ�����Ͷ�ʵĹɷ���Ѻ�����ڽϴ��ƽ�ַ��գ���ɷ���Ѻƽ�ֵ��·�����ʵ�ʿ���Ȩ����ķ�����Խϵ͡�
���⣬��������������ظ�����֮�գ������˿عɹɶ���ʵ�ʿ����������ɷ���Ѻ���Э����������У�δ������ѺȨ����ʹ��Ȩ�����Σ������˿عɹɶ���ʵ�ʿ����˵IJ�������״�����ã��Ҿ��ѳ��ߡ�����ά�ֿ���Ȩ�ȶ��ij�ŵ����
���ϣ���������������ظ�����֮�գ�����Ͷ�ʡ�����Ͷ�ʵĹɷ���Ѻ�����ڽϴ��ƽ�ַ��գ���ɷ���Ѻƽ�ֵ��·�����ʵ�ʿ���Ȩ����ķ��սϵ͡�
�������عɹɶ���ʵ�ʿ�����ά�ֿ���Ȩ�ȶ��Ե���ش�ʩ
���ݿعɹɶ���ʵ�ʿ����˳��ߵ�����˵������ŵ��Ϊ������ɷ���Ѻ��ǿ��ƽ�ֶ�Ӱ�췢���˿���Ȩ���ȶ����عɹɶ���ʵ�ʿ��������ƶ���ά�ֿ���Ȩ�ȶ�����ش�ʩ���������£�
1������ר�˽���ÿ�ո��������й�ע��˾�ɼۣ���ǰ���з���Ԥ����
2�����ݹɷ���Ѻ�������Ϸ����˹ɼ۲���Ԥ����Ӧ���������ʽ��緢���˳��ֹɼ۴���µ����Σ��عɹɶ���ʵ�ʿ����˽���ȡ�ӱ�֤�𡢲����ṩ���������ǰ���عɷݵȴ�ʩ����ƽ�ַ��գ��������ֹ�˾�ɷݱ����á�
3���عɹɶ���ʵ�ʿ����˳��ߡ�����ά�ֿ���Ȩ�ȶ��ij�ŵ����
��1���عɹɶ�����Ͷ�ʡ�����Ͷ���ѳ��߳�ŵ���£�
��1����������ŵ����֮�գ����ϻ���ҵ�Ա���ҩҵ�Ĺɷ���Ѻϵ���ںϷ�����������δ���ɷ���Ѻ�����ʽ����ڷǷ���;��
2����������ŵ����֮�գ����ϻ���ҵ�Ա���ҩҵ�ɷ���Ѻ���е����ʲ��������ڳ�����������ΥԼ���Ρ������¼���
3�����ϻ���ҵ�߱���Լ������ծ������峥������ɷ���Ѻ����������������������Դ�Ϸ����ʽ���ʲ�����������Լ�峥����ҩҵ�ɷ���Ѻ������ծ���ϻ���ҵ���µı���ҩҵ�ɷ���Ѻ����Ӱ�챾�ϻ���ҵ�Ա���ҩҵ�Ŀ���Ȩ���õȿ���Ȩ�����ȶ��ԣ�
4�������ϻ���ҵ���е���Ѻ�ɷݴ���ƽ�������Լ������Ȩʵ�����Σ����ϻ���ҵ����������Ȩ�˽���Э�̣���ȡ��ǰ�������ʿ���عɷݡ��ӱ�֤����ṩ������ȷ�ʽ�������в��������Ȿ�ϻ���ҵ���еı���ҩҵ�Ĺɷݱ����ã�ȷ�����ϻ���ҵ�Ա���ҩҵ����Ȩ���ȶ��ԣ�
5������ҩҵ�ɼ��µ����±��ϻ���ҵ�Ա���ҩҵ�Ŀ���Ȩ���ֱ������ʱ�����ϻ���ҵ��������ȡ���Ŵ�ʩ��ȷ�����ϻ���ҵ�Ա���ҩҵ����Ȩ���ȶ��ԣ�
6���籾�ϻ���ҵ���µı���ҩҵ�ɷ���Ѻ������ծ��δ����Լ���еģ����ϻ���ҵ�������Ŭ�����ȴ��ñ��ϻ���ҵӵ�еij�����ҩҵ�ɷ�֮��������ʲ�����ȷ�����ϻ���ҵ�Ա���ҩҵ����Ȩ���ȶ��ԡ���
��2��ʵ�ʿ����˶������ѳ��߳�ŵ���£�
��1����������ŵ����֮�գ�����Ͷ�ʡ�����Ͷ�ʶԱ���ҩҵ�Ĺɷ���Ѻϵ
���ںϷ�����������δ���ɷ���Ѻ�����ʽ����ڷǷ���;��
2����������ŵ����֮�գ�����Ͷ�ʡ�����Ͷ���Ա���ҩҵ�ɷ���Ѻ���е����ʲ��������ڳ�����������ΥԼ���Ρ������¼���
3������Ͷ�ʡ�����Ͷ�ʾ߱���Լ������ծ������峥������ɷ���Ѻ����������������������Դ�Ϸ����ʽ���ʲ��������˽���ȡһ����Ч��ʩȷ������Ͷ�ʡ�����Ͷ����Լ�峥����ҩҵ�ɷ���Ѻ������ծ����Ͷ�ʡ�����Ͷ�����µı���ҩҵ�ɷ���Ѻ����Ӱ����Ա���ҩҵ�Ŀ���Ȩ���õȿ���Ȩ�����ȶ��ԣ�
4��������Ͷ�ʡ�����Ͷ�ʳ��е���Ѻ�ɷݴ���ƽ�������Լ������Ȩʵ�����Σ����˽���ȡһ����Ч��ʩȷ������Ͷ�ʡ�����Ͷ�ʻ�������Ȩ�˽���Э�̣���ȡ��ǰ�������ʿ���عɷݡ��ӱ�֤����ṩ������ȷ�ʽ�������в��������Ա��ⱴ��Ͷ�ʡ�����Ͷ�ʳ��еı���ҩҵ�Ĺɷݱ����ã�ȷ������ҩҵ����Ȩ���ȶ��ԣ�
5������ҩҵ�ɼ��µ����±���Ͷ�ʡ�����Ͷ�ʶԱ���ҩҵ�Ŀ���Ȩ���ֱ������ʱ�����˽�ȷ������Ͷ�ʡ�����Ͷ�ʻ�����ȡ���Ŵ�ʩ��ȷ������Ͷ�ʡ�����Ͷ�ʶԱ���ҩҵ����Ȩ���ȶ��ԣ�
6���籴��Ͷ�ʡ�����Ͷ�����µı���ҩҵ�ɷ���Ѻ������ծ��δ����Լ���еģ����˽���ȡһ����Ч��ʩȷ������Ͷ�ʡ�����Ͷ�ʾ����Ŭ�����ȴ�����ӵ�еij�����ҩҵ�ɷ�֮��������ʲ�����ȷ������Ͷ�ʡ�����Ͷ�ʶԱ���ҩҵ����Ȩ���ȶ��ԡ���
���ϣ������˿عɹɶ���ʵ�ʿ��������ƶ���ά�ֿ���Ȩ�ȶ�����ش�ʩ�����������ŵ���õȴ�ʩ�ܹ���Ч���ơ����ͷ����˿عɹɶ���ʵ�ʿ����˹ɷ���Ѻ�Է����˿���Ȩ�ȶ���ɵķ��ա�
����������������ʦ�ĺ˲����
��һ���˲����
1������˷������ṩ�Ĺɶ����ᡢ�й�֤ȯ�Ǽǽ����������ι�˾���ߵġ�֤ȯ��Ѻ��˾��������ϸ�������빫˾��¶�Ĺɷ���Ѻ���һ�£�
2�������˷������ṩ�ġ���Ʊ��Ѻʽ�ع�����ҵ��Э�顷������Ʊ��Ѻʽ�ع����ͻ������顷������Ʊ��Ѻʽ�ع�����Э���顷������Ʊ����Ȩת�ü��ع���ͬ���ȹɷ���Ѻ����ļ����˽���Ѻ�ʽ������;�����
3����ȡ������˿عɹɶ���ʵ�ʿ����˵ġ���ҵ���ñ��桷�����������ñ��桷�����������ϣ�
4����ȡ�˷����˿عɹɶ���ʵ�ʿ����˳��ߵĹ��ڹɷ���Ѻ������������˵�������ȶ�����Ȩ�������ŵ��
5����ѯ���й��������������й�ִ����Ϣ�������Ĺ�����Ϣ��
�������˲����
���˲飬������������ʦ��Ϊ��
1�������˿عɹɶ���ʵ�ʿ����������ɷ���Ѻ��ԭ��������ɷ���Ѻ���Э����������У�δ������ѺȨ����ʹ��Ȩ�����Σ�
2�������˿عɹɶ���ʵ�ʿ����˵IJ���״��������״�����ã����н�ǿ��ծ���峥������
3������Ͷ�ʡ�����Ͷ�ʵĹɷ���Ѻ�����ڽϴ��ƽ�ַ��գ���ɷ���Ѻƽ�ֵ��·�����ʵ�ʿ���Ȩ����ķ�����Խϵͣ�
4�������˿عɹɶ���ʵ�ʿ��������ƶ���ά�ֿ���Ȩ�ȶ�����ش�ʩ�����������ŵ���õȴ�ʩ�ܹ���Ч���ơ����ͷ����˿عɹɶ���ʵ�ʿ����˹ɷ���Ѻ�Է����˿���Ȩ�ȶ���ɵķ��ա�
���������2��
�뷢����˵��������Ŀ�����Ƿ��г��ۼƻ���������Ŀǰ������⳧���ͺ�����Ŀ�Ƿ������ع涨���뱣����������ʦ���Ժ˲飬���Է������Ƿ���ڷ��ز�����ҵ����ȷ������������У���������������
�ظ���
һ���뷢����˵��������Ŀ�����Ƿ��г��ۼƻ���������Ŀǰ������⳧���ͺ�����Ŀ�Ƿ������ع涨
��һ��������Ŀ
�㽭����ҽҩ�Ƽ�����˾ӵ�еĺ�����Ŀ�����ں������ຼ��δ���Ƽ��ǣ�������������188�š���������������ظ�����֮�գ�������Ŀ���ѽ�����ɡ����ݡ��ຼ�����н����õ�ʹ��Ȩ���ú�ͬ���Լ�������Ȩ֤�飬������Ŀ�����������ʹ��Ȩ�Ĺ滮��;Ϊ��������õأ���������ʹ��Ȩ�˺Ͳ�����Ȩ����Ϊ�㽭����ҽҩ�Ƽ�����˾��
���ݡ��ຼ�����н����õ�ʹ��Ȩ���ú�ͬ����Լ����������Ŀ���ɺ�ɷָ�ת�ã����ۡ����������裩������ô��ڵ����ܽ��������30%�����ಿ�����Գֲ��÷ָ�ת�ã�����Ԥ�ۣ���˸���Ŀ����ռ�ܽ������30%�IJ�����Ȩ֤Ϊ�ָ��IJ�Ȩ֤�����ݷ����˵�˵�����ṩ����ز��ϣ�������Ŀ������Ϊ�Գ֣��õ��ʲ��ָ���ۼƻ���Ŀǰ�����ڱ����ι���������ҵ�����Ӫ��
ҽ�ƽ�����ҵ�ر�����ҩ�з���ҵ����Ͷ��ʱ�䳤��Ͷ�ʽ���Ͷ�ʷ�����Խϸߵ��ص㡣�����ι���������ҵ��Ŀ�չ��ϵ�����˳�ֿ���ҽ�ƽ�����ҵ���ص㣬���ñ����ι���������ҵ����ؿ���˾ս�Ժ���������ȡ��Ʒ���ߡ���չҵ�������DZ���ƶ����á�����ص�����������������⣬Ŀǰ����������Ҫ��פ����ҵ������Ϊ��������ࡢ���\���ࡢҽ�ƽ������Լ�ҽ����Ϣ�����ռ�ѳ������Լ60%��
���ϣ�������ĿĿǰϵΪ��Ϸ����˷�չս�ԣ����ڱ����ι���������ҵ������������к����ԡ�
���������·����������·�������ⲿ��
���ݷ������ṩ�IJ��ϣ����·����Ϊ��˾���ϳ�����Ϊ��˾����ǰ�ܲ��칫���Ƽ�������ԭ�Ϻϳɡ���ҩ�з��ij��������ڹ�˾��Ʒ����������������������ҩ��Ʒ�������࣬���·�������Ƽ���ԭ��ҩ����������ԶԶ��������ʵ�������ǵ����·����ռ�ؽ�40Ķ�Լ���Ӧ�Ļ��������������ܽ��м�������������ܵĿռ�dz����ޡ�
Ϊ�˱�֤��˾������Ӫ����˾��ĸ��˾Ϊʵʩ���壬��������·������Ϊ��˾�ܲ��칫���Ƽ���������ҩ�з��ij�������������·������Ϊ��˾�ĺϳɻ��أ�����ԭ��ҩ�ĺϳɡ�����2019��12��31�գ���˾��������·�����½��˳����������÷������������ʩ����Ͷ����Ӫ������·������δ��ȫͶ����Ӫ��ͨ����������·����������·��������˾�������������������2,500��Ƭ������6,000��Ƭ��������δ��������г�����ҩƷ��������������Ҫ��ߣ����辭ҩ������պ�GMP��֤��Ͷ�������⣬ҩ�����������Ľ�������һ��ϳ����粻��ǰ���в��ܹ滮��һ���²�Ʒ�з��ɹ���û����صij�������˾��δ�����г������н����ڷdz������ĵ�λ�����Ϊ�˱�֤��������δ��������ģ�ij�������Ϊδ��5-10���ڵ��²�Ʒ��ر����ռ��Ա�ȷ���²�Ʒ�з��ɹ���Ͷ����������˾���������·����ռ�ؽ�147Ķ���������82,636.71ƽ���ס����·����������·��������������Ϊ��ҵ�õء����ں��·��������ʱ����磬������ʩ��Ϊ�¾ɣ���������Ҳ��Ϊ��һ������·����Ͷ����Ӫ��������Ҫ�������Ƽ����������Ǩ������·����������·�������ֽ��ɺ�������ԭ�Ϻϳɰ�Ǩ������·���������·������������������δ������������죬�����ƻ���Ϊ�����˾�Ӫ�����IJ��䡣������Ŀǰ���ú��·����������·������δʹ�õij������г��⣬���ڶԹ�˾������ҵ�ĺ���ʹ�ã��ܹ�Ϊ��˾����һ����������룬δ�����ŷ����˲�Ʒ���������ӡ������ߵ������Լ��з����ŵ��������ٳ��������Ŀǰ�õȳ�����ҵ�ij��ⷽΪ��������ࡢҩƷ�з��ࡢ���\���ࡢҽ����Ϣ������ҵ�����Ϸ����˵Ķ������ս�Է���
������Ŀǰ������δʹ�õij������г������Ϊ���к����ԡ�
������������Ŀǰ������⳧���ͺ�����Ŀ�Ƿ������ع涨
�Թ�˾����������������ʼ�ձ����ԡ�Better medicine,Better life��Ϊʹ����Ŭ�������Ϊ���ܲ����й��Ŀ����ҩ��ҵ���������з���ս�Ժ������г������Ƿ����˷�չս�Ե�������������˾���ϼ�ǿ�������£�ǿ��Դͷ���º�ת���о�������Ʒ��Ӫ���ʱ���Ӫ���ϣ�Ŭ����չΪһ������ҩ�з�Ϊ���ľ��������Կ�����ҩΪ���IJ�Ʒ�ĸ�����ҩ��ҵ��
��������������ظ�����֮�գ��㽭����ҽҩ�Ƽ�����˾�ľ�Ӫ��ΧΪ������������Ѫ��ҩ����о�������������ת�á�������ѯ�������߱����ز��������ʣ������ڷ��ز���ҵ�������˼�����Ƶ������ӹ�˾Ҳ���߱����ز��������ʣ������ڷ��ز���ҵ�������˼���ع��ӹ�˾Ҳδ�漰���������ش��ð취����������Ժ���ڴٽ���Լ��Լ�õص�֪ͨ��������[2008]3�ţ���������Ժ���ڼ�����Ʋ��ֳ��з��۹������ǵ�֪ͨ��������[2010]10�ţ��������ڼ������÷��ز��г����ع�����֪ͨ�������췢[2013]17�ţ��������ڽ�һ����ǿ���ز��г����������Ʒס��Ԥ���ƶ��й������֪ͨ��������[2010]53�ţ�����ط��ɷ��桢�������ļ��涨���������ء����ؼ�����ϧ�ۡ���̧���۵����Ρ�
������Ŀ���ڱ����ι���������ҵ��ϵΪ��Ϸ����˷�չս�ԣ����·����������·�������ⲿ��ϵ�����˶���δʹ�ó����ĺ���ʹ�ã��õȳ�����Ϊ�����������ء������Ĺ滮��;��
��ˣ�����������������⳧���ͺ�����Ŀ������ع涨��
�����뱣����������ʦ���Ժ˲飬���Է������Ƿ���ڷ��ز�����ҵ����ȷ������������У�������������
��������������ظ��������֮�գ������˵���Ӫҵ��Ϊ�Էΰ�����Ϊ�����ص㣬�����������Ƶ���������֪ʶ��Ȩ����ҩ����з���������Ӫ���������˼��������ع��ӹ�˾���߱����ز��������ʣ������ڷ��ز���ҵ��
Ŀǰ�����˶������ĺ�����Ŀ���ڱ����ι���������ҵ��ϵ��Ϸ����˷�չս�ԣ��õȷ����ָ���ۼƻ������·����������·�������ⲿ��ϵ�Է�������δʹ�ó����ĺ���ʹ�ã����������ݷ����˲�Ʒ�������ӡ��з������Ⱦ�Ӫ��ģ���������ٳ��������
��ˣ���������������ظ��������֮�գ������˲����ڷ��ز�����ҵ��
Ϊ�ӿ��ʽ�������Ӵ�֧�ֹ�˾����ҩ�з�ҵ�������⽫����е��㽭����ҽҩ�Ƽ�����˾100%�Ĺ�Ȩ��������������Ŀ����25,146.35��Ԫת�ø�ʵ�ʿ����˶�����ȫ�ʿعɵ������������¿Ƽ�����˾��
������Ȩת�õı�Ĺ�Ȩ�Ѿ������ʲ���������˾���������ߡ����������֣�2020������0639�š�������ҩҵ�ɷ�����˾���Ȩת���漰���㽭����ҽҩ�Ƽ�����˾�ɶ�ȫ��Ȩ���ֵ������Ŀ�ʲ��������桷�����¼�ơ����ʲ��������桷���������ݡ��ʲ��������桷��������������2020��3��31�գ��㽭����ҽҩ�Ƽ�����˾100%��Ȩ�����ʲ�������ȷ����������ֵΪ25,146.35��Ԫ��������Ȩת�õļ۸�ϵ�ɽ���˫������ǰ�������������ƽ�ȡ���Ը����ƽ�Ļ�����Э��һ��ȷ����
����������2020��6��12���ٿ������춭�»���ߴλ��飬����ͨ�������ڳ��۱���ҽҩ�Ƽ�100%��Ȩ�߹��������鰸�����������������¿Ƽ�����˾ǩ����Ч�����ġ������㽭����ҽҩ�Ƽ�����˾��Ȩת��Э�顷�����������Ѿͱ��ν���������ǰ�Ͽ�����ȷͬ��Ķ�����������ν��������ύ�����˹ɶ�������顣
����������������ʦ�˲����
��һ���˲����
����������������������ʦ��ȡ�ĺ˲鷽ʽ�����������ڣ�
1����������˶������ĺ�����Ŀ�����·����������·�����������ء������ij��ú�ͬ����������Ȩ֤�顢������Ȩ֤�顢�����˵����춭�»���ߴλ�����顢�������㽭����ҽҩ�Ƽ�����˾��Ȩת��Э�顷�Լ����ʲ��������桷���Է����ˡ��㽭����ҽҩ�Ƽ�����˾�Լ������˿��Ƶ������ӹ�˾�Ƿ���ڷ��ز��������ʽ����˺˲飻
2�����ķ����˷�����Ͷ���Է��ز��Ķ�����������������Ŀ�뱴���ι���������ҵ���ս�Է�չ�ļ�������Ժ�����Ŀ�뱴���ι���������ҵ��Ĺ滮�����̸�˷�������ظ����ˡ�
�������˲����
���˲飬������������ʦ��Ϊ��
1���㽭����ҽҩ�Ƽ�����˾�����ĺ�����Ŀ������Ϊ�ù�˾�Գ֣�Ŀǰ���ڱ����ι���������ҵ�������ָ���ۼƻ���
2����������������ظ�����֮�գ������˼���ع��ӹ�˾������⳧���ͺ�����Ŀ����Ϊ�����������ء������Ĺ滮��;����ط��ɷ��桢�������ļ��Ĺ涨��
3����������������ظ�����֮�գ������˼���ع��ӹ�˾�����߱����ز��������ʣ������ڷ��ز�������ҵ��������Ŀ���ڱ����ι���������ҵ��ϵΪ��Ϸ����˵ķ�չս�ԣ����·����������·�������ⲿ��ϵ�Է�������δʹ�ó����ĺ���ʹ�ã������˲����ڷ��ز�����ҵ��
���������3��
�뷢���˲�����¶ļͶ��Ŀ��ҩ�з�����������Ŀ�Ľ�չ�������������̼��������ʱ�䣬�Լ����ڵ��ٴ��з����պ��������ա��뱣����������ʦ���к˲鲢���������
�ظ���
һ��ļͶ��Ŀ��ҩ�з�����������Ŀ�Ľ�չ�������������̼��������ʱ��
��ѧ��ҩ���з���һ����Ϊ���ӵĹ��̣������������ưб�Ļ����о���ȷ�ϣ���б����Ӧ�Ļ�ѧ���ӵ���ƺͻ�ѧ�ϳɣ��ȵ��������������������ģ�ͺͷ���ѧ�Ľ������ٴ�ǰ����ҩЧ��ҩ����������ҩ������ѧ�о����Ƽ�ѧ�о����Լ�����I�ڡ�II�ڡ�III���ٴ������о����걨NDA�����ҩ�ಿ�ŵ�����
��������������ظ���������գ����η���ļͶ��Ŀ����ҩ�з����з��豸������Ŀ���з���ҩ�ľ���Ʒ�֡���;����ǰ��չ�����������ɵĹ���������еı�������������Ԥ������ʱ�����±���ʾ��
| ��� | �з���Ŀ | ��ҩƷ�� | ��; | ��չ��� | ������ɵĹ��� | Ԥ�ƻ����������ʱ�� |
| ��� | �з���Ŀ | ��ҩƷ�� | ��; | ��չ��� | ������ɵĹ��� | Ԥ�ƻ����������ʱ�� |
| 1.1 | X-396����ALK����NSCLC���������ٴ����� | ��ɳ���ᣬ�ڶ������ALK���ԵĿڷ����Ƽ�����ҩ1�� | ����ʹ�ÿ����������ƺ���ҩ���չ��ALK���Ե����ڷ�Сϸ���ΰ��������� | CDE�����У��ѵݽ�ҩѧ������� | ���CDE����ͨ�� | 2020�� |
| 1.2 | X-396����ALK����NSCLCһ�������ٴ����� | ����ALK���Ե����ڷ�Сϸ���ΰ������� | �����ٴ�������ɻ������� | ��ɢ����ٴ����飬�걨NDA ������ͨ�� | 2022�� | |
| 1.3 | CM082���������ٴ���/���� | Vorolanib�����VEGFR��PDGFR�ȵĶ�е�ڷ����Ƽ�����ҩ1�� | ���ڼ���VEGFR-TKIһ������ʧ�ܵ�ת�������������� | ��/�����ٴ�������ɻ������� | ��ɢ�/�����ٴ����飬�걨NDA������ͨ�� | 2021�� |
| 1.4 | CM082����JS001����ճĤ��ɫ���������ٴ����� | ���ھֲ���չ��ת����ճĤ��ɫ���������� | �չ�����ٴ� | ���III���ٴ����飬�걨NDA ������ͨ�� | 2023�� | |
| 1.5 | MIL60����״ϸ����Сϸ���ΰ������ٴ����� | ������������ά͡����������ҩ��VEGF���Ƽ� | �������ڻ��Է���״ϸ����Сϸ���ΰ������� | �걨BLA������� | ���CDE����ͨ�� | 2021�� |
| 1.6 | BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ����� | ������EGFR�ڷ����Ƽ�����ҩ1�� | ����ʹ�� EGFR���Ƽ���ҩ�����T790Mͻ��ľֲ����ڻ�ת���Է�Сϸ���ΰ������� | �����ٴ������������� | ��ɢ����ٴ����飬�걨NDA������ͨ�� | 2022�� |
| 1.7 | BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/���� | ����EGFRͻ��ľֲ����ڻ�ת���Է�Сϸ���ΰ������� | ��/�����ٴ������������� | ��ɢ�/�����ٴ����飬�걨NDA������ͨ�� | 2023�� |
������Ŀ��Ϊ��ҩ��������ǰ�����һ���ٴ�����μ�ע�����ٴ�����Ŀ���ٴ�������ɺ��걨NDA/BLA���걨����������һ����Ҫ1-2�ꡣ���ݷ����˵�˵�����ٴ������ҩƷע����������ܲ��������ٶȡ�ҩ���ٴ����֡�ҩЧ����ָ�ꡢCDE�����ٶ��Լ�ҩ���������ߵ����ص�Ӱ�졣
�������ڵ��ٴ��з����պ���������
��һ������ҩҵ����ҩ�з�����
1������ҩҵ�ǹ���ҵ��Ϊ�������ӵ����������ҩ�з��������߱�������ٴ�ǰ�з����ٴ��о���ע���걨��������ҩ��˾����2011�꣬��˾�����з��Ĺ���1.1����ҩ���������ԭ����ʳƷҩƷ�ල�����ְ䷢����ҩ֤����������IJ���ʼ�������ۣ��ò�Ʒ���й���һ��ӵ������֪ʶ��Ȩ��С���Ӱ�����ҩ������ҩҵ�������ҩ�з������Ѿ��õ���֤��
�����������к�˾�����ҩ�з���ͨ�������з���ս�Ժ�����ʵ�˹�˾���з����ߣ��ڴ˹����в��������Ż���˾�з��������ɣ�������������Ƶ��з���ϵ��������ɲ���Ϊ��˾��ҩ�з����ĺ�ҽѧ����
��˾��ҩ�з��������豱����ҩ�з����ġ�������ҩ�з����ġ���ҩ�����з�������������ﲿ����ҩ�����ٴ��о�������ţ��е�С���ӡ������ҩ�����ҩ�з���������չ��ҩ������ṹ��ơ���ѧ�ϳɡ�����ɸѡ��ҩ��ҩЧ�о�����ȫ�����ۡ�ר���걨��ҩѧ�о����ٴ�ǰ�о���ͬʱ����˾�����ٴ���Ŀ�滮�Լ�ʵʩ��
���ݹ�˾ҵ��ս�ԣ���˾ҽѧ��ȫ�渺������ǰע���ٴ��о������в�Ʒҽѧ���Ե��ƶ���ʵʩ���������ҵҽѧ��Ŀչ���о��ͷ�����Эͬ�з���ѧ���ƶ��о��ƻ���Э����˾����ҽҩ��Ŀ��ս��Ͷ�ʣ�ȫ��滮�������ٴ��о����ԣ���֯��ʵʩ�������ٴ�������Ŀ��
2������ҩҵ�߱�Խ�ĺ����з��Ŷӣ��з�ʵ��ͻ��
����ҩҵʼ�ռ�֡��˲���������Դ�ͲƸ�����һ�����˾�����Ժ��������ƺ��˲ż���ЧӦ�������ԣ�������һ��������ҩ�з�����˲ŵļ��ˡ�Ŀǰ����˾����Ա��1300���ˣ��������������ⲩʿ30���ˣ�7λ��ѡ���Ҹ߲���˲żƻ���7λ��ѡ�㽭ʡ�߲���˲żƻ���
��˾�ĺ����з��Ŷӳ�Ա�������³�����ϯִ�йٶ�������ʿ����֪���������20����С���ӻ����↑��������ܲü���ϯ��ѧ��JIABING WANG�����ұ�����ʿ��ѧ��������������ܲü���ϯҽѧ��LI MAO��ë������ʿ�Լ�ս�Ժ������ܼ�LI LILY YING����ӯ)��ʿ�������з���������HONG LAN
�����꣩��ʿ�������з�����������ʿ������������з����ܼ�LIANGDENG����������ʿ������ѧ���ܼ�WENXIN XU�������£���ʿ���ٴ�������ҽѧ�������˼��������ȡ�
3������ҩҵÿ�����з�������д���Ͷ�룬�γ��˷ḻ�����в�Ʒ�ݶӹ�˾������һ֧400���˵���ҩ�з����顣Ŀǰ��˾���в�Ʒ30����з����������ḻ���Ѿ��γ���ÿ�궼�д���ҩ�����ٴ������Է�չ̬�ƣ���Ҫ���Ƿΰ��������ȶ�����������������С���Ӱ���ҩ����з�����˾���ڲ��ִ��������ҩ���з�������������̽�����õ����Ʒ�������˾�ѽ���һ֧��Ч���ٴ��о�ҽѧ��Ա���飬���ٴ���������ơ���Ŀ�ĸ��ٹ������涼����רҵ�������ͷḻ�ľ��飬Ϊ��ҩ��Ŀ�Ŀ����ƽ��;��������ṩ��ֱ��ϡ��������ڣ���˾��ҩ�з������ƽ����з���Ա���з�Ͷ��������ӡ���˾�з�Ͷ��������£�
| ��Ŀ | 2019�� | 2018�� | 2017�� |
| �з���Ա�������ˣ� | 466 | 359 | 253 |
| �з���Առ�� | 35.09% | 30.95% | 25.71% |
| �з�Ͷ�����Ԫ�� | 67,458.50 | 59,003.25 | 38,063.98 |
| �з�֧���ʱ�������Ԫ�� | 34,822.16 | 28,633.67 | 17,790.97 |
| �з�֧���ʱ������ռ�з�Ͷ����� | 51.62% | 48.53% | 46.74% |
| �з�Ͷ��ռӪҵ������� | 43.41% | 48.20% | 37.09% |
| �з�֧���ʱ������ռ���ھ�����ı��� | 154.19% | 175.11% | 70.94% |
���ϣ�����ҩҵ���к�ǿ����ҩ�з�ʵ���ͷḻ����ҩ�з����顣
�������������ش�ȷ���Է���
1����ҩ�з��ɹ���
��ҩ���з�Ͷ��ijɹ�����ҩ������ԭ����ҩ����������Ʒ�з�ģʽ���ٴ����鷽�����ٴ���չ�ε�������ڽϴ���졣�ܵ���˵��Խ�ٽ����нΣ��з��ɹ���Խ�ߣ�����ԽС��
2���ɱȹ�˾����ҩ������кͼ����������
����ҩҵļͶ��Ŀ�е���ҩ��Ŀ������2020��4��30�գ����ֿɱȹ�˾����
�л����е�����ҩ���������£�
| ҩƷ���� | ҩƷ��� | ��Ҫ�е� | ���Ʋ�Ʒ | ������ | ��������ʱ�� | �й���½����ʱ�� |
| ��ɳ���� | �ڶ���ALK���Ƽ� | ALK | �������� | ���� | 2011�� | 2013�� |
| �������� | ���� | 2015�� | 2018�� | |||
| CM082 | ��е������Ұ��ἤø��RTKs�����Ƽ� | VEGFR��PDGFR�� | �������� | ���� | 2006�� | 2007�� |
| �������� | �ݶ� | 2005�� | 2006�� | |||
| MIL60 | ������������ά͡������������ҩ | VEGF | ��ά͡ | ���� | 2004�� | 2010�� |
| ���ɴ� | ��³ | - | 2019�� | |||
| IBI305 | �Ŵ� | - | CDE���� | |||
| BP102 | ���� | - | CDE���� | |||
| LY01008 | ��Ҷ | - | CDE���� | |||
| D0316 | ������EGFR���Ƽ� | EGFR��T790Mͻ�� | ��ϣ���� | ��˹���� | 2015�� | 2017�� |
| �������� | �ɭ | - | 2020�� | |||
| �������� | ����˹ | - | CDE���� |
���ϱ����Կ���������ļͶ��Ŀ�е���ҩ��Ŀ����Ϊ��֪����е�Ļ�ѧҩ�Լ���������ҩ����Ըðе�����ҩ��������У��з��ɹ����ʽϸߡ�ļͶ��Ŀ�е���ҩ��Ŀ��Ϊ����ǰ���ε��ٴ���Ŀ����Ŀ�Ѿ���øý���ص��ٴ���������ҽԺ������������˾�Ѿ��ٴ���ע������������CDE����������Ĺ�ͨ����˾ǰ�ڻ��۵��ٴ����ݷḻ���з��ɹ����ʴ�������������У������о��ɹ��ѷ�������Ҷ���ȹ�����Ȩ��ҽѧ�ڿ�����ɳ������������Ѿ�����CDE��Ҫ��ҩѧ�о����ϣ�Ԥ�ƽ���������С���ˣ�����ļͶ��Ŀ�е���ҩ�з���Ŀ�������ش�ȷ���Է��ա�
���������ܴ��ڵ��ٴ��з����պ���������
1���������ѳ����¶���η��е�ļ���ʽ���;�����Ϣ
��˾��2020��3��3���ٿ������춭�»�����λ��飬����ͨ������ʱ��¶�ˡ�2020��ȷǹ�������A�ɹ�ƱԤ������������2020��ȷǹ������й�Ʊļ���ʽ�ʹ�õĿ����Է������桷�ȱ��ηǹ�����������鰸����ļ���ʽ���;�����˳�ֵ���Ϣ��¶��
2������ļͶ��Ŀ�������ش�ȷ���Է���
��˾���ηǹ�������ļ���ʽ�������ҩ�з����з��豸������Ŀ�����������ʽ���Ŀ����˾�Ѿ���ļͶ��Ŀ�Ŀ����Լ���Ҫ�Խ����˳�ֵ��о���֤��ļͶ��Ŀ�漰����ҩ�з���Ŀ��Ϊ����ǰ�����һ���ٴ��μ�ע�����ٴ�����Ŀ���������ش�ȷ���Է��ա�
3�����ܴ��ڵ��ٴ��з����պ���������
��˾�ڡ�2020��ȷǹ�������A�ɹ�ƱԤ�����жԱ��ηǹ������еķ��ս����˳�ֵĽ�ʾ������ļ���ʽ���Ŀ������Ԥ������ķ��ս������ص���ʾ�����б��η���ļͶ��Ŀ���ܴ��ڵ��ٴ��з����պ�������������¶���£�
������ļ���ʽ���Ҫ���ڡ���ҩ�з����з��豸������Ŀ������ҩ�з���Ŀ���������·��գ���������ļ���ʽ�Ͷ����Ŀ������Ԥ������ķ��ա�
��1�������
��ҩ�з�Ͷ������ڳ�������Ԥ�����ؽ϶࣬���з������кܿ���������Ч��ȷ������ȫ������ȶ���ԭ�����з�ʧ�ܣ��Ӷ������з����ա�
��2����������
��ҩ������ڽϳ���ʱ�䲻ȷ���Խ�ǿ��δ���������ߴ���һ���̶ȱ䶯�Ŀ��ܣ���˲�Ʒ�����ſ�����ȡ��ҩƷע���������������ɵķ��գ��Ӷ��������������ۡ���
���ϣ����η��е�ļͶ��Ŀ�������ش�ȷ���Է��գ��������ѳ����¶���η��е�ļ���ʽ���;�����Ϣ�Լ����ܴ��ڵ��ٴ��з����պ��������գ����η��еľ��߳�����ϡ���˾��������֤ȯ�����������а취������ط��ɷ��桢�淶���ļ�������˾�³̡��Ĺ涨�����η��в����������й�˾����С�ɶ�����������Ρ�
����������������ʦ�˲����
��һ���˲����
����������������������ʦ��ȡ�ĺ˲鷽ʽ�����������ڣ�
1����������˷����˱��η���ļ���ʽ�Ͷ����Ŀ��ص��ٴ��������ٴ�֪ͨ�顢�����������������о����桢CDE��ͨ���ϼ�����������ϣ�
2����ȡ�˷����˹���ļ���ʽ�Ͷ����ĿͶ�������ʱ��滮��
3����������ҩ�з����̺��з����յĽ������ϼ�ļ���ʽ�Ͷ����Ŀ��������ҩ�����Ʋ�Ʒ������������ļ���ʽ�Ͷ����Ŀ��չ����ؼ�����̸�˷�������ظ����ˡ�
�������˲����
���˲飬������������ʦ��Ϊ��
1�����η��е�ļͶ��Ŀ�Ѿ߱���չע�����ٴ��ı�Ҫ�����ļ���Ŀǰ������ҩ�з�����Ŀ�����ƻ��ƽ��У���չ˳�������������Լ�����ʱ���Ϊ��ȷ��
2���������з�ʵ��ǿ���з�����ḻ��ļͶ��Ŀ�е���ҩ�з�����Ŀ��Ϊע�����ٴ�����Ŀ��ļͶ��Ŀ�������ش�ȷ���Ե��ٴ��з����պ��������գ�
3�����������ڱ��ηǹ�������Ԥ���жԿ��ܴ��ڵ��ٴ��з����պ������������Գ����¶����ʾ�����������˶��»ᡢ�ɶ��������ͨ�������η��в����������й�˾����С�ɶ�����������Ρ�
���������4��
�����˱��η�����ļ���ʽ�10.02��Ԫ�����ڡ���ҩ�з����з��豸������Ŀ���Ͳ��������ʽ��������˲���˵������1������ļͶ��Ŀ����Ͷ���������ϸ��Ͷ������IJ������ݺͲ�����̣�����Ͷ�ʹ����Ƿ������ʱ���֧�����Ƿ���ļ���ʽ�Ͷ�롣��2��ļͶ��Ŀ���ʽ�ʹ�ú���Ŀ����Ľ��Ȱ��ţ�����ļ���ʽ��Ƿ�������η�����ض��»������ǰ��Ͷ���ʽ𡣣�3������ҩ�з����з��豸������Ŀ���з���ҩ�ľ���Ʒ�֡���;����ǰ��չ�����������ɵĹ����������еı�������������Ԥ������ʱ�䣬��Ϲ�˾��ҩ�з��������������ڹ�˾��ҩ�з�������ɱȹ�˾����ҩ����з����˵��ļͶ��Ŀ��ҩ�з��Ƿ����
�ش�ȷ���Է��գ��Կ��ܴ��ڵķ��ս����ش������ʾ����4��ļͶ��Ŀ��ز�Ʒ���г��ռ���������ٵľ���������Ƿ�����г����ز���Ԥ�ڵķ��ռ����ȡ��Ӧ�Դ�ʩ����5���з��豸��������Ҫ�豸������豸�����ı�Ҫ�ԡ�
�뱣�����������˲�������ظ���
һ������ļͶ��Ŀ����Ͷ���������ϸ��Ͷ������IJ������ݺͲ�����̣�����Ͷ�ʹ����Ƿ������ʱ���֧�����Ƿ���ļ���ʽ�Ͷ��
��һ������ļͶ��Ŀ����Ͷ���������ϸ��Ͷ������IJ������ݺͲ������
���ηǹ�������ļͶ��ĿΪ��ҩ�з����з��豸������Ŀ�Ͳ��������ʽ���Ŀ��ļ���ʽ�۳����з��ú�ȫ������������Ŀ��Ͷ�ʣ�
| ��� | ��Ŀ���� | ��Ŀ��Ͷ�ʽ�� ����Ԫ�� | ļ���ʽ�ʹ�ý�� ����Ԫ�� |
| 1 | ��ҩ�з����з��豸������Ŀ | 112,674.73 | 74,200.00 |
| 2 | ���������ʽ� | 26,000.00 | 26,000.00 |
| �ϼ� | 138,674.73 | 100,200.00 | |
���У���ҩ�з����з��豸������Ŀ��7����ҩ�з�����Ŀ���з��豸������Ŀ��ɣ�����Ŀ��Ͷ��Ϊ112,674.73��Ԫ�����й̶��ʲ�Ͷ�ʺϼ�7,320.58��Ԫ����ҩ�з�Ͷ��ϼ�105,354.15��Ԫ������Ŀ��ʹ��ļ���ʽ�74,200.00��Ԫ��
| ��� | Ͷ����� | Ͷ�ʽ�� ����Ԫ�� | ��ʹ��ļ���ʽ���Ԫ�� | �ʱ������� |
| 1 | ��ҩ�з�Ͷ�� | 105,354.15 | 66,879.42 | 100% |
| 1.1 | X-396����ALK����NSCLC���������ٴ����� | 6,851.35 | 892.17 | 100% |
| 1.2 | X-396����ALK����NSCLCһ�������ٴ����� | 14,267.00 | 4,680.77 | 100% |
| ��� | Ͷ����� | Ͷ�ʽ�� ����Ԫ�� | ��ʹ��ļ���ʽ���Ԫ�� | �ʱ������� |
| 1.3 | CM082���������ٴ���/���� | 17,689.58 | 11,793.90 | 100% |
| 1.4 | CM082����JS001����ճĤ��ɫ���������ٴ����� | 10,577.10 | 10,448.82 | 100% |
| 1.5 | MIL60����״ϸ����Сϸ���ΰ������ٴ����� | 23,613.77 | 10,758.12 | 100% |
| 1.6 | BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ����� | 17,646.10 | 13,853.81 | 100% |
| 1.7 | BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/���� | 14,709.25 | 14,451.83 | 100% |
| 2 | �з��豸���� | 7,320.58 | 7,320.58 | 100% |
| �ϼ� | 112,674.73 | 74,200.00 | 100% | |
���ϸ�����ҩ�з���Ŀ��������ҩ����ǰ���һ���ٴ��������Ŀ����ע�����ٴ��������Ŀ��������Ŀ��Ͷ���ܶ��������Ŀ��Ӧ�ٴ���������������������ɺ����������ڼ��Ͷ�ʽ�
������Ͷ������IJ������ݺͲ������
1����ҩ�з����з��豸������Ŀ
��1����ҩ�з���Ŀ
1.1��X-396����ALK����NSCLC���������ٴ�����
| ��Ŀ | ���� | Ͷ�ʶ� ����Ԫ�� | ��ע |
| �ٴ�ʵ�鲿��������� | �ٴ������ | 2,430.00 | �����������ѡ��о��߹۲�ѡ����Ʒѡ�Ѫ���ɼ������ѡ������豸�ѡ�ҽԺ�����ѵȣ� ��������ƽ�⣨C14�������������ѡ��о��߹۲�ѡ����Ʒѡ�Ѫ���ɼ������ѡ������豸�ѡ��о����ĵĹ����ѵȣ� ʳ��ҩ�������������ѡ��о��߹۲�ѡ����Ʒѡ�Ѫ���ɼ������ѡ������豸�ѡ��о����ĵĹ����ѵ� |
| ��Ŀ | ���� | Ͷ�ʶ� ����Ԫ�� | ��ע |
| SMO���ٴ������ֳ�������֯���ȵ���������� | 1,906.35 | II���ٴ����ݹ�����ͳ�Ʒѡ��ٴ��о�Э������ѡ������������ѡ����շѡ�������Ӱ�������ѣ� X396-��������ƽ�⣨C14����������ļ�ѡ�������Ʒѡ�����д�ѡ��ٴ����ݹ�����ͳ�Ʒѡ����ѡ����շѡ��ٴ��о�Э������ѣ� ʳ��ҩ���ٴ����ݹ�����ͳ�Ʒѡ����ѡ����շѡ��ٴ��о�Э������� | |
| ���� | 445.00 | ������Ա���á��������ʡ�����ӡˢ���������䡢�о����顢ҩƷע��� | |
| �� | 4,781.35 | ||
| �ٴ���ҩ��������ط��� | �ٴ���ҩ | 1,560.00 | �ٴ����鼰�걨�����Ʒ���������ã�����ԭ���ϡ��IJġ����ġ���Ʒ���� |
| �ȶ��о� | 380.00 | �ٴ������ڼ䣺ÿ��ǰ3�����г����ȶ��Կ��죻ÿ�ι����Ż��������г��ڡ������ȶ��Կ��죻 ҩƷע����/������֤����ÿ�����г��ڡ������ȶ��Կ��죻 ��ҩ����ȶ��Խ����о�������֧��ϵ����ҩƷ�ȶ����о��ļ����õ� | |
| �������� | 130.00 | �����豸���Է��á����������жԸ����豸���м��Ʒ��ԭ�����ϵ�ȷ�Ϻ���֤���á����ͼ����Ʒ������õ� | |
| �� | 2,070.00 | ||
| �ϼ� | 6,851.35 | ||
1.2 X-396����ALK����NSCLCһ�������ٴ�����
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| �ٴ�ʵ�鲿��������� | ����ҩ���� | 4,912.00 | ����ҩ�������� |
| �ٴ������ | 1,790.00 | �����о��߹۲�ѡ����Ʒѡ��������ѡ�Ѫ���ɼ������ѵȣ� ��ת�ư����о��߹۲�ѡ����Ʒѡ��������ѡ�Ѫ���ɼ������ѵ� | |
| SMO���ٴ������ֳ�������֯���ȵ���������� | 3,510.00 | III���ٴ��о�Э������ѡ��ٴ���Ŀ������������ѡ����շѡ��ʿطѵȵ���������ѣ� ��ת���ٴ����ݹ�����ͳ�Ʒѡ����շѡ����ѡ�������Ӱ�������ѡ��ٴ��о�Э������� | |
| ���� | 375.00 | ������Ա���á��������ʡ�����ӡˢ���������䡢�ļ����롢�о����顢ҩƷע��� |
| �� | 10,587.00 | ||
| �ٴ���ҩ��������ط��� | �ٴ���ҩ | 2,230.00 | �ٴ����鼰�걨�����Ʒ���������ã�����ԭ���ϡ��IJġ����ġ���Ʒ���� |
| �ȶ��о� | 890.00 | �ٴ������ڼ䣺ÿ��ǰ3�����г����ȶ��Կ��죻ÿ�ι����Ż��������г��ڡ������ȶ��Կ��죻 ҩƷע����/������֤����ÿ�����г��ڡ������ȶ��Կ��죻 ��ҩ����ȶ��Խ����о�������֧��ϵ����ҩƷ�ȶ����о��ļ����õȣ� ҩ��һ�����о� | |
| �������� | 560.00 | �������ͼ����Ʒ������á��豸���Է��á����������жԸ����豸���м��Ʒ��ԭ�����ϵ�ȷ�Ϻ���֤���õ� | |
| �� | 3,680.00 | ||
| �ϼ� | 14,267.00 | ||
1.3 CM082���������ٴ���/����
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| �ٴ�ʵ�鲿��������� | ����ҩ���� | 3,250.00 | ����ҩ��άĪ˾ |
| �ٴ������ | 4,812.00 | �����о��߹۲�ѡ����Ʒѡ�ʵ���Ҽ��ѡ�Ӱ��ѧ���ѡ�Ӱ�������ѵ��ٴ�������ط��ã� ��������ƽ�⣨C14�������о��߹۲�ѡ����Ʒѡ�ʵ���Ҽ��ѡ�Ӱ��ѧ���ѡ�Ӱ�������ѵ��ٴ�������ط��� | |
| SMO���ٴ������ֳ�������֯���ȵ���������� | 3,319.00 | III���ٴ����ݹ�����ͳ�Ʒѡ��ٴ���Ŀ������������ѡ��ٴ��о�Э������ѡ�������Ӱ�������ѡ�ҩ������������������ȷ���ѣ� CM082-��������ƽ�⣨C14���ٴ����ݹ�����ͳ�Ʒѡ����ѡ����շѡ��ٴ��о�Э������ѡ���������ļ�ѡ������������ѡ�������Ʒѡ�����д�� | |
| ���� | 440.00 | ������Ա���á��������ʡ�����ӡˢ���������䡢�о����顢ҩƷע��� | |
| �� | 11,821.00 | ||
| �ٴ���ҩ��������ط��� | �ٴ���ҩ | 4,708.58 | �ٴ����鼰�걨�����Ʒ���������ã�����ԭ���ϡ��IJġ����ġ���Ʒ���� |
| �ȶ��о� | 580.00 | �ٴ������ڼ䣺ÿ��ǰ3�����г����ȶ��Կ��죻ÿ�ι����Ż��������г��ڡ������ȶ��Կ��죻 ҩƷע����/������֤����ÿ�����г��ڡ������ȶ��Կ��죻 ��ҩ����ȶ��Խ����о�������֧��ϵ����ҩƷ�ȶ����о��ļ����õ� | |
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| �������� | 580.00 | �������ͼ����Ʒ������á��豸���Է��á����������жԸ����豸���м��Ʒ��ԭ�����ϵ�ȷ�Ϻ���֤���õ� | |
| �� | 5,868.58 | ||
| �ϼ� | 17,689.58 | ||
1.4 CM082����JS001����ճĤ��ɫ���������ٴ�����
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| �ٴ�ʵ�鲿��������� | �ٴ������ | 3,147.80 | �����������ѡ��о��߹۲�ѡ����Ʒѡ�������Ƭ����ѡ����̺����������ѡ�ҽԺ�����ѵ� |
| SMO���ٴ������ֳ�������֯���ȵ���������� | 3,865.10 | III���ٴ����ݹ�����ͳ�Ʒѡ��ٴ���Ŀ������������ѡ��ٴ��о�Э������ѡ����շѡ����ѡ������������ | |
| ���� | 459.20 | ������Ա���á��������ʡ�����ӡˢ���������䡢�ļ���ݡ�SAE/AE���á��о����顢ҩƷע��� | |
| �� | 7,472.10 | ||
| �ٴ���ҩ��������ط��� | �ٴ���ҩ | 1,945.00 | �ٴ����鼰�걨�����Ʒ���������ã�����ԭ���ϡ��IJġ����ġ���Ʒ���� |
| �ȶ��о� | 580.00 | �ٴ������ڼ䣺ÿ��ǰ3�����г����ȶ��Կ��죻ÿ�ι����Ż��������г��ڡ������ȶ��Կ��죻 ҩƷע����/������֤����ÿ�����г��ڡ������ȶ��Կ��죻 ��ҩ����ȶ��Խ����о�������֧��ϵ����ҩƷ�ȶ����о��ļ����õ� | |
| �������� | 580.00 | �������ͼ����Ʒ������á��豸���Է��á����������жԸ����豸���м��Ʒ��ԭ�����ϵ�ȷ�Ϻ���֤���õ� | |
| �� | 3,105.00 | ||
| �ϼ� | 10,577.10 | ||
1.5 MIL60����״ϸ����Сϸ���ΰ������ٴ�����
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| �ٴ�ʵ�鲿��������� | ����ҩ���� | 8,048.00 | ����ҩ��ά͡ |
| ����ҩƷ���� | 283.61 | ��ɼ���Ϳ��� |
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| �ٴ������ | 5,757.00 | �����������ѡ����Ʒѡ��о��߹۲�ѡ������ѡ�ҽԺ�����ѵ� | |
| SMO���ٴ������ֳ�������֯���ȵ���������� | 4,915.00 | Ⱥ��ҩ��PK��PD���ѡ����շѡ��ٴ���Ŀ������������ѡ��ٴ��о�Э������ѡ�������Ӱ�������ѵ� | |
| ���� | 480.16 | ������Ա���á��������ʡ�����ӡˢ���������䡢�ļ���ݡ�SAE/AE���á��о����顢ҩƷע��� | |
| �� | 19,483.77 | ||
| �ٴ���ҩ��������ط��� | ���� | 4,130.00 | �ٴ����鼰�걨�����Ʒ���������ã�����ԭ���ϡ��IJġ����ġ���Ʒ���� |
| �� | 4,130.00 | ||
| �ϼ� | 23,613.77 | ||
1.6 BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ�����
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| �ٴ�ʵ�鲿��������� | �ٴ������ | 7,381.34 | �����������ѡ��о��߹۲�ѡ�ҽԺ�����ѵȣ� D0316-��������ƽ�⣨C14�������о��߹۲�ѡ����Ʒѡ�ʵ���Ҽ��ѡ�Ӱ��ѧ���ѡ�Ӱ�������ѵ��ٴ�������ط��� |
| SMO���ٴ������ֳ�������֯���ȵ���������� | 4,563.57 | II���ٴ��о�Э������ѡ��ٴ���Ŀ������������ѡ��ٴ����ݹ�����ͳ�Ʒѡ��Ŵ����������ѡ����շѡ�������ѡ�Ѫ������������ѡ�������Ӱ�������ѡ�������ҩƷ�����ѡ��������������ѵȣ� D0316-��������ƽ�⣨C14�������ٴ����ݹ�����ͳ�Ʒѡ����ѡ����շѡ��ٴ���Ŀ������������ѡ����ʷ��á���������ļ�ѡ���������Ʒ�����ѡ�����д�� | |
| ���� | 431.19 | ������Ա���á��������ʡ�����ӡˢ���������䡢�ļ���ݡ�SAE/AE���á��о����顢ҩƷע��� | |
| �� | 12,376.10 | ||
| �ٴ���ҩ��������ط��� | �ٴ���ҩ | 4,130.00 | �ٴ����鼰�걨�����Ʒ���������ã�����ԭ���ϡ��IJġ����ġ���Ʒ���� |
| �ȶ��о� | 590.00 | �ٴ������ڼ䣺ÿ��ǰ3�����г����ȶ��Կ��죻ÿ�ι����Ż��������г��ڡ������ȶ��Կ��죻 | |
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| ҩƷע����/������֤����ÿ�����г��ڡ������ȶ��Կ��죻 ��ҩ����ȶ��Խ����о�������֧��ϵ����ҩƷ�ȶ����о��ļ����õȡ� | |||
| �������� | 550.00 | �������ͼ����Ʒ������á��豸���Է��á����������жԸ����豸���м��Ʒ��ԭ�����ϵ�ȷ�Ϻ���֤���õ� | |
| �� | 5,270.00 | ||
| �ϼ� | 17,646.10 | ||
1.7 BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/����
| ��Ŀ | ���� | Ͷ�ʶ��Ԫ�� | ��ע |
| �ٴ�ʵ�鲿��������� | ����ҩ���� | 256.00 | ����ҩ������ |
| �ٴ������ | 5,282.56 | �����о��߹۲�ѡ��������ѡ�ǣͷ�ѡ�ҽԺ�����ѵ� | |
| SMO���ٴ������ֳ�������֯���ȵ���������� | 4,489.61 | �������շѡ�������ѡ��������������ѡ�������Ӱ�������ѡ��ٴ��о�Э������ѡ��ٴ���Ŀ������������ѡ��ٴ����ݹ�����ͳ�Ʒѡ�FACT-L��Ȩ�ѡ�IDMCίԱ����� | |
| ���� | 426.09 | ������Ա���á��������ʡ�����ӡˢ���������䡢�ļ���ݡ�SAE/AE���á��о����顢ҩƷע��� | |
| �� | 10,454.25 | ||
| �ٴ���ҩ��������ط��� | �ٴ���ҩ | 3,085.00 | �ٴ����鼰�걨�����Ʒ���������ã�����ԭ���ϡ��IJġ����ġ���Ʒ���� |
| �ȶ��о� | 590.00 | �ٴ������ڼ䣺ÿ��ǰ3�����г����ȶ��Կ��죻ÿ�ι����Ż��������г��ڡ������ȶ��Կ��죻 ҩƷע����/������֤����ÿ�����г��ڡ������ȶ��Կ��죻 ��ҩ����ȶ��Խ����о�������֧��ϵ����ҩƷ�ȶ����о��ļ����õ� | |
| �������� | 580.00 | �������ͼ����Ʒ������á��豸���Է��á����������жԸ����豸���м��Ʒ��ԭ�����ϵ�ȷ�Ϻ���֤���õ� | |
| �� | 4,255.00 | ||
| �ϼ� | 14,709.25 | ||
��2���з��豸����
��˾��Ա����з����ĺͺ����з����ĵ��з��豸��������Ͷ����ֱ�Ϊ2,984.93��Ԫ��4,335.65��Ԫ������7,320.58��Ԫ���з��豸��������ϸͶ�ʲ������£�
�����з����ĵ��豸������Ŀ��ϸ���£�
| �з����ģ������� | ||||
| ���� | ʹ�ò��� | ���� | ���ۣ���Ԫ�� | ����Ԫ�� |
| ҩ���ȶ��������� | ������ | 1 | 20.00 | 20.00 |
| ��ЧҺ��ɫ���� | 2 | 45.00 | 90.00 | |
| ����ЧҺ��ɫ���� | 2 | 60.00 | 120.00 | |
| ������ | 2 | 1.00 | 2.00 | |
| ���� | 2 | 0.50 | 1.00 | |
| ϴƿ�� | 2 | 25.00 | 50.00 | |
| ˮԡ�� | 2 | 0.50 | 1.00 | |
| ����ɫ������������ | 1 | 150.00 | 150.00 | |
| ����ɫ���� | 1 | 60.00 | 60.00 | |
| �����ϵ������������� | 1 | 120.00 | 120.00 | |
| ����ɫ���� | 1 | 120.00 | 120.00 | |
| ������ | 1 | 22.00 | 22.00 | |
| watersArc����ЧҺ��ɫ���� | 4 | 42.00 | 168.00 | |
| �� | 22 | - | 924.00 | |
| ��װ�� | �Ƽ��� | 1 | 25.00 | 25.00 |
| ������ƽ | 2 | 1.50 | 3.00 | |
| С��̨�� | 2 | 1.00 | 2.00 | |
| ȫ�Զ�ȡ���ܳ��� | 2 | 40.00 | 80.00 | |
| ������� | 1 | 15.00 | 15.00 | |
| ��ϻ��϶� | 1 | 2.00 | 2.00 | |
| �������� | 1 | 40.00 | 40.00 | |
| �豸��� | 1 | 15.00 | 15.00 | |
| �� | 11 | - | 182.00 | |
| �������ʲ����� | �������� �Ƽ��� | 1 | 10.00 | 10.00 |
| Ӳ���� | 1 | 7.00 | 7.00 | |
| �ܷ��Լ���� | 1 | 1.00 | 1.00 | |
| ��ϻ� | 1 | 20.00 | 20.00 | |
| �������� | 1 | 70.00 | 70.00 | |
| �� | 5 | - | 108.00 | |
| 96�װ�綯��Һ�� | ҩ���� | 12 | 1.20 | 14.40 |
| 384�װ�綯��Һ�� | 6 | 2.80 | 16.80 | |
| �з����ģ������� | ||||
| ���� | ʹ�ò��� | ���� | ���ۣ���Ԫ�� | ����Ԫ�� |
| ӫ������ | 2 | 35.00 | 70.00 | |
| ��Drop?�� | 1 | 3.00 | 3.00 | |
| ��ͨPCR�� | 2 | 6.00 | 12.00 | |
| WBתĤϵͳ | 2 | 1.00 | 2.00 | |
| ��ͨ��WBϵͳ | 2 | 3.00 | 6.00 | |
| Һ��ɫ������������ | 2 | 260.00 | 520.00 | |
| ��ѹ����� | 1 | 10.00 | 10.00 | |
| ��������̨ | 1 | 2.00 | 2.00 | |
| ��ƽ�����֮һ�� | 3 | 1.50 | 4.50 | |
| ø����EnVision���Ƕ���ϵͳ2105-0010 | 1 | 120.00 | 120.00 | |
| ����������Ӿϵͳ | 1 | 3.50 | 3.50 | |
| �� | 36 | - | 784.20 | |
| 3L��ת������ | �ϳ��� | 10 | 3.50 | 35.00 |
| 20L��ת������ | 1 | 2.00 | 2.00 | |
| ��ȴѭ���� | 5 | 2.00 | 10.00 | |
| ��ȴѭ���ã���20L������ | 1 | 5.00 | 5.00 | |
| ���������� | 30 | 0.80 | 24.00 | |
| ��Ĥ�� | 15 | 1.50 | 22.50 | |
| ���ϳ��� | 3 | 25.00 | 75.00 | |
| ��ѹ�Ʊ��� | 10 | 15.00 | 150.00 | |
| 50L������Ӧ�� | 2 | 4.00 | 8.00 | |
| 20L������Ӧ�� | 1 | 4.00 | 4.00 | |
| ������ƽ�����֮һ�� | 8 | 1.50 | 12.00 | |
| ���������� | 20 | 0.10 | 2.00 | |
| ���ˮ�� | 30 | 0.20 | 6.00 | |
| �����Ʊ�Һ�� | 2 | 80.00 | 160.00 | |
| �ͱ� | 3 | 3.00 | 9.00 | |
| Һ��ɫ������������ | 3 | 100.00 | 300.00 | |
| ɫ���� | 8 | 3.00 | 24.00 | |
| ����ɫ���� | 6 | 5.00 | 30.00 | |
| ʵ�����ͷ�ϵͳ���� | 1 | 70.00 | 70.00 | |
| LCMS-2020������Һ��ɫ������������ | 1 | 15.05 | 15.05 | |
| YMC KSA99S05-2530WXF�Ʊ������� | 2 | 11.59 | 23.18 | |
| �� | 162 | - | 986.73 | |
| �з����ģ������� | ||||
| ���� | ʹ�ò��� | ���� | ���ۣ���Ԫ�� | ����Ԫ�� |
| �ϼ� | 2,984.93 | |||
�����з����ĵ��豸������Ŀ��ϸ���£�
| �з����ģ����ݣ� | ||||
| ���� | ʹ�ò��� | ���� | ���ۣ���Ԫ�� | ����Ԫ�� |
| ���»� | �Ƽ��� | 1 | 20.00 | 20.00 |
| ������ƽ | 3 | 1.50 | 4.50 | |
| ������ | 1 | 60.00 | 60.00 | |
| ���ۼ����� | 1 | 200.00 | 200.00 | |
| nano-milling������ĥ�� | 1 | 100.00 | 100.00 | |
| ������� | 1 | 15.00 | 15.00 | |
| �� | 8 | - | 399.50 | |
| ����ЧҺ��ɫ����UPLC | ������ | 2 | 65.00 | 130.00 |
| ����ɫ���� | 1 | 120.00 | 120.00 | |
| Һ��ɫ������������ | 1 | 150.00 | 150.00 | |
| watersArc����ЧҺ��ɫ���� | 4 | 30.24 | 120.96 | |
| ҩƷ�ȶ���ʵ���� | 2 | 15.00 | 30.00 | |
| �������նȼ�¼�� | 1 | 3.00 | 3.00 | |
| ����� | 1 | 3.00 | 3.00 | |
| ��ո����� | 1 | 1.00 | 1.00 | |
| ���� | 4 | 0.50 | 2.00 | |
| �� | 17 | - | 559.96 | |
| Һ��ɫ������������ | �ϳɲ� | 4 | 100.00 | 400.00 |
| ���������� | 6 | 15.00 | 90.00 | |
| UPS��Դ | 10 | 3.00 | 30.00 | |
| 20L��ת������ | 10 | 4.00 | 40.00 | |
| ��ȴѭ���ã���20L������ | 10 | 6.00 | 60.00 | |
| ��ȴѭ���� | 10 | 5.00 | 50.00 | |
| ��Ĥ�� | 5 | 3.00 | 15.00 | |
| ���ϳ��� | 2 | 25.00 | 50.00 | |
| ��ѹ�Ʊ��� | 2 | 15.00 | 30.00 | |
| ��ƽ�����֮һ�� | 10 | 1.50 | 15.00 | |
| ���������� | 10 | 1.00 | 10.00 | |
| ���ˮ�� | 10 | 1.00 | 10.00 | |
| �ͱ� | 10 | 3.00 | 30.00 | |
| ɫ���� | 10 | 3.00 | 30.00 | |
| ��ʽƫ������ | 1 | 132.00 | 132.00 | |
| �з����ģ����ݣ� | ||||
| ���� | ʹ�ò��� | ���� | ���ۣ���Ԫ�� | ����Ԫ�� |
| ҩ���з����ܽᾧƽ̨ | 1 | 20.50 | 20.50 | |
| ���� | 5 | 0.50 | 2.50 | |
| �� | 116 | - | 1,015.00 | |
| �������������� | ����Ӳ� | 1 | 274.00 | 274.00 |
| ҡ����CO2�� | 3 | 28.00 | 84.00 | |
| AKTA���״���ϵͳ | 1 | 118.00 | 118.00 | |
| �ӹܻ� | 1 | 21.00 | 21.00 | |
| ��ܻ� | 1 | 14.50 | 14.50 | |
| ����ЧҺ��ɫ���� | 1 | 48.00 | 48.00 | |
| �������� | 1 | 4.20 | 4.20 | |
| С�ͷ��� | 3 | 30.00 | 90.00 | |
| ��������� | 1 | 150.00 | 150.00 | |
| Ѫ������� | 1 | 20.00 | 20.00 | |
| ��ܻ� | 1 | 25.00 | 25.00 | |
| ��ѹ����� | 1 | 20.00 | 20.00 | |
| ���ﰲȫ�� | 1 | 7.50 | 7.50 | |
| ȫ������ëϸ�ܡ��ȵ�۽� | 1 | 150.00 | 150.00 | |
| �����±��� | 1 | 10.00 | 10.00 | |
| Һ����(Tank) | 4 | 5.00 | 20.00 | |
| �Ʊ����Ļ� | 1 | 60.00 | 60.00 | |
| ���±��䣨-20�ȣ� | 2 | 8.00 | 16.00 | |
| �����䣨CO2�� | 2 | 8.00 | 16.00 | |
| �� | 28 | - | 1,148.20 | |
| �����±��� | ҩ���� | 1 | 10.00 | 10.00 |
| ������Һ�� | 57 | 0.20 | 11.40 | |
| �����Һ�� | 19 | 0.40 | 7.60 | |
| 96����Һ����վ | 4 | 48.00 | 192.00 | |
| ���� | 1 | 76.82 | 76.82 | |
| ���ﰲȫ�� | 3 | 5.00 | 15.00 | |
| �Ʊ����Ļ� | 3 | 25.22 | 75.65 | |
| ���±��䣨-20�ȣ� | 3 | 2.07 | 6.21 | |
| ������̼������ | 3 | 4.83 | 14.50 | |
| ����ԡ | 5 | 4.00 | 20.00 | |
| Envision alpha��� | 1 | 25.00 | 25.00 | |
| ���ﰲȫ�� | 4 | 6.00 | 24.00 | |
| ��������ӡ����װ | 3 | 2.00 | 6.00 | |
| ��Һǹ | 10 | 3.00 | 30.00 | |
| �з����ģ����ݣ� | ||||
| ���� | ʹ�ò��� | ���� | ���ۣ���Ԫ�� | ����Ԫ�� |
| ϸ������ | 2 | 8.00 | 16.00 | |
| ���Ļ�ת�� | 4 | 2.00 | 8.00 | |
| Һ���� | 3 | 3.60 | 10.80 | |
| ˫ɫ��������ϵͳ | 1 | 65.00 | 65.00 | |
| �� | 127 | - | 613.99 | |
| ȫ�Զ���Һ����վ | ҩ������ѧ�� | 2 | 30.00 | 60.00 |
| 96������ | 1 | 13.00 | 13.00 | |
| Һ��ɫ������������ | 2 | 260.00 | 520.00 | |
| ���±��䣨-20�ȣ� | 2 | 3.00 | 6.00 | |
| �� | 7 | - | 599.00 | |
| �ϼ� | 4,335.65 | |||
2�����������ʽ�
����2019��12��31�գ���˾���д��5.21��Ԫ�����ڸ�ծ3.63��Ԫ����˾����Ͷ���ر������������ֽ�ֺ죬2020�����2019����ֽ����0.76��Ԫ��
��1����˾�з����µ���Ҫ
��ҩ�з��ǹ�˾�ĺ��ľ���������˾�з�Ͷ����������2017���з�Ͷ��
3.81��Ԫ��2018���з�Ͷ��5.90��Ԫ��2019���з�Ͷ��6.75��Ԫ���з�Ͷ����Ҫ��Դ�������ʽ�Ŀǰ��˾�з���Ŀ�ߴ�30����������ٴ��ε�Ʒ���������ӣ�����2020��4��30�գ���˾����13����Ʒ�����ٴ��Σ��Ҷ����Ŀ��������ǰ���һ���ٴ��μ�ע�����ٴ��Σ���˾�����ƶ���ɳ�����������ٴ��о���ע�ᡣ����֮�⣬��˾�������ִ��������ҩ���з������������˶��������з���Ŀ�������ƽ��з������Ź�˾�з����߲��Ϸḻ��δ����������ٴ��������Ŀ���������ӣ����Т����ر��Ǣ����ٴ���Ŀ�������ٴ�������Ŀ�Լ�������з���Ŀ�������ʽ����ϴ�Ԥ��δ�����깫˾���з�Ͷ���Խ����ֽϿ���������Ҫ���������ʽ�
��2�������������۲��������Լ���ɳ���������������۵���Ҫ
2019�꣬�����������۶��15��Ԫ�����ٳ���20%�����Ű���������Ӧ֢�����������ỹ�����ֽϿ��������ͬʱһ����ҩ��ɳ���Ὣ��2020��
�������У���������֯���������ۣ���Ҫ����һ���������ʽ𡣱��ηǹ�������ļ���ʽ����ڲ��������ʽ�2.60��Ԫ��ռ����ļ���ʽ��ܶ��
25.95%��δ��������ļ���ʽ��ܶ��30%��
����������Ͷ�ʹ����Ƿ������ʱ���֧�����Ƿ���ļ���ʽ�Ͷ���MIL60��Ŀ�⣬���ϸ�����ҩ�з���Ŀ�IJ�Ʒ��Ϊ����һ����ҩ��������ҩ����ǰ���һ���ٴ�����μ�ע�����ٴ��������Ŀ��MIL60��ĿΪ��������ҩ�Ģ����ٴ�����Ŀ�����չ�˾�Ļ�����ߣ�����������ҩ�з���Ŀ��Ͷ�ʾ�Ϊ�����ε�Ͷ�ʣ������ʱ�������������ˣ����˲��������ʽ���Ŀ�⣬��ҩ�з���Ŀ���з��豸������Ŀ��Ͷ�ʾ�Ϊ�ʱ���֧�������в���Ͷ�ʲ���ļ���ʽ�Ͷ�롣
����ļͶ��Ŀ���ʽ�ʹ�ú���Ŀ����Ľ��Ȱ��ţ�����ļ���ʽ��Ƿ�������η�����ض��»������ǰ��Ͷ���ʽ�
��һ��ļͶ��Ŀ����Ľ��Ȱ���
| ��� | Ͷ����� | �걨/Ԥ���걨NDA/BLAʱ�� | Ԥ����Ŀ��ɣ�����������ɣ�ʱ�� |
| 1 | ��ҩ�з�Ͷ�� | ||
| 1.1 | X-396����ALK����NSCLC���������ٴ����� | 2018�� | 2020�� |
| 1.2 | X-396����ALK����NSCLCһ�������ٴ����� | 2021�� | 2022�� |
| 1.3 | CM082���������ٴ���/���� | 2021�� | 2021�� |
| 1.4 | CM082����JS001����ճĤ��ɫ���������ٴ����� | 2023�� | 2023�� |
| 1.5 | MIL60����״ϸ����Сϸ���ΰ������ٴ����� | 2020�� | 2021�� |
| 1.6 | BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ����� | 2021�� | 2022�� |
| 1.7 | BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/���� | 2022�� | 2023�� |
| 2 | �з��豸���� | 2020�꿪ʼ���� | 2023����� |
����������ļͶ��Ŀ���ʽ�ʹ�����
���������˶��»�����գ�2020��3��3�գ�������ļͶ��Ŀ��Ͷ���ʣ��Ͷ�ʽ�����ʹ��ļ���ʽ������±���ʾ��
| ��� | Ͷ����� | Ͷ�ʽ���Ԫ�� | ���»�Ԥ��ǰ�Ľ�չ��� | ���»�Ԥ��ǰ��Ͷ�����Ԫ�� | ʣ��Ͷ�ʽ���Ԫ�� | ��ʹ��ļ���ʽ���Ԫ�� |
| 1 | ��ҩ�з�Ͷ�� | 105,354.15 | 38,384.08 | 66,970.08 | 66,879.42 | |
| 1.1 | X-396����ALK����NSCLC���������ٴ����� | 6,851.35 | CDE�����У�����ҩѧ�о������� | 5,868.52 | 982.83 | 892.17 |
| 1.2 | X-396����ALK����NSCLCһ�������ٴ����� | 14,267.00 | ����ɢ����ٴ��������� | 9,586.23 | 4,680.77 | 4,680.77 |
| 1.3 | CM082���������ٴ���/���� | 17,689.58 | ����ɢ�/�����ٴ��������� | 5,895.68 | 11,793.90 | 11,793.90 |
| 1.4 | CM082����JS001����ճĤ��ɫ���������ٴ����� | 10,577.10 | �չ�����ٴ����� | 128.28 | 10,448.82 | 10,448.82 |
| 1.5 | MIL60����״ϸ����Сϸ���ΰ������ٴ����� | 23,613.77 | �ѻ�����ɢ����ٴ��������� | 12,855.65 | 10,758.12 | 10,758.12 |
| 1.6 | BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ����� | 17,646.10 | �����ٴ����������� | 3,792.29 | 13,853.81 | 13,853.81 |
| 1.7 | BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/���� | 14,709.25 | ��/�����ٴ����������� | 257.42 | 14,451.83 | 14,451.83 |
| 2 | �з��豸���� | 7,320.58 | 0 | 7,320.58 | 7,320.58 | |
| �ϼ� | 112,674.73 | 38,384.08 | 74,290.65 | 74,200.00 | ||
����������ļ���ʽ��Ƿ�������η�����ض��»������ǰ��Ͷ���ʽ�
���ϱ���֪������ļ���ʽ������η��ж��»������ǰ���ʽ�Ͷ�롣
��������ҩ�з����з��豸������Ŀ���з���ҩ�ľ���Ʒ�֡���;����ǰ��չ�����������ɵĹ����������еı�������������Ԥ������ʱ�䣬��Ϲ�˾��ҩ�з��������������ڹ�˾��ҩ�з�������ɱȹ�˾����ҩ����з����˵��ļͶ��Ŀ��ҩ�з��Ƿ�����ش�ȷ���Է��գ��Կ��ܴ��ڵķ��ս����ش������ʾ
��һ������ҩ�з����з��豸������Ŀ���з���ҩ�ľ���Ʒ�֡���;����ǰ��չ�����������ɵĹ����������еı�������������Ԥ������ʱ��
��ѧ��ҩ���з���һ����Ϊ���ӵĹ��̣������������ưб�Ļ����о���ȷ�ϣ���б����Ӧ�Ļ�ѧ���ӵ���ƺͻ�ѧ�ϳɣ��ȵ��������������������ģ�ͺͷ���ѧ�Ľ������ٴ�ǰ����ҩЧ��ҩ����������ҩ������ѧ�о����Ƽ�ѧ�о����Լ�����I�ڡ�II�ڡ�III���ٴ������о����걨NDA�����ҩ�ಿ�ŵ�����
��������������ظ���������գ�����ҩ�з����з��豸������Ŀ���з���ҩ�ľ���Ʒ�֡���;����ǰ��չ�����������ɵĹ����������еı�������������Ԥ������ʱ�����±���ʾ��
| ��� | �з���Ŀ | ��Ʒ��� | ��; | ��չ��� | ������ɵĹ��� | Ԥ�ƻ����������ʱ�� |
| 1.1 | X-396����ALK����NSCLC���������ٴ����� | ��ɳ���ᣬ�ڶ������ALK���ԵĿڷ����Ƽ�����ҩ1�� | ����ʹ�ÿ����������ƺ���ҩ���չ��ALK���Ե����ڷ�Сϸ���ΰ��������� | CDE�����У��ѵݽ�ҩѧ������� | ���CDE����ͨ�� | 2020�� |
| 1.2 | X-396����ALK����NSCLCһ�������ٴ����� | ����ALK���Ե����ڷ�Сϸ���ΰ������� | �����ٴ�������ɻ������� | ��ɢ����ٴ����飬�걨NDA ������ͨ�� | 2022�� | |
| 1.3 | CM082���������ٴ���/���� | Vorolanib����е������Ұ��ἤø��RTKs�����Ƽ�����ҩ1�� | ���ڼ���VEGFR-TKIһ������ʧ�ܵ�ת�������� | ��/�����ٴ�������ɻ������� | ��ɢ�/�����ٴ����飬�걨NDA ������ͨ�� | 2021�� |
| 1.4 | CM082����JS001����ճĤ��ɫ���������ٴ����� | ���ھֲ���չ��ת����ճĤ��ɫ���������� | �չ�����ٴ� | ���III���ٴ����飬�걨NDA ������ͨ�� | 2023�� | |
| 1.5 | MIL60����״ϸ����Сϸ���ΰ������ٴ����� | ������������ά͡����������ҩ��VEGF���Ƽ� | �������ڻ��Է���״ϸ����Сϸ���ΰ������� | �걨BLA������� | ���CDE����ͨ�� | 2021�� |
| ��� | �з���Ŀ | ��Ʒ��� | ��; | ��չ��� | ������ɵĹ��� | Ԥ�ƻ����������ʱ�� |
| 1.6 | BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ����� | ������EGFR�ڷ����Ƽ�����ҩ1�� | ����ʹ�� EGFR���Ƽ���ҩ�����T790Mͻ��ľֲ����ڻ�ת���Է�Сϸ���ΰ������� | �����ٴ������������� | ��ɢ����ٴ����飬�걨NDA ������ͨ�� | 2022�� |
| 1.7 | BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/���� | ����EGFRͻ��ľֲ����ڻ�ת���Է�Сϸ���ΰ������� | ��/�����ٴ������������� | ��ɢ�/�����ٴ����飬�걨NDA������ͨ�� | 2023�� |
�ٴ������ҩƷע����������ܲ��������ٶȡ�ҩ���ٴ����֡�ҩЧ����ָ�ꡢCDE�����ٶ��Լ�ҩ���������ߵ����ص�Ӱ�졣��˾����ļͶ��Ŀ��Ϊ��ҩ��������ǰ�����һ���ٴ�����μ�ע�����ٴ�����Ŀ���ٴ�������ɺ��걨NDA/BLA���걨����������һ����Ҫ1-2�ꡣ
��������Ϲ�˾��ҩ�з��������������ڹ�˾��ҩ�з�������ɱȹ�˾����ҩ����з����˵��ļͶ��Ŀ��ҩ�з��Ƿ�����ش�ȷ���Է���
1������ҩҵ����ҩ�з�����
��1������ҩҵ�ǹ���ҵ��Ϊ�������ӵ����������ҩ�з��������߱�������ٴ�ǰ�з���ע���걨���ٴ��о��������Ŷӵ���ҩ��˾��
����2011�꣬��˾�����з��Ĺ���1.1����ҩ���������ԭ����ʳƷҩƷ�ල�����ְ䷢����ҩ֤����������IJ���ʼ�������ۣ��ò�Ʒ���й���һ��ӵ������֪ʶ��Ȩ��С���Ӱ�����ҩ������ҩҵ�������ҩ�з������Ѿ��õ���֤��
�����������к�˾�����ҩ�з���ͨ�������з���ս�Ժ�����ʵ�˹�˾���з����ߣ��ڴ˹����в��������Ż���˾�з��������ɣ�������������Ƶ��з���ϵ��������ɲ���Ϊ��˾��ҩ�з����ĺ�ҽѧ����
��˾��ҩ�з��������豱����ҩ�з����ġ�������ҩ�з����ġ���ҩ�����з�������������ﲿ����ҩ�����ٴ��о�������ţ��е�С���ӡ������ҩ�����ҩ�з���������չ��ҩ������ṹ��ơ���ѧ�ϳɡ�����ɸѡ��ҩ��ҩЧ�о���
��ȫ�����ۡ�ר���걨��ҩѧ�о����ٴ�ǰ�о���ͬʱ����˾�����ٴ���Ŀ�滮�Լ�ʵʩ�����ݹ�˾ҵ��ս�ԣ���˾ҽѧ��ȫ�渺������ǰע���ٴ��о������в�Ʒҽѧ���Ե��ƶ���ʵʩ���������ҵҽѧ��Ŀչ���о��ͷ�����Эͬ�з���ѧ���ƶ��о��ƻ���Э����˾����ҽҩ��Ŀ��ս��Ͷ�ʣ�ȫ��滮�������ٴ��о����ԣ���֯��ʵʩ�������ٴ�������Ŀ��
��2������ҩҵ�߱�Խ�ĺ����з��Ŷӣ��з�ʵ��ͻ��
����ҩҵʼ�ռ�֡��˲���������Դ�ͲƸ�����һ����������ƺ��˲ż���ЧӦ�������ԣ�������һ��������ҩ�з�����˲ŵļ��ˡ�Ŀǰ����˾����Ա��1300���ˣ��������������ⲩʿ30���ˣ�7λ��ѡ���Ҹ߲���˲żƻ���7λ��ѡ�㽭ʡ�߲���˲żƻ���
��˾�ĺ����з��Ŷӳ�Ա�������³�����ϯִ�йٶ�������ʿ����֪���������20����С���ӻ����↑��������ܲü���ϯ��ѧ��JIABING WANG�����ұ�����ʿ��ѧ��������������ܲü���ϯҽѧ��LI MAO��ë������ʿ�Լ�ս�Ժ������ܼ�LI LILY YING����ӯ)��ʿ�������з���������HONG LAN������)��ʿ�������з�����������ʿ������������з�LIANG DENG����������ʿ������ѧ���ܼ�WENXIN XU�������£���ʿ���ٴ�������ҽѧ�������˼��������ȡ�
��3������ҩҵÿ�����з�������д���Ͷ�룬�γ��˷ḻ�����в�Ʒ�ݶ�
��˾������һ֧400���˵���ҩ�з����顣Ŀǰ��˾���в�Ʒ30����з����������ḻ���Ѿ��γ���ÿ�궼�д���ҩ�����ٴ������Է�չ̬�ƣ���Ҫ���Ƿΰ��������ȶ�����������������С���Ӱ���ҩ����з�����˾���ڲ��ִ��������ҩ���з�������������̽�����õ����Ʒ�������˾�ѽ���һ֧��Ч���ٴ��о�ҽѧ��Ա���飬���ٴ���������ơ���Ŀ�ĸ��ٹ������涼����רҵ�������ͷḻ�ľ��飬Ϊ��ҩ��Ŀ�Ŀ����ƽ��;��������ṩ��ֱ��ϡ��������ڣ���˾��ҩ�з������ƽ����з���Ա���з�Ͷ��������ӡ���˾�з�Ͷ��������£�
| ��Ŀ | 2019�� | 2018�� | 2017�� |
| ��Ŀ | 2019�� | 2018�� | 2017�� |
| �з���Ա�������ˣ� | 466 | 359 | 253 |
| �з���Առ�� | 35.09% | 30.95% | 25.71% |
| �з�Ͷ�����Ԫ�� | 67,458.50 | 59,003.25 | 38,063.98 |
| �з�֧���ʱ�������Ԫ�� | 34,822.16 | 28,633.67 | 17,790.97 |
| �з�֧���ʱ������ռ�з�Ͷ����� | 51.62% | 48.53% | 46.74% |
| �з�Ͷ��ռӪҵ������� | 43.41% | 48.20% | 37.09% |
| �з�֧���ʱ������ռ���ھ�����ı��� | 154.19% | 175.11% | 70.94% |
��ˣ�����ҩҵ���к�ǿ����ҩ�з�ʵ���ͷḻ����ҩ�з����顣
2���������ڹ�˾����ҩ�з����
��˾�з����߷ḻ��Ŀǰ������ҩ��Ŀ30����ѽ����ٴ��о������в�Ʒ��13���Ҫ���Ƿΰ������������ٰ��ȶ����������������γ���ÿ�궼�д���ҩ�����ٴ������Է�չ̬�ơ�����С���Ӱ���ҩ����з�����˾���ڻ������ִ��������ҩ���з��������Ѿ������˴����ҩ���з��Ŷӣ����������з���Ŀ����ý�չ���ر��ڷΰ�������������˾�����γɲ�Ʒ����Ŀǰ��ɳ�������������Ŀ���ύ�й��������룬��������������������
��˾���в�Ʒ�γ������õ��νӣ�����2020��4��30�գ���Ҫ������Ŀ��չ���£�
| ��� | ��Ʒ | ��Ʒ��Ϣ | ��Ӧ֢ | �з���ע�ᣩ�� | ��չ��� | 2020��Ŀ�� |
| һ�������� | ||||||
| 1 | �������� | ��ҩ1�࣬ һ��EGFR-TKI | EGFR����ͻ���Сϸ���ΰ����������� | �ٴ����� | ���� | �걨NDA |
| 2 | �����ɳ���� | ��ҩ1�࣬ ��һ��ALK���Ƽ� | ALK����NSCLC���ߵĶ������� | �걨���� | CDE������ | ȡ��ҩƷע��֤�� |
| ALK����NSCLC���ߵ�һ�����ƣ�ȫ������ģ� | �ٴ����� | ���� | ����������� | |||
| ROS1����NSCLC���ߵ����� | �ٴ����� | ���� | �����о� | |||
| 3 | CM082 | ��ҩ1�࣬ ��е������Ұ��ἤø | ����VEGFR-TKIһ������ʧ�ܵ�ת�������� | �ٴ����� | ��/���� | �걨NDA |
| ����JS001���ڼ���δ������ | �ٴ����� | ���� | �ƽ����� |
| ��� | ��Ʒ | ��Ʒ��Ϣ | ��Ӧ֢ | �з���ע�ᣩ�� | ��չ��� | 2020��Ŀ�� |
| ��RTKs�����Ƽ� | �ľֲ���չ��ת����ճĤ��ɫ���� | �ٴ����� | ||||
| ʪ����������Իư߱��ԣ�w-AMD�� | �ٴ����� | ���� | �����о� | |||
| 4 | MIL60 | ��������ҩ | ���ڻ��Է���״ϸ����Сϸ���ΰ� | �ٴ�����[ע] | ���� [ע] | �걨BLA [ע] |
| 5 | BPI-D0316 | ��ҩ1�࣬ ����EGFR-TKI | ����ʹ��EGFR-TKI��ҩ�����T790Mͻ��ľֲ����ڻ�ת���Է�Сϸ���ΰ� | �ٴ����� | ���� | ����������� |
| ����δ�����Ƶ�EGFR����ͻ��ֲ����ڻ�ת����NSCLC���ߣ�һ�����ƣ� | �ٴ����� | ��/���� | ��ɻ������� | |||
| 6 | BPI-16350 | ��ҩ1�࣬ CDK4/6���Ƽ� | ʵ���� | �ٴ����� | ���� | �ƽ��ٴ����� |
| 7 | MRX2843 | ��ҩ1�࣬ MerTK��FLT3˫�����Ƽ� | ʵ���� | �ٴ����� | I�� | �ƽ��ٴ����� |
| 8 | BPI-17509 | ��ҩ1�࣬ FGFR1/2/3С�������Ƽ� | ����ʵ���� | �ٴ����� | ���� | �ƽ��ٴ����� |
| 9 | BPI-23314 | ��ҩ1�࣬ BETС�������Ƽ� | ������ϵ��Ѫ�� | �ٴ����� | ���� | �ƽ��ٴ����� |
| 10 | BPI-27336 | ��ҩ1�࣬ ERK1/2���Ƽ� | ����ʵ���� | �ٴ����� | ���� | �ƽ��ٴ����� |
| 11 | BPI-28592 | ��ҩ1�࣬TRK���Ƽ� | ����ʵ���� | �ٴ����� | ���� | �ƽ��ٴ����� |
| �������� | ||||||
| 12 | BPI-3016 | ��ҩ1�� | ���� | �ٴ����� | ���� | �ƽ��ٴ��о� |
| ��������ҩƷע�� | ||||||
| 13 | ����ľ���� | ������������Ʒ��7�� | RASҰ����ת���Խ�ֱ������mCRC�� | ע������ | �걨�������� | �ƽ�BLA�걨 |
ע����������������ظ���������գ�MIL60�걨BLA�ѻ��������Ԥ��2021����CDE����ͨ����
���ϱ�����ʾ����Ŀ�⣬��˾�����ƽ�20����ٴ�ǰ�о���Ŀ���۽�������������С���Ӱ���ҩ���չ�����ҩ���з���
3���ɱȹ�˾����ҩ������кͼ����������
��ҩ���з�Ͷ��ijɹ�����ҩ������ԭ����ҩ����������Ʒ�з�ģʽ���ٴ����鷽�����ٴ���չ�ε�������ڽϴ���졣�ܵ���˵��Խ�ٽ����У��ɹ�����Խ����2020��4��30�գ�����ҩҵļͶ��Ŀ�е���ҩ��Ŀ�����ֿɱȹ�˾�����л����е�����ҩ��������£�
| ҩƷ���� | ҩƷ��� | ��Ҫ�е� | ���Ʋ�Ʒ | ������ҵ | ��������ʱ�� | �й���½����ʱ�� |
| ��ɳ���� | �ڶ���ALK���Ƽ� | ALK | �������� | ���� | 2011�� | 2013�� |
| �������� | ���� | 2015�� | 2018�� | |||
| CM082 | ��е������Ұ��ἤø��RTKs�����Ƽ� | VEGFR��PDGFR�� | �������� | ���� | 2006�� | 2007�� |
| �������� | �ݶ� | 2005�� | 2006�� | |||
| MIL60 | ������������ά͡������������ҩ | VEGF | ��ά͡ | ���� | 2004�� | 2010�� |
| ���ɴ� | ��³ | - | 2019�� | |||
| IBI305 | �Ŵ� | - | CDE���� | |||
| BP102 | ���� | - | CDE���� | |||
| LY01008 | ��Ҷ | - | CDE���� | |||
| D0316 | ������EGFR���Ƽ� | EGFR��T790Mͻ�� | ��ϣ���� | ��˹���� | 2015�� | 2017�� |
| �������� | �ɭ | - | 2020�� | |||
| �������� | ����˹ | - | CDE���� |
���ϱ����Կ���������ļͶ��Ŀ�е���ҩ��Ŀ����Ϊ��֪����е�Ļ�ѧҩ�Լ���������ҩ����Ըðе�����ҩ��������У��з��ɹ����ʽϸߡ�ļͶ��Ŀ�е���ҩ��Ŀ��Ϊ����ǰ���ε��ٴ���Ŀ����Ŀ�Ѿ���øý���ص��ٴ���������ҽԺ������������˾�Ѿ��ٴ���ע������������CDE����������Ĺ�ͨ����˾ǰ�ڻ��۵��ٴ����ݷḻ���з��ɹ����ʴ�������������У������о��ɹ��ѷ�������Ҷ���ȹ�����Ȩ��ҽѧ�ڿ�����ɳ������������Ѿ�����CDE��Ҫ��ҩѧ�о����ϣ�Ԥ�ƽ���������С�
��ˣ�����ļͶ��Ŀ��ҩ�з��������ش�IJ�ȷ���Է��ա�
�������Կ��ܴ��ڵķ��ս����ش������ʾ
1���������ѳ����¶���η��е�ļ���ʽ���;�����Ϣ
��˾��2020��3��3���ٿ������춭�»�����λ��飬����ͨ������ʱ��¶�ˡ�2020��ȷǹ�������A�ɹ�ƱԤ������������2020��ȷǹ������й�Ʊļ���ʽ�ʹ�õĿ����Է������桷�ȱ��ηǹ�����������鰸����ļ���ʽ���;�����˳�ֵ���Ϣ��¶��
2������ļͶ��Ŀ�������ش�ȷ���Է���
��˾���ηǹ���ļ���ʽ�������ҩ�з����з��豸������Ŀ�����������ʽ���Ŀ����˾�Ѿ���ļͶ��Ŀ�Ŀ����Լ���Ҫ�Խ����˳�ֵ��о���֤��ļͶ��Ŀ�漰����ҩ�з���Ŀ��Ϊ����ǰ�����һ���ٴ��μ�ע�����ٴ�����Ŀ���������ش�ȷ���Է��ա�
3���Կ��ܴ��ڵķ��ս����˳�ֵĽ�ʾ
��˾�ڡ�2020��ȷǹ�������A�ɹ�ƱԤ�����жԱ��ηǹ������еķ��ս����˳�ֵĽ�ʾ����ļ���ʽ���Ŀ������Ԥ������ķ��ս������ص���ʾ���£�
������ļ���ʽ���Ҫ���ڡ���ҩ�з����з��豸������Ŀ������ҩ�з���Ŀ���������·��գ���������ļ���ʽ�Ͷ����Ŀ������Ԥ������ķ��ա�
��1�������
��ҩ�з�Ͷ������ڳ�������Ԥ�����ؽ϶࣬���з������кܿ���������Ч��ȷ������ȫ������ȶ���ԭ�����з�ʧ�ܣ��Ӷ������з����ա�
��2����������
��ҩ������ڽϳ���ʱ�䲻ȷ���Խ�ǿ��δ���������ߴ���һ���̶ȱ䶯�Ŀ��ܣ���˲�Ʒ�����ſ�����ȡ��ҩƷע���������������ɵķ��գ��Ӷ��������������ۡ�
��3�������
����ҩ��ҽҩ��ҵ�ص��з�����δ����Ʒ���»����ٶȻ�ӿ죬�����Ӿ���ܻᵼ�²�Ʒ����Ƚ��ۺ��г��ƹ��ѶȼӴ������˾���ܿ��������о���
���IJ�Ʒ���������ֺ�����Ʒ���ߣ�ļͶ��Ŀ����������һ�����г����ա�
��4�������ƹ����
����ҩ��Ʒ��Ҫרҵ�������ƹ��Ŷӽ���ѧ���ƹ㣬���ҽ���ͻ��߶Բ�Ʒ���˽⣬�Ӷ�������Ʒ�ϿɶȺ�ʹ���ʡ����⣬�����ƹ��Ŷ���Ҫ��ʱ�����˽����ҽ�����б����߱仯���ƶ����������۲��ԣ���ȷ����Ʒ�����ܹ�˳����ء���˹�˾������һ���������ƹ���ա���
���ϣ����η��е�ļͶ��Ŀ�������ش�ȷ���Է��գ��������ѳ����¶���η���ļͶ��Ŀ����ҩ�з����з��豸������Ŀ�������Ϣ�Լ����ܴ��ڵķ��գ����η��еľ��߳�����ϡ���˾��������֤ȯ�����������а취������ط��ɷ��桢�淶���ļ�������˾�³̡��Ĺ涨�����η��в����������й�˾����С�ɶ�����������Ρ�
�ġ�ļͶ��Ŀ��ز�Ʒ���г��ռ���������ٵľ���������Ƿ�����г����ز���Ԥ�ڵķ��ռ����ȡ��Ӧ�Դ�ʩ
��һ��ļͶ��Ŀ��ز�Ʒ���г��ռ���������ٵľ������
1����ɳ����
��ɳ�����ǹ�˾�Ϳع��ӹ�˾Xcovery��˾��ͬ������ȫ�µġ�ӵ����ȫ����֪ʶ��Ȩ��С���ӻ������һ������ǿЧ����ѡ���Ե���һ��ALK��������ܰ�����ø�����Ƽ�������ѧҩƷ1�ࡣ���ڶ�ɳ��������ALK����NSCLC���߶������Ƶ���ҩע���Ѿ�����CDE����Σ�ͬʱ��˾Ҳ�ڻ����ƽ���ɳ��������ALK����NSCLC����һ�����Ƶ�ȫ������Ģ����ٴ���Ŀǰ�Ѿ�������顣��ɳ����������Ϊ��˾��һ��ȫ�����еĴ���ҩ��
��1���������
��ɳ�������Ҫ��������������£�
| ��� | ��Ʒ | ������ | ��������ʱ�� | �й���½����ʱ�� | ȫ�����۽�����Ԫ�� | |||
| �������� | һ������ | �������� | һ������ | 2018�� | 2019�� | |||
| ��� | ��Ʒ | ������ | ��������ʱ�� | �й���½����ʱ�� | ȫ�����۽�����Ԫ�� | |||
| �������� | һ������ | �������� | һ������ | 2018�� | 2019�� | |||
| һ�� | �������� | ���� | - | 2011�� | - | 2013�� | 5.24 | 5.30 |
| ���� | ɫ������ | ŵ�� | 2014�� | 2017�� | 2018�� | 2020�� | - | - |
| �������� | ���� | 2015�� | 2017�� | - | 2018�� | 6.37 | 8.76 | |
| �������� | ���� | 2017�� | 2020�� | - | - | - | - | |
| ���� | �������� | ���� | 2018�� | - | - | - | - | - |
������Դ��https://www.druganalyst.com/��CDE
����������Ҫ����ALK���Ե����ڻ�ת���Եķ�Сϸ���ΰ������ƣ����ڵ�һ��ALK���Ƽ���ɫ�����ᡢ�������ᡢ���������ǵڶ���ALK���Ƽ������а��������Ѿ���2018��ͨ��CDE�����У��Ƕ�ɳ�������Ҫ�������֡�������������ALK�������ڷ�Сϸ���ΰ�һ�����Ƶ���λ��չ�����ڣ�mPFS���ߴ�25.7����
��Զ�������������10.9����
������ۻ����ʣ�ORR��Ҳ���������������ᣬͬʱ�����������ת�Ƶ���Ч���������ڿ���������ҩ��Ķ������Ƶ�mPFS8.9���£�ORR50.0%
����˰����������к����۽��Ѹ�ٳ����������ᡣ���ݶ�ɳ�����ѷ������ٴ������ʾ����ɳ����һ�����Ƶ�mPFS26.2���£�ORR80.0%
���Ͱ�����������൱������������ίԱ�ᣨIRC����������ɳ����������Ƶ�mPFS11.2���£�ORR52.6%��
��2���г��ռ�
���ݹ��Ұ�֢���ķ��������ݣ�2015���й�ÿ��ΰ��ķ������ߴ�78.7��������Сϸ���ΰ�ռ��ԼΪ85%���������о��������й�ALK���Ե�NSCLCԼռ����NSCLC��3%-7%������ƽ��ֵ5%���㣬ÿ������ALK����NSCLC
Roche.com. 2020. Follow-Up Phase III Data Showed Roche��S Alecensa Helped People WithALK-Positive Metastatic Non-Small Cell Lung Cancer Live A Median Of Almost Three YearsWithout Their Disease Worsening Or Death. [online] Available at:
<https://www.roche.com/media/releases/med-cor-2018-05-17b.htm>
Solomon, B.,et al, 2018. Final Overall Survival Analysis From a Study Comparing First-LineCrizotinib Versus Chemotherapy in ALK-Mutation-Positive Non�CSmall-Cell Lung Cancer. Journal ofClinical Oncology, 36(22), pp.2251-2258.
Tran, P. and Klempner, S., 2016. Focus on Alectinib and Competitor Compounds for Second-LineTherapy in ALK-Rearranged NSCLC. Frontiers in Medicine, 3��65
Horn, L. et al.,Ensartinib (X-396) in ALK-Positive Non�CSmall Cell Lung Cancer: Results from aFirst-in-Human Phase I/II, Multicenter Study. Clinical Cancer Research, 2018,24(12), pp.2771-2779.
����Լ3.3���ˡ��ڲ�����δ��ҩƷ���ۡ������ʺ�ҩ�����ʵ����ص�����£���������Ϊ������������2019���ҽ��̸�м۸�15,232Ԫ/�У�ÿ�п�ʹ��28�죬�����ն������ƹ���ÿ������9���µ���ҩʱ�䣬�˾���ҩ���146,880Ԫ���й��г��ռ�Լ48��Ԫ�����ǵ��������������ALKһ���������ݣ�������ÿ��25���µ�ʹ��ʱ�䣬�й��г��ռ�ߴ�135��Ԫ���ҡ���ɳ������Ϊ�밢��������Ч�൱�Ĺ���һ����ҩ��������ALK����ҩ�г�ռ��һϯ֮�ء�
���������г���2018�������ΰ��·�������22.9���ˣ���85%��NSCLC�ı������Լ�5%��ALK���Ա������㣬2018�������·��ΰ�������ALK���Ի���Լ1���ˡ��ڲ�����δ��ҩƷ���ۡ������ʺ�ҩ�����ʵ����ص�����£��ο�������������13����Ԫ/������Ʒ��ã��Լ���������Ͷ�ɳ�������һ��ALK���Ƽ���ɫ��PFS����ÿ������25���µ�ʹ��ʱ����㣬����ALK���Ƽ����г��ռ�Լ27������
2��CM082
CM082���ǿڷ�����һ����ҩ����һ��ȫ�½ṹ��VEGFR��PDGFRΪ���Ķ�е㼤ø���Ƽ�����������������������ʪ����������Իư߱��ԣ�w-AMD���Լ���PD-1����ɼ������άĪ˾�ȿ�����ҩ������ҩ�ȡ�
CM082�й�����Ŀ��ȫ���ӹ�˾���ϼ�ҽҩ�Ƽ����Ϻ�������˾�����ƽ���2013������������Ӧ֢��ҩ���ٴ�����������2013��-2016�����CM082��ҩI���ٴ�����,2015��-2017�����CM082������άĪ˾I���ٴ����顣Ŀǰ�Ѿ���������������ƵĢ�/�����ٴ�����IJ������顣
��1��������������ҩ�ᄎ�����
����������������ҪС����ҩ���У�
| ������Ʒ | ������ | ��������ʱ�� | �й���½����ʱ�� | ȫ�����۽�� ������Ԫ�� | |||
| ���� ���� | һ�� ���� | ���� ���� | һ�� ���� | 2018�� | 2019�� | ||
| �������� | ���� | - | 2006�� | - | 2007�� | 10.49 | 9.36 |
| ������Ʒ | ������ | ��������ʱ�� | �й���½����ʱ�� | ȫ�����۽�� ������Ԫ�� | |||
| ���� ���� | һ�� ���� | ���� ���� | һ�� ���� | 2018�� | 2019�� | ||
| ��άĪ˾ | ŵ�� | 2009�� | - | 2013�� | - | 15.56 | 15.39 |
| �������� | �ݶ� | - | 2005�� | - | 2006�� | 7.12 | 7.06 |
| �������� | ���� | 2012�� | - | 2015�� | - | 2.98 | 4.77 |
| �������� | Exelixis | 2016�� | 2017�� | - | - | - | - |
| �ط����ᣨ+��άĪ˾�� | ���� | 2016�� | - | - | - | - | - |
������Դ��https://www.druganalyst.com/��CDE�������������ݰ��������Ӧ֢��
���У���άĪ˾Ϊ����ҩ��������ᡢ���������ѷֱ��ڹ��ڻ�������һ�����ƣ���������Ϳ���������Ӧ֢Ϊ��ҩ�����Ѿ����ܹ�һ�����Ƶ������������ط�����������άĪ˾����VEGFR-TKI����ʧ�ܵ���������mPFS14.6����
�������ӳ���������������չ�����ڡ�CM082������άĪ˾����VEGFR-TKI����ʧ�ܵ�RCC�Ģ����ٴ�������ʾ�䰲ȫ�����ã�ORR32%��PFS�����ﵽ12��������
��
��2���������������г��ռ�
��ϸ������RCC����һ��ȫ��Χ�ڳ����Ķ��������������������������������֯���ݣ�ȫ������������ռȫ����������2%��3%��������ϵͳ���������У��䷢���ʽ����ڰ��װ����ҳ������������ơ�2016�꣬ȫ��ԭ��ר���г���������ҩ�����۶��Ѵ�162.50����Ԫ��ͬ����һ��������23.87%���ڸ��������£���������ҩ���г���2006���27.61����Ԫ������5����
���ݹ��Ұ�֢���ķ��������ݣ��ҹ�2015�������·�������6.68�������ң�������������ƽ��ÿ��6.5%���ٶ��������·�����������ռ70%���ϣ�����71%��������������Ϊ��ϸ������
��������2019��ĩҽ��̸�м۸�5700Ԫ/�У�60Ƭ����ÿ����ҩ���11,400
R.J. Motzer, et al.Lenvatinib, everolimus, and the combination in patients with metastatic renal cellcarcinoma: a randomised, phase 2, open-label, multicentre trial Lancet Oncol, 16 (15) (2015),pp. 1473-1482
Sheng, X., et al. 2020. Phase 1 trial of vorolanib (CM082) in combination with everolimus inpatients with advanced clear-cell renal cell carcinoma. EBioMedicine, 55, p.102755.
Ԫ���ڲ�����δ��ҩƷ���ۡ������ʺ�ҩ�����ʵ����ص�����£������������ҽ��̸�м۸�Ϊ�ο�����10������ΪCM082����ҩʱ�䣬CM082���������������г��ռ�38��Ԫ���ҡ�
��3������ճĤ��ɫ����ҩ�ᄎ�����
�ڹ����ĺܶ����ճĤ��ɫ����������û�б����Ʒ�ʽ��������������ճĤ��ɫ����������ȡ����һЩͻ���ԵĽ�չ���������ڸ��廯�������ƺ�������������ʱ��ʩ��BMS����˾���������CTLA-4�е�ҩ����ƥ������Ipilimumab���������������е�������������ҩ�����Ӧ֢Ϊ���ڶ��Ժ�ɫ������2014�꣬��ʱ��ʩ��BMS����˾���ձ�СҰҩҵ���Ͽ�����PD-1���Ƽ����䵥����Nivolumab�����ձ����У��������ں�ɫ���������ơ����Ĭ�ˣ�MERCK����PD-1���Ƽ���ķ������Pembrolizumab�����������У�Ҳͬ���������ں�ɫ���������ƣ�ĿǰPD-1���Ƽ��ѱ�NCCNָ���Ƽ�Ϊ��ɫ�����ı�һ�����ơ���������������ҵ�⣬��ʵ������������������JS001�����ں�ɫ������������Ҳ���ڹ������С�
̽�������Ʒ�����PD-1/PD-L1������������ҩ�����ϣ�Ѱ���ʺ��ض������ĸ���Ч��ȫ���������Ʒ������ǵ�ǰȫ������ҩ���о��Ĵ��µ��ͻ�Ƶ㡣2018��3�£�Ĭɳ����MSD����������Eisai����lenvatinib��ҩ����������ķ�������ڰ�����ɫ�������ڵ���������11����Ӧ֢���ٴ�������������ʵ�������������������JS001���밢���������ϣ�����ճĤ�����ں�ɫ����Ҳ���ٴ��з��Ρ�
CM082����JS001����ճĤ��ɫ�����Ѿ���ɢ����ٴ����չ�����ٴ���
��4������ճĤ��ɫ���г��ռ�
���ݹ��Ұ�֢���ķ��������ݣ��й�2015���ɫ�����·�������Ϊ8000�����ң�ճĤ��ɫ����ռ��Լ22.6%��������������2%����ÿ��ÿ��10������Ʒ��ü��㣬�г��ռ�1.8��Ԫ���ҡ�
3��MIL60
MIL60Ϊ������������ά͡������������ҩ����Ҫ������ڻ��Է���״
ϸ����Сϸ���ΰ�����ֱ�����ȶ��ʵ������Ӧ֢������������Ϊ����VEGF�Ŀ���ҩ���ͨ����������Ѫ�����ɷ��ӿ����������á���������ԭ��Ϊ����̩�˹�˾���������չ�������Ʒ������ά͡����2004����FDA�����С���ά͡��2010�����й��������У�Ŀǰ�ѻ�����Ӧ֢����ת���Խ�ֱ����������ת���Ի��Է�Сϸ���ΰ���Ԥ�ƺ�������w-AMD�����������ٰ��ȶ��ְ�֢����Ӧ֢��
��1���������
�����������еı�����������ҩ��ABP215����������Zirabev�����𣩵ȡ����ڵ�һ�һ���������еı�����������ά͡����������ҩΪ��³��ҩ�İ��ɴ�������ڡ�ת���Ի��Է�Сϸ���ΰ���ת���Խ�ֱ�������ߵ����ƣ��������ȽϿ�Ļ����Ŵ��������ҽҩ���������硢��Ҷ��ҩ�ͱ���ҩҵ�ȡ�2018�갲ά͡ȫ�����۶�68.5����Ԫ�������г����۶�Լ27.4��Ԫ��2019��ȫ�����۶�70.7����Ԫ�������г����۶�Լ36.6��Ԫ���г��ռ������
| ������Ʒ | ������ | ��������ʱ�� | �й�����ʱ�� |
| ��ά͡ | ���� | 2004�� | 2010�꣬2015��������۷�Сϸ���ΰ���Ӧ֢ |
| ���ɴ� | ��³��ҩ | - | 2019�� |
������Դ��https://www.druganalyst.com/��CDE
��2���г��ռ�
�й�ÿ��ΰ��ķ������ߴ�78.7��������Сϸ���ΰ�ռ��ԼΪ85%����Сϸ���ΰ��У���״ϸ����ռ30%���ң����۷�Сϸ���ΰ�ռ70%���ҡ�
��ά͡���Ͽ�������ɼ�����Ʒ���״ϸ����Сϸ���ΰ���mPFS9.2����
��2019��ף����ϰ�ά͡ҽ��̸�м۸�1,500Ԫ/ƿ����³���ɴﶨ��1,266Ԫ/ƿ��
�ڲ�����δ��ҩƷ���ۡ������ʺ�ҩ�����ʵ����ص�����£�����³��
Zhou, C., et al., 2015. BEYOND: A Randomized, Double-Blind, Placebo-Controlled, Multicenter,Phase III Study of First-Line Carboplatin/Paclitaxel Plus Bevacizumab or Placebo in Chinese PatientsWith Advanced or Recurrent Nonsquamous Non�CSmall-Cell Lung Cancer. Journal of ClinicalOncology, 33(19), pp.2197-2204.
��������������ҩΪ������60kg���صĻ����㣬ÿ������ҩ300mg���൱��ÿ������ҩ3ƿ��ÿ����Ҫ����3,798Ԫ��һ������ҩ���Σ�ÿ����ҩ����7,596Ԫ��9������Ҫ����68,364Ԫ����������������������ҩ�ڷ���״ϸ����Сϸ���ΰ�����Լ50%�������������ԵĻ��ߣ����Ƶ��г��ռ�ߴ�160��Ԫ������ҩҵ�걨��MIL60��Ӧ֢����Сϸ���ΰ��⣬����ת���Խ�ֱ������
4��D0316
D0316������T790Mͻ��ĵ�����EGFR-TKIҩ�EGFR���Եķ�Сϸ���ΰ������ڽ��ܵ�һ��EGFR-TKI����һ��ʱ��������������ҩͻ�䣬����T790Mͻ���ǵ�һ��EGFR-TKI��ҩ�����ͻ����ƣ�Լռ��ҩͻ���60%���ϡ�������EGFR-TKI�ܹ�����������ҩ���ߵ������������ӳ���չ�����ڡ�Ϊ�˴ﵽ���õ�����Ч����ͬʱ������ҩ�����ԣ�Ŀǰ�����ٴ�һ����á�1+3�����Ʒ����������õ�һ��ҩ���������ᡢ�������ᡢ�������ᣩ������T790Mͻ����õ�����ҩ����ϣ���ᣩ��
��1���������
���������еĵ�����EGFR�е�ҩ�����±���
| ������Ʒ | ������ | ��������ʱ�� | �й���½����ʱ�� | ȫ�����۽�� ������Ԫ�� | |||
| �������� | һ������ | �������� | һ������ | 2018�� | 2019�� | ||
| ��ϣ���� | ��˹���� | 2015�� | 2018�� | 2017�� | 2019�� | 18.60 | 31.89 |
| �������� | �ɭ | - | - | 2020�� | - | - | - |
������Դ��https://www.druganalyst.com/��CDE
�����з���չ�Ͽ�ĵ�����EGFR-TKI��ҩ�У�����˹�İ������ᡢ����ҩҵ��D0316����������ASK120067��Ԥ��D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�Ķ������ƽ���2021���걨NDA��D0316����EGFR���Ե�NSCLC��һ�����ƽ���2022���걨NDA��
��2���г��ռ�
�й�ÿ��ΰ��ķ������ߴ�78.7��������Сϸ���ΰ�ռ��ԼΪ85%����Сϸ���ΰ���EGFRͻ��Ϊ��������ͣ�ռ��Լ40-50%��T790Mͻ��ռʹ�õ�һ��EGFR-TKI��ҩͻ���60%���ϡ�
��ϣ�������й����к����ۿ���������2019��Ժ���������۸ߴ�21.35��Ԫ����������IQVIA����Ŀǰ��ϣ����Ķ���������Ӧ֢�Ѿ�����ҽ����̸�м۸�Ϊ510Ԫ/80mg��ÿ���·���15,300Ԫ����ϣ�������ڶ������Ƶ�mPFS 10.1���£�����һ�����Ƶ�mPFS18.9����
���ڲ�����δ��ҩƷ���ۡ������ʺ�ҩ�����ʵ����ص�����£���ϣ�����ҽ���۸��PFS��Ϊ�ο����Լ���Сϸ���ΰ�������40%��EGFRͻ���ʺ�60%��T790Mͻ���ʵ�����£�������EGFR-TKI�������Ƶ��г��ռ�ߴ�245��Ԫ��һ�������г��ռ�Ԥ�ƻ�ȶ������ƴ�һ����
�������Ƿ�����г����ز���Ԥ�ڵķ��ռ����ȡ��Ӧ�Դ�ʩ
�г����ز���Ԥ�ڵķ��ս�С����Ҫԭ���У�
1���й�ҽҩ��ҵ�г�ǰ������
������˿��������˿����仯�̶ȼ��������ҵӭ���µĻ�����2019��ĩ���й�60���꼰�����˿�Ϊ25,388���ˣ�ռ18.13%��65���꼰�����˿�Ϊ17,603���ˣ�ռ12.57%����2018��ĩ��ȣ� 60���꼰�����˿�����439���ˣ�65���꼰�����˿�����945���ˣ���������Դ������ͳ�ƾ֣������仯�̶ȼ��һ������ζ���Ͷ��˿ڸ������Ӵ���ҽ������������ѹ����ҵ�����������Ͽطѡ���ҩ�۵ĸ�ѹ���ߣ���һ�������仯���̼�����ҩ������ҩ�ķ�չ�Լ����ٵĽ���ҽ�����ѡ��й��������������ʡ����Բ�������Ⱥ�������Ӹ߲��£�����ҵ�г���һ�����ݡ�2019��9�£�����ί��NMPA��ҽ���ֵ�10��ί����ӡ���ˡ������й��ж�������֢����ʵʩ������2019��2022�꣩�����Խ����������ҹ��İ�֢���ι�������ȫ��IJ��𣬰����ƽ���֢ɸ�顢�������κ淶���ƣ��ƽ���֢����ҽ�����Ľ��裬�������ƿ���ҩ���ٴ��ۺ�������ϵ�ȣ����ҹ�����ҩ��
J.-C. Soria, et al., 2018. Osimertinib in untreated epidermal growth factor receptor (EGFR)-mutatedadvanced non-small cell lung cancer. Translational Lung Cancer Research, 7(S2), pp.S165-S170.
�з���ҵ�������Ҫ��ҲΪ�ҹ�����ҩ��ķ�չ�������»�����2019�꣬�ҹ������г����۶�ﵽ1024.37�ڣ�ͬ������22.09%������ҩ�ﱣ�ָ�����������ȥ��ͬ�������ʴ�77.21%��������Դ��IQVIA������˾ļͶ��Ŀ����ҩ��Ʒ��Ϊ������Ʒ����Էΰ������������߱��������г��ռ䡣
2����˾�߱��ḻ����ҩ�г��ƹ��������ƹ㾭��
2011�꣬����������Ϊ��һ���������֪ʶ��Ȩ�Ĺ���������ҩ�����г�����������ҵ̨ͬ�����������������ھ�����Ʒ�������ӡ��������Ƹ����Ͼ�������£�����������Ȼ���ָ���������2019���Ʒ����ͻ��15��Ԫ�����˸��Ǻ����۶���ͬ���Ʒ�м����������ȵ�λ��������Ա�˾�����Լ300��Ԫ���ڹ�����������ҩ��ҵ�б������ȡ���˾������һ֧רҵ���ɵľ��о��������г��ƹ��Ŷӣ���֧�Ŷ���Ϥ�������ߣ����Ȳ�������ҩҽ��̸�У�ͨ��������ʽ�Ļ��顢��̳�ȷ�ʽ����ѧ���ƹ㡢�Ӵ����ҽԺ�ĸ��ǣ���ǿ���߽������ƹ����ȡ���˾ļͶ��Ŀ����ҩ��Ʒ��Ϊ��������Ʒ���ر������еĶ�ɳ���ᡢMIL60��D0316�ȷΰ����Ʋ�Ʒ���밣��������г�ЭͬЧӦ�ϴ���˱���ҩҵ��ȫ����������ҩ���к���п�����Ч���г��ƹ㡣
��Թ�˾��ҩ��Ʒ��½�����У���˾��ͨ��ץס������������ҩ̸�еĻ��ᣬ�ӿ���ҩ���г����֣���ǿ��˾�г��ƹ��Ŷӵ�רҵ���������Ӫ���ƹ��֧������ҽԺ�ĸ��Ƿ�Χ������ҽ���Ͳ�����ʶ����ǿ��˾���������磬ͨ������ҵ�������г��������֣����������������������Ч�ʡ������������ã�ͨ���ӿ첿�ֲ�Ʒ��ȫ�����У���һ��������Ʒ���г�Ӱ������
�塢�з��豸��������Ҫ�豸������豸�����ı�Ҫ��
��һ���з��豸��������Ҫ�豸���
��˾��Ա����з����ĺͺ����з����ĵ��з��豸��������Ͷ����ֱ�Ϊ2,984.93��Ԫ��4,335.65��Ԫ������7,320.58��Ԫ���з��豸��������Ҫ�豸�����������ظ�֮��һ������ļͶ��Ŀ����Ͷ���������ϸ��Ͷ������IJ������ݺͲ�����̣�����Ͷ�ʹ����Ƿ������ʱ���֧�����Ƿ���ļ���ʽ�Ͷ�롱֮��������Ͷ������IJ������ݺͲ�����̡�֮��1����ҩ�з����з��豸������
Ŀ��֮����2���з��豸��������
�������豸�����ı�Ҫ��
��˾��һ������ҩ�з�Ϊ���ľ��������Կ�����ҩΪ���IJ�Ʒ����ҩ��ҵ����˾��ǿ�������£�ǿ��Դͷ���¡�ת���о��Լ��ⲿս�Ժ��������к�˾���������Ż���˾�з��������ɣ�������������Ƶ��з���ϵ����ʵ������ҩ�з����ĺ�ҽѧ�����������з����ŵ�ʵ�����з��豸�����ı�Ҫ���У�
1����˾�з������������ƺ���Ա���ϳ�ʵ����Ҫ
��˾��ҩ�з��������豱����ҩ�з����ġ�������ҩ�з����ġ���ҩ�����з�������������ﲿ����ҩ�����ٴ��о�������ţ��е�С���ӡ������ҩ�����ҩ�з���������չ��ҩ������ṹ��ơ���ѧ�ϳɡ�����ɸѡ��ҩ��ҩЧ�о�����ȫ�����ۡ�ר���걨��ҩѧ�о����ٴ�ǰ�о���ͬʱ����˾�����ٴ���Ŀ�滮�Լ�ʵʩ��ҽѧ��ȫ�渺������ǰע���ٴ��о������в�Ʒҽѧ���Ե��ƶ���ʵʩ���������ҵҽѧ��Ŀչ���о��ͷ�����Эͬ�з���ѧ���ƶ��о��ƻ���Э����˾����ҽҩ��Ŀ��ս��Ͷ�ʣ�ȫ��滮�������ٴ��о����ԣ���֯��ʵʩ�������ٴ�������Ŀ��ͨ���������Ƶ��з���������˾��ҩ�з������ƽ����з���Ա���з�Ͷ��������ӡ�2016����������˾�з���Ա��������ӣ����з��豸���������ӡ���ˣ���Ҫ�����з��豸��������
| ��Ŀ | 2019�� | 2018�� | 2017�� | 2016�� |
| �з���Ա�������ˣ� | 466 | 359 | 253 | 246 |
| �з���Առ�� | 35.09% | 30.95% | 25.71% | 30.30% |
2���з���Ŀ�������з���Ŀ�ѶȲ������ӵ���Ҫ
����2020��4��30�գ�������ҩ��Ŀ30����ѽ����ٴ��о������в�Ʒ��13���2016��ף���˾����1����ҩ��2����ҩ��6��������14��3���4�����ҩ��Ŀ����˾�з���Ŀ�������ӣ��з����߲��Ϸḻ���з��豸�����������ӣ���˾��ҩ����з���Ŀ�Ĵ�������ӣ���Ŀ�з��Ѷ�Ҳ����������Է�������⡢�ϳɵ��з��豸����Ҫ�������Ҫ��ͬʱ������
3������������з��ŶӺͿ�չ������з���Ŀ������
����ҩ����ҩ��ҵ��������չ��������ҵ֮һ����˾�ڽ���С���Ӱ���ҩ���з���ͬʱ���������ִ��������ҩ���з�������Ŀǰ�Ѿ�������һ֧�����ҩ���з��Ŷӣ������˶��������з���Ŀ�������ƽ��з��������ҩ����С����ҩ���ڳ�ҩ������ҩ�����ԡ����������ȶ����������������ͬ����Ҫ���ƵĴ����ҩ����з��豸�Խ���һ���Ƚ��Ĵ����ҩ�↑����ϵ��
ͨ��ʵʩ����Ŀ�����������㹫˾δ��һ��ʱ������ҩ�з��ر���������������Ŀ���豸���������ڹ�˾�������һ���Ĵ���ҩ���з�����ƽ̨��
�������������˲����
��һ���˲����
��������������������ȡ�ĺ˲鷽ʽ�����������ڣ�
1����������˷����˱��η���ļ���ʽ�Ͷ����Ŀ��ص��ٴ��������ٴ�֪ͨ�顢�����������������о����桢CDE��ͨ���ϼ�����������ϣ�
2����ȡ�˷����˶���ļͶ��ĿͶ����������˵�����������ļͶ��Ŀ��Ͷ�ʹ��ɣ���Ͷ�ʹ�ģ�ĺ����ԡ�Ч�����Ľ����Ժͺ����Խ����˷�������ȡ�˷����˹���ļ���ʽ�Ͷ����Ŀ��Ͷ�������ʱ��滮��
3����������ҩ�з����̺��з����յĽ������ϣ���ѯ��ļ���ʽ�Ͷ����Ŀ��������ҩ�����Ʋ�Ʒ������������ļ���ʽ�Ͷ����Ŀ��չ����ؼ�����̸�˷�������ظ����ˣ�
4��������ļͶ��Ŀ��ز�Ʒ���г��ռ�˵���ļ��������˷�������̸�˷����������Ա���г����ز���Ԥ�ڵ�Ӧ�Դ�ʩ��
5����ȡ�˷������豸������Ŀ��Ͷ����ϸ�����Է����˵��з���������˺˲������
�������˲����
���˲飬����������Ϊ��
1������ļͶ��ĿͶ������߱��������ݣ���������������������ʽ���Ŀ�⣬��ҩ�з���Ŀ���з��豸������Ŀ��Ͷ�ʾ�Ϊ�ʱ���֧�������в�����ĿͶ�ʲ���ļ���ʽ�Ͷ�룻
2������ļͶ��ĿĿǰ���ڰ��ƻ��ƽ������У�����ļ���ʽ������η�����ض��»������ǰ��Ͷ���ʽ�
3����˾�з�ʵ��ǿ���з�����ḻ��ļͶ��Ŀ�е���ҩ�з���Ŀ��Ϊע�����ٴ�����Ŀ����˾�߱���չע�����ٴ����ٴ��������ٴ�֪ͨ�顢CDE�Ĺ�ͨ�ļ�����ҩ�з���Ŀ�滮��ȷ����չ˳����ļͶ��Ŀ�������ش�ȷ���Է��գ�
4��ļͶ��Ŀ��ز�Ʒ���г��ռ�ϴ����ٵľ������ֽ����ҹ�˾��Ʒ�߱�һ���ľ������ƣ��г����ز���Ԥ�ڵķ��ս�С����˾�Ѿ��߱�������ҩ�г��ƹ��������
5�����Ź�˾�з��������з���Ա�IJ������ơ��з���Ŀ���������Ӻ��ѶȵļӴ���ҩ�з�����������з��豸�������б�Ҫ�ԡ�
���������5��
���һ��ĩ�������������ʲ����5.1��Ԫ����ҪΪ����ʹ��Ȩ������ĿȨ�档����֧�����8.2��Ԫ����ҪΪ��Ŀ�ʱ����з�Ͷ�롣�������˲���˵����
��1�������ʲ�����ĿȨ�����Ҫ���ݣ��Ƿ����ʹ�ü�ֵ����ֵ���Լ���ֵ��������������������ʲ�Ϊ��˾������Ч�����˵����ؼ�ֵ�������Ƿ��֡���2���з�֧���ʱ��������������ݣ��Ƿ�һ���ԣ��������һ��ĩ����֧�������Ŀ����Ҫ���ݣ������ʱ���������˵���������Ŀ��չ������Ƿ�������ƽ�����һ���з���ֵ���ڹ��˵����Σ��Ƿ�Ӧ�����ֵ�����������з������ʱ�����������ӵ�ԭ�����ԡ���3����ϱ������ڹ�˾�з������ʱ�����������ļͶ��Ŀ��ҩ�з��ľ������˵������ļͶ��Ŀ�����з������Ƿ�����ʱ���������
�뱣�����������ʦ�����˲������
�ظ���
һ�������ʲ�����ĿȨ�����Ҫ���ݣ��Ƿ����ʹ�ü�ֵ����ֵ���Լ���ֵ��������������������ʲ�Ϊ��˾������Ч�����˵����ؼ�ֵ�������Ƿ���
��һ�������ʲ�����ĿȨ�����Ҫ���ݣ��Ƿ����ʹ�ü�ֵ
�����ʲ�����ĿȨ�����Ҫ�������£�
| ��Ŀ | �����ʲ����� | ����ԭֵ����Ԫ�� | �����ֵ����Ԫ�� |
| ����ֹʹ�� | ����ֹʹ���������� | 190.00 | - |
| BPI-3006 | ���͵�II����������ҩ�˹��ȸ�Ѫ��������-1��GLP-1��ר������ | 320.00 | - |
| ���ᰣ������ | ��EGFR�Ұ��ἤø���Ƽ�����ص�ר�������ͷ�ר������ | 6,048.48 | 856.87 |
| MIL60��ĿȨ�� | MIL60���й��IJ�ƷȨ��Ͳ�Ʒ�������Լ���Ʒ����Ȩ�� | 3,000.00 | 2,206.58 |
| MRX-2843��ĿȨ�� | MRX-2843��ؼ������й����в�Ʒ���������졢ʹ�á����ۡ���ŵ���ۺͽ��ڵ�Ȩ�� | 1,353.97 | 1,026.76 |
| X-396 | X-396��ؼ����Լ��ں���Ŀ���Ȩ�� | 19,887.29 | 14,657.89 |
| D-0316��ĿȨ�� | D-0316���й���ר����ר�м����������ҿ��������졢��ҵ��D-0316��Ȩ�� | 5,000.00 | 4,766.02 |
| MCLA-129��ĿȨ�� | MCLA-129��ؼ������й����в�Ʒ��������ҵ����Ȩ�� | 675.36 | 619.08 |
| X-82 | Equinoxӵ�е�X-82��ؼ����Լ��������ۿ���Ӧ֢�ĺ���Ȩ�� | 17,440.50 | 13,545.46 |
| CM082 | ���ϼ�ӵ�е�CM082��ؼ����Լ��������ۿ���Ӧ֢���й���Ȩ�� | 11,044.52 | 6,878.78 |
| �ϼ� | 64,960.12 | 44,557.43 | |
��1������ֹʹ��
����ֹʹ��ԭϵ�����ʴ���ҩҵ����˾ӵ�е�������������������������2006�꣬��˾ͨ���չ��ʴ���ȡ�ø������ʲ����������������۸ò�Ʒ��ֱ��2015��ֹͣ�������������ʲ�����2014��̯����ϡ�
��2��BPI-3006
BPI-3006��ָ���͵�II����������ҩ�˹��ȸ�Ѫ��������-1��GLP-1��ר���������������������������ʲ�����2017��̯����ϡ�
���ڸü�������˾��������������ҩBPI-3016�з���Ŀ������2017��ȡ���ٴ���������������Ŀǰ������Ŀ�����ٴ�I�����顣
��3�����ᰣ������
���ᰣ������ϵ��˾�����з����й���һ��С���Ӱ���ҩ�����������Ʊ�Ƥ�����������壨EGFR�������������ͻ��ľֲ����ڻ�ת���Է�Сϸ���ΰ���NSCLC�����ߵ�һ�����ơ���˾��2011��6�»�ȡ���ᰣ������������������ؿ���֧��ת�������ʲ����ò�Ʒ��������ϵ��˾Ŀǰ��ҪӪҵ���뼰������Դ��
��4��MIL60��ĿȨ��
MIL60����������/����̩�˹�˾��Avastin������������������ҩ�������Ѫ����������VEGF�İ�����ҩ��������Ʒ�Сϸ���ΰ�����ֱ���������ٰ��ȶ��ʵ������Ӧ֢��
2017��3�¹�˾�뱱�����ʵ���\���ɷ�����˾ǩ������Э�飬��MIL60������Ŀ��չ������ȡ�������Եġ����ҵġ��������ɵ�MIL60����������������ҩ��ƷȨ�档��˾����ò�Ʒ���ٴ��������顢�ٴ����ں�IJ�Ʒ�о����鹤�����걨ע��Ͳ�Ʒ��ҵ����
2017��4�¹�˾�����з���Ŀ���Ƚ�MIL60�Ͱ�ά͡�ֱ�������ɼ��+�����������ڻ��Է���״ϸ����Сϸ���ΰ����λ��ߵ���Ч�ԺͰ�ȫ�Ե������˫ä��������III���о�������չ�����о�������Ŀǰ������Ŀ�걨BLA�ѻ��������
��5��MRX-2843��ĿȨ��
MRX-2843��ӵ��ȫ�»�ѧ�ṹ��Mer�Ұ��ἤø��MerTK����FMS���Ұ���ø3��FLT3��˫�����Ƽ���������MerTK��FLT3ͨ·��������ʵ����
���ơ�2017��7�£���˾��200����Ԫ���MRX-2843���й������Ȩ�棬����MRX-2843���й����з����걨������
2017��11�£���˾����MRX-2843��Ŀ����С�鲢�����з���Ŀ�������й��걨IND���з�������Ŀǰ������Ŀ�����ٴ�I�����顣
��6��X-396
X-396����ɳ��������Ŀǰȫ�����ڿ����ĵڶ�����ALK���Ƽ�������������ALKͻ��ķΰ����ߣ��ɹ�˾�ع��ӹ�˾Xcovery��˾����������
Ŀǰ��˾���ڸü������е���Ŀ�������ں���Ķ����ٴ���Ŀ������X-396����ALK����NSCLC���������ٴ����������X-396�Ĺ��ʶ����ķΰ�III���ٴ����顣
��7��D-0316��ĿȨ��
D-0316�����淽����Ƽ����Ϻ�������˾�����з���ȫ�µ�����EGFR���Ƽ���2018��12�¹�˾���淽����Ƽ����Ϻ�������˾ǩ��������Э�顷������D-0316��Ŀ�й�Ȩ�棨�����й���½����ۺ�̨�壩��������Լ�������ڽ���D-0316��Ʒ�Ŀ�������ҵ����
���ڸü�������˾�ֱ���2019��1�º�2019��12�������з���Ŀ��D-0316��EGFRͻ��ֲ����ڻ�ת���Է�Сϸ���ΰ������еĢ����ٴ����顱�͡�D-0316�ڼ���δ�����Ƶ�EGFR����ͻ��ֲ����ڻ�ת���Է�Сϸ���ΰ������е�II/III���ٴ����顱������������ĿĿǰ�����ڻ�������Ρ�
��8��MCLA-129��ĿȨ��
MCLA-129���ɺ���Merus��˾�з�����EGFR��c-MetΪ�е��˫�����Կ��塣2019��1�£���˾�����Merus��˾���ս�Ժ��������MCLA-129��Ŀ��EGFR & cMet˫�������й��Ŀ�������ҵ���Ķ�����Ȩ��ͬʱ����˾�����з���Ŀ������MCLA-129����IND�걨��Ŀǰ����Ŀ�д����ٴ�ǰ�з��Ρ�
��9��X-82
X-82��ָ��˾�ӹ�˾Equinoxӵ�е�X-82��Vorolanib������ʲ��Լ�������Ӧ֢���ۿ���Ӧ֢�ĺ���Ȩ�档X-82ָһ�����Ѫ����Ƥ�����������壨VEGFR����ѪС���ܻ������������壨PDGFR���е�Ŀڷ����Ƽ���Ŀǰ����Ŀ�����ٴ�����Ρ�
��10��CM082
CM082��Vorolanib��ΪVEGFR��PDGFR�ȵĶ�е������Ұ��ἤø��RTKs�����Ƽ���������Ͷ������õ��ŵ���ж�����Ĺ㷺Ӧ���龰��Ŀǰ���������������۵ư߲���ȶ����Ӧ֢����2017���ϰ��꣬��˾����4.8��Ԫ�����ȫ���չ����ϼ�ҽҩ�Ƽ����Ϻ�������˾��ȡ��CM082��Ŀ���й������ȫ��Ȩ�档
Ŀǰ���ڽ��е���Ҫ�ٴ��о�����CM082������άĪ˾��������������ЧII/III���ٴ��о���CM082Ƭ����JS001ע��Һ��������ճĤ��ɫ����������Ч�Ͱ�ȫ�Ե��ٴ��о�����������������۵ư߱��Եĵ�ҩ���顣
����������������ֹʹ�༰���ᰣ�����������������⣬����������ĿȨ�����ר����ר�м�������˾��������к����з�������Ŀ�з���չ˳��������ʹ�ü�ֵ��
��������ֵ���Լ���ֵ��������������������ʲ�Ϊ��˾������Ч�����˵����ؼ�ֵ�������Ƿ���
�����ʲ���ֵ�������ݡ���ҵ������8�š����ʲ���ֵ���������ж��Ƿ����ʹ��������ȷ���������ʲ�������ʹ��������ȷ���������ʲ�Ӧ�����м�ֵ���ԣ����ڷ�ʹ��������ȷ���������ʲ��ж��Ƿ���ڿ��ܷ�����ֵ�ļ�����Σ�����ڼ�ֵ�ļ����ٹ�������ջؽ�����ջؽ��ļ������������ʲ��Ŀ��ջؽ������������ֵ�ģ����ȷ��Ϊ�ʲ���ֵ��ʧ������Ӧ���ʲ���ֵ�������뵱�����档
���ݡ���ҵ������8��--�ʲ���ֵ���涨���������м���ģ������ʲ����ܷ����˼�ֵ���ʲ����м۵��ڴ�����µ�����������Ը�����ʱ������ƻ�������ʹ�ö�Ԥ�Ƶ��µ�����ҵ��Ӫ�����ľ��á��������߷��ɵȻ����Լ��ʲ�
�������г��ڵ��ڻ��߽��ڽ��ڷ����ش�仯���Ӷ�����ҵ��������Ӱ�죻�г����ʻ��������г�Ͷ�ʱ������ڵ����Ѿ���ߣ��Ӷ�Ӱ����ҵ�����ʲ�Ԥ��δ���ֽ�������ֵ�������ʣ������ʲ����ջؽ�����Ƚ��ͣ���֤�ݱ����ʲ��Ѿ��¾ɹ�ʱ������ʵ���Ѿ����ʲ��Ѿ����߽������á���ֹʹ�û��ƻ���ǰ���ã���ҵ�ڲ������֤�ݱ����ʲ��ľ��ü�Ч�Ѿ����ڻ��߽�����Ԥ�ڣ����ʲ�������ľ��ֽ���������ʵ�ֵ�Ӫҵ�����߿���ԶԶ���ڣ����߸��ڣ�Ԥ�ƽ��ȣ����������ʲ������Ѿ�������ֵ�ļ��������ڣ���˾������ʹ��������ȷ���������ʲ�������ÿ��������ĩ����ʹ��������ȷ���������ʲ�δ������ֵ����δ������Ӧ��ֵ����
��������ֹʹ���BPI-3006�ֱ���2014���2017��̯����ϣ������ֵΪ�㣬�����ڼ�ֵ��
���������ʲ�Ϊ��˾������Ч������Լ��Ƿ���ڼ�ֵ����ľ����ж����£�
��1�����ᰣ������
���ᰣ�����ἴ�������ǹ�˾��һ��������������Ĵ���ҩ����2011���������ۣ�Ϊ��˾��ҪӪҵ���뼰������Դ�����������������������������������2019��ʵ������1,501,824,533.94Ԫ�����Ű��������������ҽ��Ŀ¼���һ���ҩ��Ŀ¼��Ԥ��δ���������뽫�����������ʲ����ڼ�ֵ����
��2��MIL60��ĿȨ��
2019��12��5�գ���˾���MIL60��Ŀ��չ����Ч������������ʾ�ﵽ��Ҫ�о��յ㡣����2015��ԭ����ʳƷҩƷ�ල�����ַܾ����ġ���������ҩ�з������ۼ���ָ��ԭ�����У�����MIL60��˳���������Ҫ����뱴���鵥��ԭ��ҩ��ά͡�ٴ�ǰ�ȶ��о����ٴ�ҩ������ѧ�ȶ��о����Լ��ٴ�III����Ч�Աȶ��о��ȣ�Ŀǰ��Ŀ�걨BLA�ѻ������������Ŀ�з���չ���ã���Ŀ���ȳ������£������ڼ�ֵ����
��3��MRX-2843��ĿȨ��
2019��1��28�գ�MRX2843Ƭ����ٴ�����֪ͨ�飬��������ٴ�ʵ��Σ���Ŀ��չ���ã������ڼ�ֵ����
��4��X-396
ĿǰX-396�Ķ����ٴ��о�˳���ƽ��У����С�X-396���ڿ���������ҩALK����NSCLC���ߵĢ����о�����������鹤������ɻ�����Ч�Ͱ�ȫ�����ݵ��ռ����ܺͶ�����Ч���۹��������ύ����NDA�����������Ŀǰ��������Ρ�
ͬʱ��X-396�Ĺ��ʶ����ķΰ�III���ٴ�����Ҳ�ڽ����У��й�����ȫ��������ȫ���������飬Ŀǰ���ڻ�����ýΡ�X-396�Ķ����ٴ��о���չ���ã������ڼ�ֵ����
��5��D-0316��ĿȨ��
ĿǰD-0316�������ٴ��о���˳���ƽ�����D-0316��EGFRͻ��ֲ����ڻ�ת���Է�Сϸ���ΰ������еĢ����ٴ����顱�͡�D-0316�ڼ���δ�����Ƶ�EGFR����ͻ��ֲ����ڻ�ת���Է�Сϸ���ΰ������е�II/III���ٴ����顱��Ŀ�����ڻ�������Ρ�
D-0316�����������ٴ��о���չ���ã������ڼ�ֵ����
��6��MCLA-129��ĿȨ��
MCLA-129��Ŀϵ��˾2019����������Ŀ��MCLA-129�ܹ�������NSCLC����Ⱥ���������ڵĶ�EGFR�������Ʋ�����ҩ�Ե�δ������ٴ�����Ŀǰ����Ŀ�д����ٴ�ǰ�о��Σ������ڼ�ֵ����
��7��X-82
X-82��Ŀ���ڽ����ٴ����飬���ڻ�������Σ���Ŀ���ȳ������£������ڼ�ֵ����
��8��CM082
ĿǰCM082�Ķ����ٴ��о�˳���ƽ��У����С�CM082������άĪ˾��������������ЧII/III���ٴ��о��������ȫ���������飬Ŀǰ���ڽ��л�����ã���CM082Ƭ����JS001ע��Һ��������ճĤ��ɫ����������Ч�Ͱ�ȫ�Ե��ٴ��о��� II�ڽ��������III���ٴ����顣ͬʱ����������������۵ư߱�����Ŀ���ڽ���II���ٴ����顣�������������������ĿȨ����з���Ŀ��˳���ƽ��������ʲ������ڼ�ֵ������������ֵ����
�����з�֧���ʱ��������������ݣ��Ƿ�һ���ԣ��������һ��ĩ����֧�������Ŀ����Ҫ���ݣ������ʱ���������˵���������Ŀ��չ������Ƿ�������ƽ�����һ���з���ֵ���ڹ��˵����Σ��Ƿ�Ӧ�����ֵ�����������з������ʱ�����������ӵ�ԭ������
��һ���з�֧���ʱ��������������ݣ��Ƿ�һ����
��˾��ϴ���ҩ�з���ҵ���ص㣬���ݡ���ҵ������6�š������ʲ����ƶ����з�֧���ʱ����Ļ�����ߣ��������£�
1�������о��κͿ����εľ������
��˾�ڲ��о�������Ŀ��֧����Ϊ�о���֧���Ϳ�����֧����
�о��Σ�Ϊ��ȡ�������µĿ�ѧ����֪ʶ�ȶ����еĶ����Ե��мƻ����顢�о���ĽΡ�
�����Σ��ڽ�����ҵ��������ʹ��ǰ�����о��ɹ�������֪ʶӦ����ij��ƻ�����ƣ����������µĻ����ʵ���ԸĽ��IJ��ϡ�װ�á���Ʒ�Ȼ�ĽΡ�
2��������֧���ʱ����ľ�������:
����1��2����ҩ���Կ�ʼ����չʵ����III���ٴ�����ǰΪ�о��Σ��Կ�ʼ��չʵ����III���ٴ�������ȡ�������������ڼ�Ϊ�����Ρ�
����3�����ҩ���Կ�ʼ��ȡ���ٴ������������ڼ�Ϊ�о��Σ�ȡ���ٴ�������������ȡ�������������ڼ�Ϊ�����Ρ�
����4�����ҩ�������з�����Ϊ�о��Σ�����������֧�������Է��û���
�������������ҩ������ҩ����Կ�ʼ��ȡ���ٴ������������ڼ�Ϊ�о��Σ�ȡ���ٴ�������������ȡ�������������ڼ�Ϊ�����Ρ�
�����Ԣ����ٴ�����֧�������������ҩ�з���Ŀ���Կ�ʼ����չʵ���Ԣ����ٴ�����ǰΪ�о��Σ��Կ�ʼ��չʵ���Ԣ����ٴ�������ȡ�������������ڼ�Ϊ�����Ρ�
��˾�����������з�֧���ʱ������߱���һ�£�Ԥ��δ����˾�з���������Ӫ�����ڲ��ᷢ���ش�仯�����������ֻ�����ߵ�һ���ԡ�
�������������һ��ĩ����֧�������Ŀ����Ҫ���ݣ������ʱ���������˵��
����2019��ĩ����˾����֧�������Ŀ������£�
| �з���Ŀ | ���� | �ʱ������ | |
| 1.1 | ��һ��ALK���Ƽ�X-396����ҩ | 1����ҩ | III���ٴ����� |
| 1.2 | ��һ��ALK���Ƽ�X-396������ҩ | 1����ҩ | �����ٴ����飨�����ٴ�����֧���������룩 |
| 1.3 | MIL60��Ŀ | ���������ҩ������ҩ� | III���ٴ����� |
| 1.4 | CM082��Ŀ | 1����ҩ | ʵ����III���ٴ����� |
| 1.5 | D-0316��Ŀ������ҩ | 1����ҩ | �����ٴ����飨�����ٴ�����֧���������룩 |
| 1.6 | D-0316��Ŀһ����ҩ | 1����ҩ | ʵ����III���ٴ����� |
�����з���Ŀ����Ҫ���ݼ������ʱ����������˵�����£�
��1����һ��ALK���Ƽ�X-396����ҩ
X-396����ɳ���ᣩ����Է�Сϸ���ΰ�����һ��ALK���Ƽ����ٴ������ڿ���������ҩ���߲����ܵ�ALK���Ե�NSCLC���ߣ�����1.1����ҩ��
��˾�ӹ�˾Xcovery��˾�������FDA��,���ڿ�չX-396����ALK����NSCLCһ�����Ƶ�III���ٴ��о������������������������롣ͬʱ�ɱ���
ҩҵ�ƶ���ʵʩX-396����ALK����NSCLCһ�������ٴ�III��(ȫ�������)�й������ٴ����飬�������й����������������롣
���ݹ�˾�Ļ�����ߣ�����Ŀ��III���ٴ����鿪ʼ�ʱ������Ϲ涨��
��2����һ��ALK���Ƽ�X-396������ҩ
X-396����ɳ���ᣩ������ҩ��Ҫ��ָ��X-396���ڿ���������ҩALK����NSCLC���ߵĢ����о�����Ŀ�����������������������ƺ��չ��ALK����NSCLC���Լ�ROS1��������NSCLC���ߡ����о���Ϊע�����о����������Ԣ����ٴ�����֧�������������ҩ�з���Ŀ�����ݹ�˾�Ļ�����ߣ�����Ŀ�Կ�չ�����ٴ����鿪ʼ�ʱ������Ϲ涨��
��3��MIL60��Ŀ
MIL60��Ŀ��ָ���Ƚ�MIL60�Ͱ�ά͡�ֱ�������ɼ��+�����������ڻ��Է���״ϸ����Сϸ���ΰ����λ��ߵ���Ч�ԺͰ�ȫ�Ե������˫ä��������III���о�����Ŀ��MIL60����������/����̩�˹�˾��Avastin������������������ҩ�������Ѫ����������VEGF�İ�����ҩ��������Ʒ�Сϸ���ΰ�����ֱ���������ٰ��ȶ��ʵ������Ӧ֢���������������ҩ������ҩ�������������ҩ��
���ݹ�˾�Ļ�����ߣ�����Ŀ��ȡ���ٴ�����������ʼ�ʱ�������˾�뱱�����ʵ���\���ɷ�����˾ǩ������Э��Լ����˾����ò�Ʒ���ٴ��������飬�ʸ���Ŀ�ʱ������Ϲ涨��
��4��CM082��Ŀ
CM082��Ŀ��Ҫ��ָ��CM082������άĪ˾��������������ЧII/III���ٴ��о����з���Ŀ�����о���ơ���ҩ�����Լ���Ч�۲�����ۿ�������Ŀ�Ѿ�����ʵ�����ٴ�III�ڽΣ��������ﵽ�յ㣬�����������У��ʷ����ʱ���������
��5��D-0316��Ŀ������ҩ
D-0316��һ������EGFR-T790M�Ұ��ἤø���Ƽ���D-0316��Ŀ������ҩ��Ҫ��ָ��D-0316��EGFRͻ��ֲ����ڻ�ת���Է�Сϸ���ΰ������еĢ����ٴ����顱��Ŀ�����о���Ϊע�����о����������Ԣ����ٴ�����֧�������������ҩ�з���Ŀ�����ݹ�˾�Ļ�����ߣ�����Ŀ�Կ�չ�����ٴ����鿪ʼ�ʱ������Ϲ涨��
��6��D-0316��Ŀһ����ҩ
D-0316��Ŀһ����ҩ��Ҫ��ָ��D-0316�ڼ���δ�����Ƶ�EGFR����ͻ��ֲ����ڻ�ת���Է�Сϸ���ΰ������е�II/III���ٴ����顱�з���Ŀ�����о���ơ���ҩ�����Լ���Ч�۲�����ۿ�������Ŀ�Ѿ�����ʵ�����ٴ�III�ڽΣ��������ﵽ�յ㣬�����������У��ʷ����ʱ���������
�����������Ŀ��չ������Ƿ�������ƽ�����һ���з���ֵ���ڹ��˵����Σ��Ƿ�Ӧ�����ֵ
����Ŀǰ����˾����֧�������Ŀ��չ������£�
| ��Ŀ���� | ��Ŀ��չ��� | |
| 1.1 | ��һ��ALK���Ƽ�X-396����ҩ | �����ٴ�III�����飬�����ȫ���������飬Ŀǰ���ڽ��л�����ã�Ԥ��2021���걨 NDA�� |
| 1.2 | ��һ��ALK���Ƽ�X-396������ҩ | CDE�����У��ѵݽ�ҩѧ������ϣ�Ԥ��2020��NDA������ |
| 1.3 | MIL60��Ŀ | �걨BLA���������Ԥ��2021����CDE����ͨ���� |
| 1.4 | CM082��Ŀ | CM082���������ٴ���/������Ŀ�����ȫ���������飬Ŀǰ���ڽ��л�����ã�Ԥ��2021���걨NDA�� |
| 1.5 | D-0316��Ŀ������ҩ | �����ٴ�II�����飬���ڽ��л������飬Ԥ��2021���걨NDA�� |
| 1.6 | D-0316��Ŀһ����ҩ | �����ٴ���/�������飬���ڽ��л������飬Ԥ��2022���걨NDA�� |
���ϱ���ʾ����˾����֧�������Ŀ����˳�����У����������ƽ�������һ���з���ֵ���ڹ��˵����Ρ�
���ݡ���ҵ������8��--�ʲ���ֵ���涨���������м���ģ������ʲ����ܷ����˼�ֵ���ʲ����м۵��ڴ�����µ�����������Ը�����ʱ������ƻ�������ʹ�ö�Ԥ�Ƶ��µ�����ҵ��Ӫ�����ľ��á��������߷��ɵȻ����Լ��ʲ�
�������г��ڵ��ڻ��߽��ڽ��ڷ����ش�仯���Ӷ�����ҵ��������Ӱ�죻�г����ʻ��������г�Ͷ�ʱ������ڵ����Ѿ���ߣ��Ӷ�Ӱ����ҵ�����ʲ�Ԥ��δ���ֽ�������ֵ�������ʣ������ʲ����ջؽ�����Ƚ��ͣ���֤�ݱ����ʲ��Ѿ��¾ɹ�ʱ������ʵ���Ѿ����ʲ��Ѿ����߽������á���ֹʹ�û��ƻ���ǰ���ã���ҵ�ڲ������֤�ݱ����ʲ��ľ��ü�Ч�Ѿ����ڻ��߽�����Ԥ�ڣ����ʲ�������ľ��ֽ���������ʵ�ֵ�Ӫҵ�����߿���ԶԶ���ڣ����߸��ڣ�Ԥ�ƽ��ȣ����������ʲ������Ѿ�������ֵ�ļ���˾�ڱ�����ĩ�Կ���֧�������Ŀ���������飬δ���ֿ���֧����Ŀ���ڼ�ֵ������������ֵ��
���ģ����������з������ʱ�����������ӵ�ԭ������
�����ڸ���ĩ����֧��������£�
��λ����Ԫ
| ��Ŀ | 2019����ĩ | 2018����ĩ | 2017����ĩ | 2016����ĩ |
| ��������[ע] | - | 858.11 | 858.11 | 858.11 |
| ��һ��ALK���Ƽ�X-396����ҩ | 55,529.98 | 38,967.32 | 21,961.23 | |
| ��һ��ALK���Ƽ�X-396������ҩ | 7,351.80 | 3,154.66 | ||
| MIL60��Ŀ | 14,158.66 | 9,470.16 | 3,274.81 | |
| CM082��Ŀ | 7,918.92 | 3,964.73 | 1,687.16 | |
| D0316��Ŀ | 6,277.77 | |||
| �ϼ� | 91,237.14 | 56,414.98 | 27,781.31 | 858.11 |
ע�����ڹ��ڷ���ҩ���ߡ��г��������ش�仯��Ϊִ�й�˾�Դ���ҩ�з�Ϊ���ĵ�ս��ѡ����Դ�������úͼ�ֵʵ����ĽǶȳ���������˾�ۺ�������������ټ�����������������Ŀ�����������ƽ�����ҩ��Ŀ�IJ�ҵ�����̡������ڸ����з��ʱ������������£�
��λ����Ԫ
| ��Ŀ | 2019�� | 2018�� | 2017�� | 2016�� |
| �������� | - | - | - | 18.49 |
| ��һ��ALK���Ƽ�X-396����ҩ | 16,043.61 | 16,107.40 | 21,961.23 | - |
| ��Ŀ | 2019�� | 2018�� | 2017�� | 2016�� |
| [ע2] | [ע1] | |||
| ��һ��ALK���Ƽ�X-396������ҩ | 4,197.15 | 3,154.66 | - | - |
| MIL60��Ŀ | 4,688.50 | 6,195.34 | 3,274.81 | - |
| CM082��Ŀ | 3,954.19 | 2,277.58 | 1,687.16 | - |
| D0316��Ŀ | 6,277.77 | - | - | - |
| �ϼ� | 35,161.22 | 27,734.98 | 26,923.20 | 18.49 |
ע1����һ��ALK���Ƽ�X-396����ҩ2017�����Ӷ�Ϊ21,961.23��Ԫ������9,132.22��Ԫϵ�ϲ����ӣ�����12,829.00��Ԫϵ��˾Ͷ�����ӡ�ע2�������ʱ����������������������ӽ�
2017���ʱ�������������������Ҫϵ����MIL60��CM082��X-396���ʱ����з���Ŀ���¡�2017�깫˾�뱱�����ʵ���\���ɷ�����˾ǩ������Э�飬ȡ��MIL60��ĿȨ�棬����ʼ�ٴ��������飬�з����ÿ�ʼ�ʱ�����ͬ�꣬��˾�չ����ϼ�ҽҩ�Ƽ����Ϻ�������˾�Լ�Xcovery Holdings,Inc.������CM082��Ŀ�Լ���һ��ALK���Ƽ�X-396����ҩ�ʱ�����Ŀ��
2018���ʱ���������������811.78��Ԫ����Ҫϵԭ���ʱ�����Ŀ����Ͷ�������Լ�������һ��ALK���Ƽ�X-396������ҩ�ʱ�����Ŀ�����ڶ�ɳ����������ص㼰ͬ��ҩ��������Ӧ֢����˾���չX-396�Ķ�����ҩ�з���Ŀ������Ŀ��Ϊע�����ٴ��о���Ŀ��������з����ü��뿪��֧����
2019���ʱ���������������7,426.24��Ԫ����Ҫϵԭ���ʱ�����Ŀ����Ͷ�������Լ�����D0316�ʱ�����Ŀ��2018��12�¹�˾���淽����Ƽ����Ϻ�������˾ǩ������Э�飬ȡ��D-0316��ĿȨ�棬�������з�D-0316��Ŀ������ҩ��D-0316��Ŀһ����ҩ���������ʱ�������������з����ü��뿪��֧����
���ϣ����������з������ʱ�����������ӣ���Ҫϵ��˾�����ʱ�����Ŀ��������Ͷ���з����£����к����ԡ�
������ϱ������ڹ�˾�з������ʱ�����������ļͶ��Ŀ��ҩ�з��ľ������˵������ļͶ��Ŀ�����з������Ƿ�����ʱ�������
�������ڹ�˾�з������ʱ�����������������5�ظ�֮�������һ��������
����ļͶ��ҩ�з���Ŀ����������£�
| ��Ŀ���� | ���� | �ʱ������ | |
| 1.1 | X-396����ALK����NSCLC���������ٴ����� | 1����ҩ | �����ٴ����飨�����ٴ�����֧���������룩 |
| 1.2 | X-396����ALK����NSCLCһ�������ٴ����� | 1����ҩ | III���ٴ����� |
| 1.3 | CM082���������ٴ���/���� | 1����ҩ | ʵ����III���ٴ����� |
| 1.4 | CM082����JS001����ճĤ��ɫ���������ٴ����� | 1����ҩ | III���ٴ����� |
| 1.5 | MIL60����״ϸ����Сϸ���ΰ������ٴ����� | ���������ҩ������ҩ� | III���ٴ����� |
| 1.6 | BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ����� | 1����ҩ | �����ٴ����飨�����ٴ�����֧���������룩 |
| 1.7 | BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/���� | 1����ҩ | ʵ����III���ٴ����� |
��Ϲ�˾������ߣ�����ļͶ��Ŀ�����з����þ������ʱ�������������������£�
��X-396����ALK����NSCLCһ�������ٴ�III�ڡ��Լ���CM082����JS001����ճĤ��ɫ���������ٴ����ڡ���Ŀ����1.1����ҩ����III���ٴ����鿪ʼ�ʱ��������ʱ���������
��X-396����ALK����NSCLC���������ٴ�II�ڡ��͡�BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ�II�ڡ���Ŀ��Ϊע�����о���������II���ٴ�����֧�������������ҩ�з���Ŀ���Ԣ����ٴ����鿪ʼ�ʱ����������ʱ���������
��MIL60����״ϸ����Сϸ���ΰ������ٴ����ڡ���Ŀ�������������ҩ������ҩ�����ȡ���ٴ�������ʼ�ʱ��������ݹ�˾�뱱�����ʵ���\���ɷ�����˾ǩ���ĺ���Э�飬��˾����ò�Ʒ���ٴ�III�����飩�������ʱ���������
��CM082���������ٴ���/���ڡ��͡�BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/���ڡ���Ŀ���о���ơ���ҩ�����Լ���Ч�۲�����ۿ����Ѿ����뵽ʵ�����ٴ����ڽΣ��������ﵽ�յ㣬�����������У��ʷ����ʱ���������
�ġ����������ͻ��ʦ�˲����
��һ���˲����
�������������������������˻��ʦ��ȡ�ĺ˲鷽ʽ�����������ڣ�
1����ȡ�����������ʲ����Э�飬���Э�����ݡ���������˽������ʲ���ĿȨ����Դ�����ݣ�
2����̸����з���Ա���˽���ҩ�з�������̡��ٴ���/��/III��ʵ�������ͻ��֡���ҵ��������˾�����ʲ�������з���Ŀ��չ����ȣ�
3�������˷����˼�ͬ��ҵ�ɱ����й�˾�з�֧���ʱ�����������Լ�����ҵ����Ĺ涨��
4����ȡ���з���Ŀ��ص��������ϡ��ٴ��������ٴ�֪ͨ�顢���������Լ�CDE��ͨ���ϣ������з���չ������Ƿ�����ʱ��������ȣ�
5����̸�������˺��з���Ա��ѯ���з������ʱ�������ڱ����ڸ��ڵĴ�����������������ԣ���ע�Ƿ���ڷ��ʱ�����֧�����뿪��֧���������
6�����˷����˶������ʲ�������֧��ִ�еļ�ֵ���������ѯ�ʷ����˸�������Ա�������ʲ�������֧����ֵ������жϹ��̣���ϻ�ȡ�����ⲿ��Ϣ�������Ƿ�ǡ����
�������˲����
���˲飬�������������ʦ��Ϊ��
1�������������ʲ�����ĿȨ�����ר����ר�м�������������������к����з�������Ŀ�з���չ˳��������ʹ�ü�ֵ��
2�������˶��з�֧���ʱ����Ļ�����߷��ϡ���ҵ����Ĺ涨�������˿���֧�������Ŀ��ļͶ��ҩ�з���Ŀ�������ʱ���������
3������������ĩ�������������ʲ�������֧������з���Ŀ��չ˳���������ڼ�ֵ������������ֵ����
4�����������з������ʱ�����������ӣ���Ҫϵ��˾�����ʱ�����Ŀ��������Ͷ���з����£����к����ԡ�
���������6��
���һ��ĩ�������������Ϊ4.14��Ԫ����ҪΪ�չ����ϼ�ҽҩ�Ƽ����Ϻ�������˾�γɡ��ù�˾���ʲ�Ϊ��ֵ����Ӫҵ���롣�������˲���˵������1�����ϼ�ҽҩ�Ƽ����Ϻ�������˾��Ӫҵ���������Ҫ�з�ҩƷ�Ľ�չ������Ƿ����Ԥ�ڣ���˾�ĺ������ƣ��չ��ÿ���˾��ԭ�����ԡ���2���չ��������ݣ��չ����۵Ĺ��ʺ����ԡ���3����ϱ��չ��ʲ���Ӫ״��������״�����չ�ʱ��������Ԥ��ҵ����ʵ���������������������ֵ������Ҫ������Ԥ�⼰ʵ������Լ���˾������������ȣ�˵��������ֵ������ij���Ժ����ԡ�
�뱣�����������ʦ�����˲������
�ظ���
һ�����ϼ�ҽҩ�Ƽ����Ϻ�������˾��Ӫҵ���������Ҫ�з�ҩƷ�Ľ�չ������Ƿ����Ԥ�ڣ���˾�ĺ������ƣ��չ��ÿ���˾��ԭ������
��һ�����ϼ�ҽҩ�Ƽ����Ϻ�������˾��Ӫҵ�����
1����Ҫҵ�����
��1����˾�����������
���ϼ�ҽҩ�Ƽ����Ϻ�������˾�����¼�ơ����ϼ�����λ���Ϻ����Ž��߿Ƽ�������˾ר�����ش��ֵ����ҩ�з������ϼ�������ҩ��ĿCM082���з���CM082ΪVEGFR��PDGFR�ȵĶ�е������Ұ��ἤø��RTKs�����Ƽ���������Ͷ������õ��ŵ���ж�����Ĺ㷺Ӧ���龰��Ŀǰ���������������۵ư߲���ȶ����Ӧ֢����
��2����˾��Ҫ�з���Ʒ����
1����������ҩ
���ϼ�������CM082ϵ2-����ͪ��е������Կ�����ҩ������������������ƹǼܽṹ��Ϊ��е������Ұ��ἤø���Ƽ�����������III�͡�V�������Ұ��ἤø����Ҫ����VEGFR��PDGFR��c-Kit��Flt-3�ȡ�����Ŀ���ڶ������������û��ƺͶ������ó���о��Ļ������з�����һ����Ʒ���ٴ��ϱ��ֳ����õİ�ȫ�Ժ�����Ч��������ҩ�ص������������ã��������ɼ������άĪ˾������ҩ�Է�Сϸ���ΰ�����ϸ�������Ȱ�֢��ͻ�����������á�
2���ۿ�
���ϼ��ѻ��CM082���ƶ���ۿ���Ӧ֢���ٴ�������������������Իư߱��ԣ�AMD�����������ư�ˮ�ס�����Ĥ���������̷��ư�ˮ�ס���������Իư߱��ԣ�AMD��������ȫ��50�꼰��������ʧ�������ԭ��10%��AMDΪ����Ѫ����©�ͣ���ʪ�ԣ������������ʧ��ȴռ��90%��ֱ������Ѫ����Ƥ��������/ѪС���������ӣ�VEGF/PDGF����ҩ��ɶ�ʪ��AMD�����������á�Ŀǰ�����ֿ�VEGF��ҩ�����ٴ��õ��㷺Ӧ�ã�Ҳ���ֳ����õ�����Ч����������Ϊ֪���ͳɹ��Ĵ���Ϊ���Ϲ�˾��Lucentis�����CM082���з���óɹ���������Ϊȫ���һ����Ч����ʪ����������Իư߱��ԣ�w-AMD���Ŀڷ�ҩ�����м��������ֵ��ѧ����ֵ��
3��ճĤ��ɫ����
���ϼ���2019���ѻ��CM082Ƭ����������������ע��Һ��JS001�����ڼ���δ�����Ƶľֲ���չ��ת����ճĤ��ɫ�������ٴ���������CM082����JS001����ճĤ��ɫ�������������II���ٴ����չ�����ٴ���
��3����Ҫ��������
1���ʲ���ծ���
��λ����Ԫ
| ��Ŀ | 2019��12��31�� | 2018��12��31�� | 2017��12��31�� |
| ���ʲ� | 102,81.37 | 7,051.14 | 5,629.02 |
| ��ծ | 11,747.51 | 7,427.11 | 4,706.29 |
| ������Ȩ�� | -1,466.14 | -375.97 | 922.73 |
2����Ӫҵ�����
��λ����Ԫ
| ��Ŀ | 2019��� | 2018��� | 2017��� |
| Ӫҵ���� | - | - | - |
| Ӫҵ���� | -1,125.83 | -1,356.24 | -676.16 |
| ������ | -1,090.17 | -1,298.70 | -670.25 |
Ŀǰ�����ϼ���Ҫ�Ǵ���CM082���з�ҵ���з�Ͷ��ϴ���δʵ��ӯ����
��������Ҫ�з�ҩƷ�Ľ�չ������Ƿ����Ԥ��
���ϼ�Ŀǰ�Ѿ����й���չCM082���ۿƣ�ʪ����������Իư߱��ԣ�w-AMD��������������JS001����ճĤ��ɫ�����ȼ������ٴ��������ֱ����II�ڡ�II/III���ٴ���II�ڽ����չ�����ٴ�����չ˳�������⣬��Բ����Խ�������Ĥ����Ѫ�ܣ�mCNV����I���ٴ��о�Ҳ���ƽ���
Ŀǰ����ע�����ٴ��ε���Ŀ��չʱ���������ʾ��
| �з���Ŀ | ��ҩƷ�� | ��; | ��չ��� | ������ɵĹ��� | Ԥ�ƻ����������ʱ�� |
| CM082���������ٴ���/���� | Vorolanib�����VEGFR��PDGFR�ȵĶ�е�ڷ����Ƽ�����ҩ1�� | ���ڼ���VEGFR-TKIһ������ʧ�ܵ�ת�������� | ��/�����ٴ�������ɻ������� | ��ɢ�/�����ٴ����飬�걨NDA������ͨ�� | 2021�� |
| CM082����JS001����ճĤ��ɫ���������ٴ����� | ���ھֲ���չ��ת����ճĤ��ɫ���������� | �����II���ٴ��������III���ٴ� | ���III���ٴ����飬�걨NDA������ͨ�� | 2023�� |
��������˾�ĺ������ƣ��չ��ÿ���˾��ԭ������
���ϼ�Ŀǰ��Ҫ���°�����ҩCM082���о�������CM082�ǿڷ�����һ����ҩ����һ��ȫ�½ṹ��VEGFR��PDGFRΪ���Ķ�е㼤ø���Ƽ���CM082�����������VEGFR��PDGFR�е��������Ч��ͬʱ�˷�����һ�����ҩ�����ĸ߶������ã����ڽ��е��ٴ��о�������������������۵ư߱��Եĵ�ҩ
���顢CM082����άĪ˾������ҩ��������ϸ���������顣CM082��ز�Ʒ���г��ռ�ϴ�������ظ����淴�����4֮���ġ�ļͶ��Ŀ��ز�Ʒ���г��ռ���������ٵľ���������Ƿ�����г����ز���Ԥ�ڵķ��ռ����ȡ��Ӧ�Դ�ʩ����
�չ���ɺ�˾���п��ϼ�100%��Ȩ��ӵ��CM082��Ŀ�й�����ȫ��Ȩ�棬���ڹ�˾���������ƽ���Ŀ���ٴ�������г�������
���ϣ������չ����к����ԡ�
�����չ��������ݣ��չ����۵Ĺ��ʺ�����
�����˶Կ��ϼ����չ��ֶ�����ɣ�
��һ����һ�����չ����ϼ�77.4091%��Ȩ
1���������
��������2017��2��26���뿨�ϼ����ֹɶ�ǩ���ˡ���Ȩת��Э�顷����˾��֧���ֽ�ķ�ʽ���ϼ�ʹ��37,156.368��Ԫ����˰�����ÿ��ϼ��ɶ��Ϻ����Ͷ�����ģ����ϻ���п��ϼ�13.6540%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ94.3855��Ԫ������������Ͷ������˾���п��ϼ�8.5846%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ59.3422��Ԫ�����Ϻ�Դ��Ͷ�ʹ�������˾���п��ϼ�0.1364%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ
0.9428��Ԫ�������˿���Ͷ�ʺϻ���ҵ�����ϻ���п��ϼ�11.0887%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ76.6527��Ԫ�����������п��ϼ�13.2758%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ91.7708��Ԫ�����ų������п��ϼ�4.2604%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ29.4505��Ԫ������ʤ�����п��ϼ�3.1653%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ21.8809��Ԫ���������ͳ��п��ϼ�1.1781%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ8.1435��Ԫ������������п��ϼ�0.9091%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ6.2842��Ԫ�����ڼ̻۳��п��ϼ�0.6818%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ4.7132��Ԫ������ϣң���п��ϼ�0.6818%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ4.7132��Ԫ������־�ճ��п��ϼ�0.4545%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ3.1421��Ԫ�������������п��ϼ�0.0909%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ0.6284��Ԫ����������п��ϼ�0.0909%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ0.6284��Ԫ�������������п��ϼ�
0.0639%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ0.4420��Ԫ���������ȳ��п��ϼ�7.8900%�Ĺ�
Ȩ����Ӧ���ʶ�Ϊ54.5409��Ԫ�������ճ��п��ϼ�7.6173%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ52.6558��Ԫ�����������п��ϼ�3.5856%�Ĺ�Ȩ����Ӧ���ʶ�Ϊ24.7857��Ԫ��������������ɺ�˾�����п��ϼ�77.4091%�Ĺ�Ȩ��
2017��3��16�գ�������2017���һ����ʱ�ɶ��������ͨ���������ֽ��չ����ϼ�ҽҩ�Ƽ����Ϻ�������˾���ֹ�Ȩ���鰸����2017��6��15�գ����ι�Ȩת�õĹ��̱����ɡ�
2����������
�������Ż��ʦ���������ߵġ����ϼ�ҽҩ�Ƽ����Ϻ�������˾��Ʊ��桷���Ż�ʦ����[2017]��ZF50004�ţ������ϼ�������2017��1��31��������Ȩ��Ϊ�����15,796,212.21Ԫ�������Ϻ������ʲ���������˾���ߵġ����ϼ�ҽҩ�Ƽ����Ϻ�������˾�ɶ�ȫ��Ȩ���ֵ��ֵ���桷�����������֣�2017����2001�ţ����ʲ���������������淨���������ϼ��ڹ�ֵ����2016��11��30�յĹɶ�ȫ��Ȩ���ֵΪ�����47,600.00��Ԫ��
��������ƺ���������Ļ����ϣ����������Ѻ�Э��ȷ�����ϼ��Ĺ�ֵΪ�����48,000.00��Ԫ����Ӧ�ı��ν��ױ�Ŀ��ϼ�77.4091%��Ȩ��ת�üۿ�ϼ�Ϊ37,156.368��Ԫ����˰����
�������ڶ������չ����ϼ�22.5909%��Ȩ
1���������
��һ���չ���ɺ��ϼ�������λ�ɶ��Ϻ��Ž�����ҽҩ��ҵ��ҵͶ������˾�����¼�ơ��Ž���������Ϻ��Ž��Ƽ���ҵͶ������˾�����¼�ơ��Ž���Ͷ����ͨ���Ϻ����ϲ�Ȩ����������������Ȩת����Ϣ������ת�÷ֱ���еĿ��ϼ�13.5000%��9.0909%�Ĺ�Ȩ�����Ƶ�Ϊ6,480.00��Ԫ��4,363.6320��Ԫ��Ϊȡ��CM082��Ŀ������Ȩ�棬������ί���Ϻ��ַ������ʲ���Ӫ��������˾���Ϻ����ϲ�Ȩ������������������Ȩ���ƣ�2017��6��16�շ��������Ž�������Ž���Ͷǩ���ˡ���Ȩ����ͬ�����������ʽ�10,843.6320��Ԫ����ժ���չ��Ž�������Ž���Ͷ�ֱ���еĿ��ϼ�13.5000%��9.0909%�Ĺ�Ȩ��2017��6��19�գ������˹�����ɹ���ժ���չ����ϼ�
22.5909%��Ȩ��ȫ�ʿعɿ��ϼ���2017��7��12�գ����ι�Ȩת�õĹ��̱����ɡ�
2����������
�����Ϻ������ʲ���������˾���ߵġ����ϼ�ҽҩ�Ƽ����Ϻ�������˾�ɶ�ȫ��Ȩ���ֵ��ֵ���桷�����������֣�2017����2001�ţ��������淨���������ϼ��ڹ�ֵ����2016��11��30�յĹɶ�ȫ��Ȩ���ֵΪ�����47,600.00��Ԫ�����ν��������淨���������Ϊ���ݣ��Ž�������Ž���Ͷͨ���Ϻ����ϲ�Ȩ��������������ת�ÿ��ϼ�22.5909%��Ȩ�Ĺ��Ƽ�Ϊ10,843.6320��Ԫ��
���ϣ������չ��Ķ��۾��й����Ժͺ����ԡ�
������ϱ��չ��ʲ���Ӫ״��������״�����չ�ʱ��������Ԥ��ҵ����ʵ���������������������ֵ������Ҫ������Ԥ�⼰ʵ������Լ���˾������������ȣ�˵��������ֵ������ij���Ժ�����
��һ�����չ��ʲ���Ӫ״��������״��
����������6�ظ�֮��һ�����ϼ�ҽҩ�Ƽ����Ϻ�������˾��Ӫҵ���������Ҫ�з�ҩƷ�Ľ�չ������Ƿ����Ԥ�ڣ���˾�ĺ������ƣ��չ��ÿ���˾��ԭ�����ԡ���
�������չ�ʱ��������Ԥ��ҵ����ʵ�����
�����չ�ʱ�Ϻ������ʲ���������˾���ߵġ����ϼ�ҽҩ�Ƽ����Ϻ�������˾�ɶ�ȫ��Ȩ���ֵ��ֵ���桷�����������֣�2017����2001�ţ����չ�ʱ��������Ԥ��ҵ����ʵ��������£�
��λ����Ԫ
| 2017��� | 2018��� | 2019��� | |
| Ԥ��ҵ�� | |||
| Ӫҵ���� | |||
| Ӫҵ���� | -1,587.83 | -1,742.64 | -1,997.45 |
| ������ | -1,587.83 | -1,742.64 | -1,997.45 |
| 2017��� | 2018��� | 2019��� | |
| ʵ��ҵ�� | |||
| Ӫҵ���� | - | - | - |
| Ӫҵ���� | -676.16 | -1,356.24 | -1,125.83 |
| ������ | -670.25 | -1,298.70 | -1,090.17 |
2017�����2019��ȣ����ϼ�ʵ��ҵ�����չ�ʱ����Ԥ��ҵ���������ش���죬�����չ�ʱ����Ԥ�������2017��2019��ȴ����з��Σ�Ԥ��2020���Ʒ���У���ʼʵ��ӯ����
��������ϱ�������������ֵ������Ҫ������Ԥ�⼰ʵ������Լ���˾�����������˵��������ֵ������ij���Ժ�����
��˾���ݡ���ҵ������8�ţ��ʲ���ֵ��������ҵ������20�š���ҵ�ϲ������йع涨��ÿ��Է�ͬһ��������ҵ�ϲ��γɵĿ��ϼ����������м�ֵ���ԣ����ݵ����۾������ߡ���ҵ��չ���ơ���ҵʵ���з���Ӫ״����Ӱ�����أ�����ҵδ����Ӫ״�����к����жϼ��滮�������������롢�������������ʵȹؼ�ָ�ꡣ
1���ʲ���ֵ�����Ͳ��Թ���
��˾���ݡ���ҵ������ 8 �š��ʲ���ֵ������ع涨��������ֵ���������������ʲ���Ŀ��ջؽ��Ϊ�����������������ʲ���Ŀ��ջؽ��Ӧ�������ʲ���Ԥ��δ���ֽ���������ֵ���ʲ��鹫�ʼ�ֵ��ȥ���÷��ú�ľ�������֮��Ľϸ���ȷ����
���ڹ�˾��������ص��ʲ���û�г�����ͼ������������Э��۸����ʲ���Ҳ��Ծ�����г��������ɿ���������ʲ���Ĺ��ʼ�ֵ��ȥ���÷��ú�ľ����˹�˾��������ֵ�����У�������ʲ���Ԥ��δ���ֽ���������ֵ��Ϊ����ջؽ����о�����Թ������£�
���β���˰ǰ�ֽ�������ģ��ȷ���ʲ����ֽ�����ֵ��������㹫ʽ���£�
ʽ�У�
��˰ǰ��ҵ�����ֽ�����ֵ����δ����i���˰ǰ��ҵ�����ֽ������������ڵ�˰ǰ��ҵ�����ֽ�������˰ǰ�����ʣ�����ȷ��Ԥ���ڡ�������Թ������£�
��λ��Ԫ
| ��Ŀ | ��ʽ | ��� |
| ���������� | A | 413,584,000.09 |
| ������ֵ����� | B | 0.00 |
| ���������ֵ | C=A-B | 413,584,000.09 |
| δȷ�Ϲ����������ɶ�Ȩ���������ֵ | D | 0.00 |
| ����δȷ�Ϲ��������ɶ�Ȩ���������ֵ | E=C+D | 413,584,000.09 |
| �ʲ���������ֵ | F | 92,772,375.11 |
| ���������������ʲ���������ֵ | G=E+F | 506,356,375.20 |
| �ʲ���Ԥ��δ���ֽ���������ֵ�����ջؽ� | H | 859,000,000.00 |
| ������ֵ��ʧ����H-G<0ʱ����ֵ��ʧ�� | I=H-G | 0.00 |
| ĸ��˾�ֹɱ��� | J | 100% |
| �ϲ�����������ֵ��ʧ | K | 0.00 |
���������δ�����ֽ�������ֵ�����������ʲ��������ֵ����δ����������ֵ����
2����Ҫ������ѡȡ������
δ�����ֽ�������ֵ��Ҫ������Ԥ�������Ŀ��ʼ��Ӫʱ�䡢Ӫҵ���뼰�����ʡ�Ӫҵ�ɱ���˰���ӡ����ۡ��������з������Լ�������Ԥ�⡣����������£�
��1����Ŀ��ʼ��Ӫʱ��
Pi
R
i
R
nR
nRr
rn
CM082��Ŀ�д����з��Σ���δ�γɾ�Ӫ�ֽ������ʱ���������Ҫϵ�з���Ͷ�룬�����з�Ͷ��ʵ�ʺ�Ԥ��������첻���з���Ŀ��չ�練�����6֮����һ���������������չ����Ԥ�ڡ�������ĩ��˾���ݸ���Ŀ�з����ȼ������ҵ��������ߵ�Ӱ�죬������ĿԤ�Ƶ�����ʱ�䣬���У���1��CM082������Ŀ����2019��6����������飬2020��ƻ����II/III���ٴ����飬2021�����У���2��CM082�ۿ���Ŀ���ƻ�2022������ٴ�III�����飬2023�����У���3��CM082��ɫ������Ŀ���ƻ�2022�����CDE���������ٴ����飬2023�꿪ʼ���С�
��2��Ԥ����Ӫҵ���뼰������
��λ����Ԫ
| Ӫҵ���� | 2021��� | 2022��� | 2023��� | 2024��� | 2025��� | 2026��� | ������ |
| ���� | 11,434.50 | 15,367.97 | 19,414.93 | 23,541.45 | 23,541.45 | 23,541.45 | 23,541.45 |
| �ۿ� | 14,053.13 | 15,848.45 | 17,474.69 | 19,247.16 | 19,247.16 | ||
| ��ɫ���� | 1,270.08 | 1,641.12 | 2,036.95 | 2,460.61 | 2,460.61 |
����������Ʒ�д����з��Σ���������ʷ���ݲο�������Ԥ��ϵ����ҩƷ��Ӧ֢����ʷ��ҩ�������г������ʼ�ͬ��ҩƷ�г��������������Ԥ�����г�ռ���ʼ��г�����ͬ���Ʒ�ļ۸�Ŀǰ�ٴ���ҩ�����е���Ѽ������㻼�����ƽ����ҩ�ɱ���������ҩ�۸�ο�ͬ���Ʒҽ���۸�ͬʱҲ������ҽ�����۵����ߵ�Ӱ�졣
��3��Ӫҵ�ɱ�
��λ����Ԫ
| Ӫҵ�ɱ� | 2021��� | 2022��� | 2023��� | 2024��� | 2025��� | 2026��� | ������ |
| ���� | 518.36 | 774.09 | 1,085.11 | 1,459.71 | 1,459.71 | 1,459.71 | 1,459.71 |
| �ۿ� | 1,107.16 | 1,379.05 | 1,697.96 | 2,077.98 | 2,077.98 | ||
| ��ɫ���� | 43.18 | 62.00 | 85.50 | 114.87 | 114.87 |
����Ŀǰ��Ʒ�߹滮��������Ʒ��ί���ⲿ��ҵ�������ɹ�˾�ṩԭ�Ϻ���Ҫ���ϣ������˳е����ָ������ϳɱ��������չ�˾Ҫ��ӹ����ﲢ��ȡ�ӹ��ѡ��ڴ�ģʽ�£�Ӫҵ�ɱ���Ҫϵ����������Ʒ��Ҫԭ���ϲɹ��ɱ�����ɱ����㡣
��4��˰����
��λ����Ԫ
| ˰���� | 2021��� | 2022��� | 2023��� | 2024��� | 2025��� | 2026��� | ������ |
| �ϼ� | 177.26 | 237.56 | 532.75 | 626.97 | 656.12 | 687.45 | 687.45 |
Ӫҵ˰����ϵ���ݲ�����˰���ֺܾ��������ġ��������ֵ˰�ĸ��й����ߵĹ��桷��������˰���ֺܾ�������2019���39�ţ���������2019��4��1����ִ�еĵ���ֵ˰˰�ʼ��㣬��13%�����ó���ά������˰7%�������Ѹ���3%���ط��������ӷ�2%��ӡ��˰˰��Ϊ��ǩ��ͬ�����֮��������ʹ��˰Ϊ1,200Ԫÿ��ÿ�ꡣ
��5�����ۡ��������з�����
��λ����Ԫ
| ��Ŀ | 2021��� | 2022��� | 2023��� | 2024��� | 2025��� | 2026��� | ������ |
| ���۷��� | 4,002.08 | 5,378.79 | 12,158.35 | 14,360.86 | 15,068.58 | 15,837.23 | 15,837.23 |
| �������� | 1,325.39 | 1,325.36 | 2,835.18 | 2,840.19 | 2,845.47 | 2,796.29 | 2,796.29 |
| ����� | 1,264.48 | 1,327.70 | 1,394.09 | 1,463.79 | 1,536.98 | 1,613.83 | 1,613.83 |
���۷���ϵ���ݹ�˾��ʷ���۷����ʼ��㣬��˾���ϲ��Ƕȣ����������۷��������£�
| ��Ŀ | 2019��� | 2018��� | 2017��� | 2016��� | 2015��� |
| ���۷����� | 36.23% | 40.55% | 38.38% | 38.51% | 36.93% |
������Ʒ���Խ�����˾ԭ��ҩƷ���������ƹ㣬�ۺ�������λ���۷���Ͷ��������ʽ�δ�����۷�����Ԥ��Ϊ35%��
����������ҪΪ���ʸ��������⡢���÷ѡ��۾�̯���ȡ����ʸ�����������á����÷Ѱ����ϼ�Ŀǰ��ģ����ҩ���к�Ԥ�����ӵ�������Ա�����Լ�ÿ��
5%��������Ԥ�⣬�з����ð���Ŀǰ��˾��Ŀ�ƻ�����Ԥ�ⲻ���ʱ������з����á��۾�̯�����ð�����ҵ������߲��㡣
��6��������
���������ݼ�Ȩƽ���ʱ��ɱ���WACC������ȷ�������У�ծ���ʱ��ɱ�������ʱ��ƽ������ˮƽ��Ȩ��������ҵͬ��ҵ���й�˾ƽ��ծ�ɼ���ȡ�á���Ȩ�ʱ��ɱ�Ke�����ձ�����Ϊ��������ֿ������г�������ۡ���ҵ�ض����յ����ȷ���ϵ����������������������ȷ��˰ǰ������Ϊ17.88%��
�ġ����������ͻ��ʦ�˲����
��һ���˲����
�������������������������˻��ʦ��ȡ�ĺ˲鷽ʽ�����������ڣ�
1����̸�����˲���������Ա���˽������˶����չ��ʲ����������巽������������������Լ����չ��ʲ������ڼ�δ����Ӫ״��������������ֵ��������ȣ�
2�����������˶����չ���ض��»�ɶ���������ļ����չ�����ʲ������Ʊ��漰�������棻
3���˽�������ֵ��صĹؼ��ڲ����ƣ�����������Ӧ�ʲ������������������ֵ�����ļ������������ֵ������������ȣ�
4�����������˶�������ֵ������ж��Լ������������ʲ���Ļ��֣�����������ԣ�����������ȷ���ļ�ֵ���Է�����ģ�͵�ǡ���ԣ���������������������ֵ������ʹ�õ���ҪԤ��������ؼ����裬�˽�����Ԥ������ʵ��������Ƿ�����ش�ƫ�������䶯�������ԡ�
�������˲����
���˲飬�������������ʦ��Ϊ��
1�����ϼ���Ҫ�з�ҩƷ�Ľ�չ����Ԥ�ڡ��չ���ɺ�˾���п��ϼ�100%��Ȩ�����ڹ�˾���������ƽ�CM082��Ŀ���ٴ�������г���������Ͷ�ʷ��Ϲ�˾�ȶ��ķ�չս�ԣ����Ϲ�˾�г���ҵ��չ����Ҫ��
2���չ����ϼ��Ķ������ݳ�֣��չ����۾��й����Ժͺ����ԣ�
3���������ڣ�������������ֵ�������֡�������
���������7������ǰļ��Ŀ���������˲���˵������1���з������豸��������ҩ�з���Ŀ��ǰ��չ������Ƿ����Ԥ�ڣ��뱾��ļͶ��Ŀ�������Ƿ��ظ����裬����2023��12�´ﵽԤ����ʹ��״̬�ĺ����ԡ���2���³�������������Ŀ�ۼ�ʵ��Ч���12.2��Ԫ��Զ����˾ͬ�ھ�����ˮƽ��˵�����Ч�������̣������Ϣ��¶�Ƿ���ʵȷ��
�뱣�����������ʦ�����˲�������ظ���
һ���з������豸��������ҩ�з���Ŀ��ǰ��չ������Ƿ����Ԥ�ڣ��뱾��ļͶ��Ŀ�������Ƿ��ظ����裬����2023��12�´ﵽԤ����ʹ��״̬�ĺ�����
��һ���з������豸��������ҩ�з���Ŀ��ǰ��չ������Ƿ����Ԥ��
ԭ�з������豸��������ҩ�з���Ŀ����Ŀ������£�
| ��Ŀ���� | ��Ŀ Ͷ�ʽ�� ����Ԫ�� | ļ���ʽ� ��ŵͶ�ʶ� ����Ԫ�� |
| 1���з������豸��������ҩ�з���Ŀ | ||
| A����������������Ӧ֢�з���Ŀ | 15,463.00 | 24,000.00 |
| B��BPI-9016 �з���Ŀ | 4,170.00 | |
| C��BPI-3016 �з���Ŀ | 5,027.00 | |
| D��BPI-2009C �з���Ŀ | 3,346.00 | |
| E������ŵ���з���Ŀ[ע] | 1,005.00 | |
| �з������豸���� | 5,352.00 | |
| �ϼ� | 34,363.00 | 24,000.00 |
ע������ŵ��Ϊ��˾�����з��Ĺ���3�����ҩ����2013���걨�ٴ���2016�����ٴ�������������˾����Դ�������úͼ�ֵʵ����ĽǶȳ���������˾�ڶ��춭�»�ڶ�
ʮ���λ���͵ڶ�����»�ڶ�ʮ�λ�������ͨ������˾����ֹ����Ŀ����ļ���ʽ�Ͷ�롰���CM-082Ƭ�� 3000��Ƭ��X-396���� 600����������Ŀ�����ӿ���ҩ�IJ�ҵ�����̡�
������Ŀ��ǰ��չ���˵�����£�
��������������Ӧ֢�з���ĿĿǰ����ɣ����а�������һ������EGFRͻ�������NSCLC���ߵ���Ӧ֢����2014����ԭ����ʳƷҩƷ�ල�����ܾ������ӡ�
BPI-9016��Ŀ�з�ҩ��ϵc-Met���Ƽ������������ٴ��о����ݣ���Чδ��Ԥ��Ŀ�꣬��˾�ۺ������������ͣ���������c-Met�е㣬��˾��2019�������MCLA-129����һ��EGFR & c-Met˫�е��˫�����Կ��壩��һ���߿���ǰ������Ŀ��Ϊ��˾�ڷΰ����Ƶ�ȫ�渲���ṩ���Ż��IJ��֡�
BPI-3016��Ŀ�з�ҩ��ϵ��˾�����з������ͽ���ҩ BPI-3016�����ڵ���Ѫ��ˮƽ����������2017��3�£���˾��� BPI-3016��ע��Һ�ٴ�����������Ŀǰ����Ŀ�����ٴ���������Ρ�
BPI-2009C��ĿͶ���Ѵﵽ��ĿͶ�ʽ�Ŀǰ����Чδ��Ԥ��Ŀ�꣬��˾������ͣ���������ۺ�����ǰ�����ݺ�ȷ����һ��������
�з������豸������ĿͶ���Ѵ���ĿͶ�ʽ���˾�½��䱸��һϵ���Ƚ��������豸�����п��������õ���ǿ��
��������Ŀ��ͣ��������ֹ�⣬������Ŀ���ռƻ��ƽ�����������Ԥ�ڡ�
�������뱾��ļͶ��Ŀ�������Ƿ��ظ�����
����ļͶ��ҩ�з����з��豸������Ŀ�������£�
| ��� | Ͷ����� | Ͷ�ʽ���Ԫ�� | ��ʹ��ļ���ʽ���Ԫ�� |
| 1 | ��ҩ�з�Ͷ�� | 105,354.15 | 66,879.42 |
| 1.1 | X-396����ALK����NSCLC���������ٴ����� | 6,851.35 | 892.17 |
| 1.2 | X-396����ALK����NSCLCһ�������ٴ����� | 14,267.00 | 4,680.77 |
| 1.3 | CM082���������ٴ���/���� | 17,689.58 | 11,793.90 |
| ��� | Ͷ����� | Ͷ�ʽ���Ԫ�� | ��ʹ��ļ���ʽ���Ԫ�� |
| 1.4 | CM082����JS001����ճĤ��ɫ���������ٴ����� | 10,577.10 | 10,448.82 |
| 1.5 | MIL60����״ϸ����Сϸ���ΰ������ٴ����� | 23,613.77 | 10,758.12 |
| 1.6 | BPI-D0316����ʹ��EGFR���Ƽ���ҩ�����T790Mͻ���NSCLC�����ٴ����� | 17,646.10 | 13,853.81 |
| 1.7 | BPI-D0316����EGFR���Ե�NSCLCһ�������ٴ���/���� | 14,709.25 | 14,451.83 |
| 2 | �з��豸���� | 7,320.58 | 7,320.58 |
| �ϼ� | 112,674.73 | 74,200.00 | |
���ϱ�������ļͶ��Ŀ��ҩ�з�Ͷ������Ŀ��ǰ��ļͶ��ĿΪ��ͬ�з���Ŀ���������ظ����衣
���з��豸������Ŀ��Ҫ�ǻ��ڹ�˾Ŀǰ�з������������ơ���Ա���ϳ�ʵ���з���Ŀ�������з���Ŀ�ѶȲ��������Լ�����������з��ŶӺͿ�չ������з���Ŀ��������ǰ��ļͶ��ĿҲ�������ظ����������
����������2023��12�´ﵽԤ����ʹ��״̬�ĺ�����
����Ŀǰ�з������豸��������ҩ�з���Ŀ�Ľ�չ���������ͣ��������ֹ��Ŀ�⣬��������������Ӧ֢���з������豸��������ɣ�BPI-3016��Ŀ�д����ٴ���������Σ���˾�����ĿĿǰ��չ�������Ŀ�ﵽԤ����ʹ��״̬��ʱ��ȷ��Ϊ2023��12�£����ۺϿ�����ҩ�з����ڳ�������Ԥ�����ؽ϶��Լ���ҩ������ڽϳ���ʱ�䲻ȷ���Խ�ǿ������ȷ�������к����ԡ�
�����³�������������Ŀ�ۼ�ʵ��Ч���12.2��Ԫ��Զ����˾ͬ�ھ�����ˮƽ��˵�����Ч�������̣������Ϣ��¶�Ƿ���ʵȷ
�³�������������Ŀ�ɱ���˾��Ϊʵʩ����,��Ŀ������ɺ�˾���г��ؽ�������Ϊ��������Ƭ�����䣬ԭ�а�������Ƭ�����佫��Ǩ���³������ó������ܽ���Ŀǰ2,500��Ƭ������6,000��Ƭ����Ҫ����������������Ȱ�������ҩ�
�³�������������Ŀʵ��Ч�������㷽�����£�
1��Ӫҵ���룺�³�������������Ŀ���ɺ�ԭ�а�������Ƭ�����佫��Ǩ���³�������Ӫҵ�������������Ʒ�γɵ�������㣻�³�����2017��9�´ﵽԤ����ʹ��״̬��2017����Ŀ���밴�մﵽԤ����ʹ��״̬���³�������ռ�ȶԵ��ڰ�������Ӫҵ������з�̯���㡣
2��Ӫҵ�ɱ�������������Ŀ�����Ӧ�ijɱ����к��㡣
3���ڼ���á�˰���ӡ�����˰������ǰ��ļͶ��Ŀ��Ʒ����������ռ����ĸ��˾Ӫҵ����ı����������̯�ʲ�����Ӧ��̯���ڼ���á�˰���ӡ�����˰������������ǰ��ļͶ��Ŀ�ص��ڼ���ý�������
��������������£�
��λ����Ԫ
| ��Ŀ | 2019��1-9�� | 2018�� | 2017�� |
| ���� | 121,664.10 | 120,844.26 | 42,458.04 |
| �ɱ� | 6,278.16 | 5,711.59 | 1,808.58 |
| � | 115,385.93 | 115,132.67 | 40,649.46 |
| ˰���� | 784.10 | 1,279.29 | 861.27 |
| �ڼ���õ� | 57,549.85 | 61,065.23 | 19,409.97 |
| ����˰���� | 3,677.63 | 2,412.88 | 1,806.85 |
| ��ĿЧ�� | 53,374.35 | 50,375.27 | 18,571.38 |
��˾��ĿЧ��Զ����˾ͬ�ھ�����ˮƽ����Ҫϵ��˾�з�Ͷ��ϴ�2017��ȡ�2018��Ⱥ�2019��1-9�£���˾�з�����֧���ֱ�Ϊ20,273.01��Ԫ��30,369.58��Ԫ��24,470.03��Ԫ�������з�����֧������ĿЧ���أ��ʼ���Ч��ʱ�����з����á�ͬʱ��Ч�����ʱ�����������³�������������ĿЧ���ص�����ͷ�����ʧ�ȣ����ӹ�˾��������֧����������á��ʲ���ֵ��ʧ�ȡ�
���ϣ���˾Ч��������ݼ�������ʵȷ���ۼ�ʵ��Ч���12.23��Ԫ��Զ����˾ͬ�ھ�����ˮƽ����Ҫϵ���Ч�����������ļͶ��Ŀ�ص�����ͷ�����ʧ��
�������������ͻ��ʦ�˲����
��һ���˲����
�������������������������˻��ʦ��ȡ�ĺ˲鷽ʽ�����������ڣ�
1������ǰļ��Ŀ��չ�����������ϣ��˽���Ŀ�Ľ����Ƿ��Ԥ��ƥ�䣬��ʵ��Ŀ�ﵽԤ����ʹ��״̬ʱ��ĺ����ԣ�
2�����Ĺ�˾����ļͶ��Ŀ���ϣ���ǰļ��Ŀ�ȶԣ���ʵ�Ƿ�����ظ��������Σ�
3����̸�������ˣ��˽�ǰļЧ�������̣�����Ч�����������¸��ˡ�
�������˲����
���˲飬�������������ʦ��Ϊ��
1���������з���Ŀ��˾�����Ŀ��Ч����ҵ��Ӫʵ���������������Ŀ��ͣ����ֹ�⣬������Ŀ�����ռƻ��ƽ�����������Ԥ�ڡ�ͬʱ����˾�����Ŀ���ȼ���ҩ�з��ص㣬����Ŀ�ﵽԼ����ʹ��״̬ʱ�������2023��12�¾��к����ԣ�
2��ǰļ��ҩ�з���Ŀ�뱾��ļͶ��ҩ�з���Ŀϵ��ͬ�з���Ŀ���������ظ��������Σ�
3���³�������������ĿЧ����㼰��Ϣ��¶��ʵȷ��
���������8��
�������ڹ�˾Ӫҵ������������ƣ����۷Ǿ����������»����������˲���˵������1�������ҵ���ߡ���Ʒ�۸ɱ��䶯���ڼ���ò��������˵����˾���������»���ԭ�����ԡ���2��2019��ҵ��ʵ�������ҵ���»������Ƿ������Ĺۣ�ԭ�����ԡ���3�������˹���2020��һ����ҵ����������ԭ��Ϊ�������������ͨϵͳ�İ�ȫ���������˵����˾�������ھ���ҵ���ռ�ȡ��������ھ����̱䶯������ն�����ʵ���������������߰�ȫ�����
��ԭ��Ϲ�˾�������ߡ�����ȷ�����ߵȣ�˵���Ƿ����ͨ��������ѹ������ҵ�����������4���¹�����Թ�˾��Ӫ��Ӱ��������뱣�����������ʦ�����˲���������Ծ���ҵ��������ʵȷ�Է����˲�������ظ���
һ�������ҵ���ߡ���Ʒ�۸ɱ��䶯���ڼ���ò��������˵����˾���������»���ԭ������
��һ����˾��Ӫҵ���������
2016����2019�꣬��˾��Ӫҵ�����䶯������±���ʾ�����±���֪��2016����2018�깫˾Ӫҵ������������ƣ����۷ǹ�ĸ������ͬ���»���2019�깫˾ҵ���������ơ�
��λ����Ԫ
| ��Ŀ | 2019��� | 2018��� | 2017��� | 2016��� | |||
| ��� | ͬ�ȱ䶯���� | ��� | ͬ�ȱ䶯���� | ��� | ͬ�ȱ䶯���� | ��� | |
| Ӫҵ���� | 155,392.43 | 26.94% | 122,417.18 | 19.27% | 102,635.87 | -0.84% | 103,506.09 |
| Ӫҵ�ɱ� | 10,522.75 | 52.53% | 6,898.92 | 57.86% | 4,370.33 | 33.12% | 3,282.93 |
| � | 144,869.68 | 25.41% | 115,518.26 | 17.56% | 98,265.54 | -1.95% | 100,223.16 |
| ë���� | 93.23% | ����1.14���ٷֵ� | 94.36% | ����1.38���ٷֵ� | 95.74% | ����1.09���ٷֵ� | 96.83% |
| ���۷��� | 56,298.85 | 13.43% | 49,635.17 | 26.01% | 39,388.73 | -1.18% | 39,857.55 |
| ��������[ע] | 25,694.35 | 47.09% | 17,468.01 | 32.17% | 13,216.12 | 125.01% | 5,873.70 |
| ����� | 32,636.34 | 7.46% | 30,369.58 | 49.80% | 20,273.01 | 25.53% | 16,150.31 |
| ������� | 4,431.22 | 224.60% | 1,365.14 | 276.20% | 362.88 | 417.51% | 70.12 |
| �ڼ���� | 119,060.76 | 20.46% | 98,837.90 | 34.95% | 73,240.74 | 18.22% | 61,951.68 |
| �ڼ������ | 76.62% | ����4.12���ٷֵ� | 80.74% | ����9.38���ٷֵ� | 71.36% | ����11.51���ٷֵ� | 59.85% |
| �۳��Ǿ��������澻���Ĺ�����ĸ��˾�����ߵľ����� | 20,831.66 | 50.13% | 13,875.59 | -30.74% | 20,035.34 | -34.30% | 30,495.32 |
ע��Ϊ��2018���Ժ����ݿھ�����һ�£�2016�ꡢ2017����з������Ѵӹ�������������
������2017��۷Ǿ������½�����
��˾2017��۷ǹ�ĸ�������2016���½�34.30%����Ҫϵ��˾��Ҫ��Ʒ�������������ۣ���Ʒë���½���ͬʱ�������á��з��������ӵ����ڼ�����������¡�
1����Ҫ��Ʒ�������ή�ۣ���˾��Ʒë���½�
| ��� | ��Ʒ | �����������У� | �������루��Ԫ�� | ���۳ɱ�����Ԫ�� | ƽ����λ�ۼۣ�Ԫ/�У� | ƽ����λ�ɱ���Ԫ/�У� | ��λë����Ԫ/�У� | ë���� |
| 2017�� | �������� | 803,225 | 102,597.18 | 4,370.33 | 1,277.32 | 54.41 | 1,222.91 | 95.74% |
| 2016�� | �������� | 562,205 | 103,483.20 | 3,282.93 | 1,840.67 | 58.39 | 1,782.27 | 96.83% |
| ��Ŀ | 2017��� | 2016��� | |
| ��� | �䶯�� | ��� | |
| ƽ����λ�ۼۣ�Ԫ/�У� | 1,277.32 | -30.61% | 1,840.67 |
| ƽ����λ�ɱ���Ԫ/�У� | 54.41 | -6.82% | 58.39 |
��˾2017�갣������ë���ʽ�2016�����1.09���ٷֵ㣬���У���Ʒƽ����λ�ۼۼ���30.61%����Ʒƽ����λ�ɱ�����6.82%����Ʒƽ����λ�ۼ��½����ȴ��ڲ�Ʒƽ����λ�ɱ��½����ȡ�2017�갣������ƽ�����ۼ۸������2016����ֽϴ�����½�����Ҫϵ��˾����������������ҩƷ�۸�̸�У�2016��5�¼۸�̸�н��������̸�м�1,399Ԫ/�У���˰���������ﵽ54.58%��2016���ļ��ȿ�ʼ������½������������̸�м۸���й����ɹ���2017��2�°������ᱻ�����°����ҽ��Ŀ¼��
2���������á��з��������������ڼ��������
��˾2017���ڼ���ý�2016������11,289.06��Ԫ������18.22%����Ҫϵ�������ú��з������������¡����У�
��˾2017��������ý�2016������7,342.42��Ԫ������125.01%����Ҫϵ�����ʲ�̯�����۾����ӡ����������ʲ�̯������2,455.66��Ԫ���۾�����1,536.10��Ԫ��ְ��н������1,132.07��Ԫ��
��˾2017���з����ý�2016������4,122.70��Ԫ������25.53%����Ҫϵ�м����������2,997.85��Ԫ��2017�깫˾��ҩ�з������ӽ���չ������Ŀ�������ƽ��������ҩ�����ٴ�����Σ�ȫ�����4��С���ӺͶ���������Ŀ����Էΰ�����ҩ���������ȫ��IJ��֡�
������2018��۷Ǿ������½�����
��˾2018��۷ǹ�ĸ�������2017���½�30.74%����Ҫϵ��˾�з��������ӵ����ڼ���ü����������¡�
��һ���棬2018�깫˾��Ҫ��Ʒ��������ë���ʻ������ֲ��䣬�½�0.47���ٷֵ㣻�ۺ�ë�����½�1.38���ٷֵ㣬��Ҫϵ��ë���ʵ�����ҵ��ռ����ߣ���������ë�������¡�
1���з��������ӵ����ڼ���ü�������
��˾2018���ڼ���ý�2017������25,597.16��Ԫ������34.95%�����������ȴ���ë���������ȣ���Ҫϵ�з������������¡�
��˾2018���з����ý�2017������10,096.57��Ԫ������49.80%����Ҫϵ2018�깫˾��ҩ�з����������ƽ����м����������5,411.34��Ԫ����н֧������2,836.66��Ԫ����֤���������������շ�������1,261.90��Ԫ����˾�����ҩ�з���ͨ�������з���ս�Ժ�����ʵ��˾���з����ߣ����γ����ݶȵ��з����ߡ�2018�깫˾��ҩ�з�����ȡ��������ijɼ������5����Ʒ��IND�걨��1��NDA�걨��������ɼƻ�Ŀ�ꡣ
���⣬2018�깫˾���۷���Ҳ������������Ҫϵ��˾��������ھ�����ҽԺ�г��⣬������������߳���ҽԺ�г���չ���мƻ����ؿ�ҽԺ��ҩ�������¡�
2����Ҫ��Ʒ��������������ۣ�ë���������½�����ë���ʵ�����ҵ��ռ����ߣ��ۺ�ë���������½�
| ��� | ��Ʒ | �����������У� | �������루��Ԫ�� | ���۳ɱ�����Ԫ�� | ƽ����λ�ۼۣ�Ԫ/�У� | ƽ����λ�ɱ� ��Ԫ/�У� | ��λë����Ԫ/�У� | ë���� |
| 2018�� | �������� | 1,047,824 | 120,844.26 | 5,711.59 | 1,153.29 | 54.51 | 1,098.78 | 95.27% |
| 2017�� | �������� | 803,225 | 102,597.18 | 4,370.33 | 1,277.32 | 54.41 | 1,222.91 | 95.74% |
| 2018��� | 2017��� | ||
| ��� | �䶯�� | ��� | |
| ƽ����λ�ۼۣ�Ԫ/�У� | 1,153.29 | -9.71% | 1,277.32 |
| ƽ����λ�ɱ���Ԫ/�У� | 54.51 | 0.18% | 54.41 |
��1����Ҫ��Ʒ��������������ۣ�ë���������½�
2018����Ҫ��Ʒ���������ƽ����λ�ۼۼ���9.71%����Ʒƽ����λ�ɱ�����0.18%����������ë���ʻ������ֲ��䣬�½�0.47���ٷֵ㡣���У�ƽ����λ�ۼ��½���Ҫϵ����1����������½��ִ�У�2018���㽭ʡ������ʡ��̽��ۣ�
��2��2018��4�²��������IJ�ί���������ڿ���ҩƷ��ֵ˰���ߵ�֪ͨ������2018��6��1���ֿ���ҩ�����3%����˰��ʽ�걨��˰����˾��Ӧ���Һ��٣��ѽ�˰�ĺ����öɸ����ߣ���2018��7�½�������������۽���1,345.05Ԫ/�У�����3.86%��2018��10�£�����������Ϊ����������ҩ�����롶���һ���ҩ��Ŀ¼����
��2������ҵ������ռ����ߣ���������ë����
2018������ҵ���Ӫҵ����ռ�ȴ�2017���0.02%������2018���1.28%����Ҫϵ����ҵ���е��ƹ����ͷ�������ҵ���������¡�2018������ҵ���ë����Ϊ24.51%��Զ���ڰ�������ë���ʣ�һ���̶��ϵ���2018�깫˾�ۺ�ë���������½���
����2019��ҵ��ʵ�������ҵ���»������Ƿ������Ĺۣ�ԭ������
2019�깫˾ҵ���»����������Ĺۣ�2019��۷ǹ�ĸ������20,831.66��Ԫ��ͬ������50.13%��2019�깫˾ҵ���Ĺ���Ҫϵ��������۸�������������£��������ӡ�Ӫҵ��������������������£�
��λ����Ԫ
| ��Ŀ | 2019��� | 2018��� | �䶯��� | ͬ�ȱ䶯���� |
| Ӫҵ���� | 155,392.43 | 122,417.18 | 32,975.25 | 26.94% |
| Ӫҵ�ɱ� | 10,522.75 | 6,898.92 | 3,623.83 | 52.53% |
| � | 144,869.68 | 115,518.26 | 29,351.42 | 25.41% |
| ë���� | 93.23% | 94.36% | - | ����1.14���ٷֵ� |
| ���۷��� | 56,298.85 | 49,635.17 | 6,663.68 | 13.43% |
| �������� | 25,694.35 | 17,468.01 | 8,226.34 | 47.09% |
| ����� | 32,636.34 | 30,369.58 | 2,266.76 | 7.46% |
| ������� | 4,431.22 | 1,365.14 | 3,066.08 | 224.60% |
| �ڼ���� | 119,060.76 | 98,837.90 | 20,222.86 | 20.46% |
| �ڼ������ | 76.62% | 80.74% | - | ����4.12���ٷֵ� |
| �۳��Ǿ��������澻���Ĺ�����ĸ��˾�����ߵľ����� | 20,831.66 | 13,875.59 | 6,956.07 | 50.13% |
���ϱ���ʾ����˾2019���Ӫҵ���������ͬ������26.94%��ë��������ͬ������29,351.42��Ԫ������25.41%���ڼ���ý�����ͬ������20,222.86��Ԫ������20.46%���ڼ�����ʼ���4.12���ٷֵ㡣��˾��Ҫ��Ʒ����������������ľ���������£�
| ��Ŀ | 2019��� | 2018��� | �䶯��� | ͬ�ȱ䶯���� |
| ������������ | 1,277,093 | 1,047,824 | 229,269 | 21.88% |
| �������루��Ԫ�� | 150,182.45 | 120,844.26 | 29,338.19 | 24.28% |
| ���۳ɱ�����Ԫ�� | 7,839.53 | 5,711.59 | 2,127.94 | 37.26% |
| ë������Ԫ�� | 142,342.92 | 115,132.67 | 27,210.25 | 23.63% |
| ë���� | 94.78% | 95.27% | - | ����0.49���ٷֵ� |
| ƽ����λ�ۼۣ�Ԫ/�У� | 1,175.97 | 1,153.29 | 22.68 | 1.97% |
| ��Ŀ | 2019��� | 2018��� | �䶯��� | ͬ�ȱ䶯���� |
| ƽ����λ�ɱ���Ԫ/�У� | 61.39 | 54.51 | 6.88 | 12.62% |
2019�갣���������۳ɱ���ͬ������37.26%�����������ڳɱ�������С��2019��ɱ�ʵ�����Ӷ��Ϊ2,127.94��Ԫ��ƽ����λ�ɱ�������Ҫϵ��������Ӫҵ�ɱ����۾�ռ�������Ͽ졣�۾�ռ�������Ͽ���Ҫ����Ϊ�����ڽ�����ת�����¡�ͬʱ2019�갣������ƽ����λ�ۼۻ��������ȶ������ۼ���������ȫ�����ۺ����ﵽ127.71��У�ͬ������21.88%��������������29,338.19��Ԫ��ͬ������24.28%��ë������27,210.25��Ԫ��ͬ������23.63%��2019�갣���������ۼ���������Ҫԭ��ϵ��������ļ��Ŭ����ƾ��һϵ�е��ٴ����飬��˾Ϊ�ٴ�ҽ���ṩ�˳�ֵ���Է�Сϸ���ΰ���NSCLC��������Ч����ȫ�Ե�ѭ֤ҽѧ֤�ݣ���������IJ��컯���Ʋ��ϻ��ۣ��ڷ�Сϸ���ΰ���NSCLC������ҩ�г�Ӯ���˺ܺõĿڱ��������˹�������ҩ��Ʒ������ͬʱ������ҽ��ҩƷĿ¼�ĸ�������Լ�������һ���ҩ��Ŀ¼��������������۲����˻��������á����⣬2019�깫˾���������������ܣ��������������Ʒ���ƹ㡢������Դ����ǿĿ��ҽԺ�Ŀ����������Ż���������ϵ��
���������˹���2020��һ����ҵ����������ԭ��Ϊ�������������ͨϵͳ�İ�ȫ���������˵����˾�������ھ���ҵ���ռ�ȡ��������ھ����̱䶯������ն�����ʵ���������������߰�ȫ�������ԭ��Ϲ�˾�������ߡ�����ȷ�����ߵȣ�˵���Ƿ����ͨ��������ѹ������ҵ�������
��һ����˾�������ھ���ҵ���ռ�ȡ��������ھ����̱䶯������ն�����ʵ�����
��1����˾�������ڰ����������밴����������ʾ���£�
��λ����Ԫ
| �������� | 2019��� | 2018��� | 2017��� | |||
| ��� | ���� | ��� | ���� | ��� | ���� | |
| ������ | 107,005.52 | 71.25% | 101,792.55 | 84.23% | 102,597.18 | 100.00% |
| ҩ�� | 43,176.93 | 28.75% | 19,051.71 | 15.77% | - | - |
| �ϼ� | 150,182.45 | 100.00% | 120,844.26 | 100.00% | 102,597.18 | 100.00% |
�������ھ���ҵ������ռ�������½�����Ҫϵҩ���������۹�ģ�������£���˾��������ά��ԭ�о��������Ļ����ϣ�������ҵ���ߣ�Ϊ������Ʊ�ƶ�ԭ�о����������ij����������չҩ����������ȡ��һ���ij�Ч����������ҩ��������ͻ����������������������ӣ��ʾ���ҵ������ռ�������½���
��2���������ھ����������䶯������£�
| ��Ŀ | 2019��� | 2018��� | 2017��� |
| �������������ң� | 194 | 125 | 80 |
| �䶯������ң� | 69 | 45 | 61 |
�����ڹ�˾�����������������ӣ���Ҫϵ����Ʊ��Ӱ�죬��ԭ�������¾����̵�����һ�����������£�ͬʱ������������г������ҽ�����ߵ���أ��������³��������������С�
��3���������ն�����ʵ�����
������ǰ��ʮ��ͻ���������ɹ�����������£�
�����
| 2019��12��31��/2019��� | 2018��12��31��/2018��� | 2017��12��31��/2017��� | |
| �ɹ����� | 615,719.00 | 656,157.00 | 747,718.00 |
| �������� | 639,152.00 | 684,525.00 | 723,927.00 |
�������ڣ������̲ɹ��IJ�Ʒ����ʵ�����ն����ۣ������ڶڻ�ѹ�������
��������������߰�ȫ�������ԭ��
������һ������߰�ȫ�������ԭ��ϵ���¹�����Ӱ�죬���������������ڼ����ҽ�Ʊ��ϳ�̨��һϵ�з����ʩ�����ߣ�������ҽ�ƻ�����Բ���ʵ��������ӵ��δ�����ҩ�����Ӷ������˰��������ն���������
����֮�⣬�����ڼ䣬���ڽ�ͨ�������裬����ط������жϣ�Ϊ��֤������ҩ����˾�;�����ͨ��������ȷ��ҩƷ��Ӧ��������Ϊ�����г���Ӧ��������˰�ȫ�������
��������Ϲ�˾�������ߡ�����ȷ�����ߵȣ�˵���Ƿ����ͨ��������ѹ������ҵ�������
��˾����ģʽ���ֿ�Ϊ�������ֺ������ϳ������������ϸߵĿͻ���������������һ���������ڣ������ھ�������������30���45��Ϊ��������ȷ���������£�
�Կͻ����᷽ʽ������Ʒ�ģ���˾�����サ���ͻ�֮���������Ȩ�����������ʧ�ķ��ռ�ת�ƣ��������ݿͻ������ȷ�����롣
��ָ�����䷽ʽ������Ʒ�ģ���˾ȡ���ʵ������䵥�ݲ����ҷ���������֪ͨ����Ϊ���������ҷ���������������������Ȩ�����������ʧ�ķ��ռ�ת�ƣ��������ݷ���֪ͨȷ�����롣
�����������ߣ��ֿ�ģʽ�£���˾����ȷ�ϵ�ͬʱ��ȫ���յ���ػ�����ڲ��������������ߵĿͻ����������ھ�������������ȫ���ջأ�����������£�
��λ����Ԫ
| ��Ŀ | 2019��� | 2018��� | 2017��� |
| �������� | 107,005.52 | 101,792.55 | 102,597.18 |
| Ӧ���˿�-������ | 4,677.48 | 6,101.53 | 9,206.84 |
| �Ƿ������� | �� | �� | �� |
| �ں��տ��� | 4,677.48 | 6,101.53 | 9,206.84 |
������Ӧ���˿���ת�����£�
��λ����Ԫ����
| ��Ŀ | 2019��� | 2018��� | 2017��� |
| �ڳ�Ӧ���˿���� | 6,381.40 | 9,206.84 | 3,815.42 |
| ��ĩӦ���˿���� | 5,605.61 | 6,381.40 | 9,206.84 |
| Ӫҵ���� | 155,392.43 | 122,417.18 | 102,635.87 |
| Ӧ���˿���ת�� | 25.93 | 15.71 | 15.76 |
ע��Ӧ���˿���ת��=Ӫҵ����/�ڳ���ĩƽ��Ӧ���˿���
���о����̶�Ӧ��Ӧ���˿���ת�����£�
��λ����Ԫ����
| ��Ŀ | 2019��� | 2018��� | 2017��� |
| �ڳ�Ӧ���˿���� | 6,101.53 | 9,206.84 | 3,815.42 |
| ��ĩӦ���˿���� | 4,677.48 | 6,101.53 | 9,206.84 |
| Ӫҵ���� | 107,005.52 | 101,792.55 | 102,597.18 |
| Ӧ���˿���ת�� | 19.85 | 13.29 | 15.76 |
���ϱ��������������ھ�����Ӧ���˿���ת�ʽϸߣ���Ϊ�ֿ����ۣ��ؿ���������������ڣ������ڳ������ڻؿ������
�������ڣ���˾���ۻ�����Ѱ���ȫ���ջأ�����ǰ��ʮ�����̱����ڿ��������£�
��λ����Ԫ����
| ��Ŀ | 2019��� | 2018��� | 2017��� |
| ǰ��ʮ�����۽�� | 72,814.37 | 57,807.47 | 93,286.50 |
| �������� | 107,005.52 | 101,792.55 | 102,597.18 |
| ռ����������� | 68.05% | 56.79% | 90.93% |
| �������� | 639,152.00 | 684,525.00 | 723,927.00 |
| ������� | 7,883.00 | 31,315.00 | 59,449.00 |
| ���ռ�� | 1.23% | 4.57% | 8.21% |
���ϱ���ǰ��ʮ�����̽�������ĩ���������С�����ռ�Ƚϵͣ������ڶڻ������
���ϣ���˾���������ֿ�Ϊ�����ҹ�˾�˿����ˮƽ�ϸߣ����������ö�ȵľ����̣����ڽ϶̣�Ӧ���˿���ת�ʽϸߡ����⣬�����̶ڻ���Ҫ�ϸߵ��ʽ�ɱ���������ʾ�������ڸ������̿��ˮƽ�ϵͣ�2020��һ������߿��ϵӦ���¹ڷ���Ӱ�����ȡ����ʱ��ʩ���ʲ�����ͨ��������ѹ������ҵ���������
�ġ��¹�����Թ�˾��Ӫ��Ӱ�����
��˾���ຼ����һ����������ҵ��2020��2��14�պ�������������Ŀǰ������Ӫ��������˾��Ʒ������ΰ����˵��β��ճ����裬��ֱ�ӹ�ϵ���˵���������������ͨ����Ϊ�����Ŀڷ���ɡ����¹�����Ӱ�죬���ڽ�ͨ�������裬����ط������жϣ�Ϊ��֤������ҩ����˾�;�����ͨ��������ȷ��ҩƷ��Ӧ����
����Ϊ�����г���Ӧ��2020��һ���Ⱥ���������˰�ȫ�������Ŀǰ����˾�����������������������������̱������㣬���������ն�����ʹ������
�塢���������ͻ��ʦ�˲����
��һ���˲����
�������������������ͻ��ʦ��ȡ�ĺ˲鷽ʽ�����������ڣ�
1����̸�˹�˾�������˼����۸����ˣ��˽��˹�˾���������
2��������ҽҩ��ҵ������߷��漰�о����棻
3����������Ҫ�����̽����������
4�������˹�˾��2016����ȱ��桷����2017����ȱ��桷����2018����ȱ��桷����2019����ȱ��桷����2020���һ���ȱ��桷�������ڶ�����֤ȯ��������ѯ���ظ��Ĺ��桷�������ţ�2020-041����
5���Թ�˾��Ҫ�ͻ������۶����ĩӦ���˿������к�֤���Է������غ��Ĺ��̽�������Ч�Ŀ��ƣ���δ�غ��Ŀͻ�ִ���˲�����صĺ�ͬ����Ʊ��ǩ�յ��Լ��ں��տ������Բ��Գ�����ȷ���������ʵ�Լ������ԣ�
6�������������ص�ԭʼ���ݣ��������ۺ�ͬ����Ʊ�����ⵥ��ǩ�յ�������������������ʵ�Լ����ۼ�¼��ȷ�ԣ�
7���Գ�����ʽ���Ƚ���ĩǰ����ض����ۼ�¼��������ⵥ��ǩ�յ������ۺ�ͬƥ��֧�������ϣ������������Ƿ�������Ӧ���ۺ�ͬ�е�����ȷ����ǡ���Ļ���ڼ��ڡ�
�������˲����
���˲飬�������������ʦ��Ϊ��
1��2016����2018�꣬�����˾�Ӫҵ���»���Ҫϵ��˾�������ҩƷ�۸�̸�У����������ۼ��½���ͬʱ��˾�з����ó������ӵ����ڼ�����������£�
2��2019��������ҵ���»����������Ĺۣ���Ҫϵ��������۸�������������£��������ӡ�Ӫҵ�����������£����к����ԣ�
3��������2020��һ���Ȳ�����ͨ��������ѹ������ҵ���������
4�����¹�����Ӱ�죬Ϊ��֤������ҩ��ȷ��ҩƷ��Ӧ��2020��һ���Ⱦ����̺���������˰�ȫ�������Ŀǰ�������˶����������������������������̱������㣬���������ն�����ʹ������
5���������ڣ���˾����ҵ��������ʵ��ȷ��
���������9��
2018������������Ͷ���Է��ز�5.05��Ԫ����ҪΪ������Ŀ�ִﵽԤ����ʹ��״̬����ת��Ͷ���Է��ز����������˲���˵��Ͷ��ϴ����ʽ��躣���ı�Ҫ�ԡ������ԣ�Ͷ���Է��ز��ľ��������ɺ�����Ͷ���Է��ز��ĺ����ԡ�
�뱣�����������˲������
�ظ���
һ��2018������������Ͷ���Է��ز�5.05��Ԫ����ҪΪ������Ŀ�ִﵽԤ����ʹ��״̬����ת��Ͷ���Է��ز����������˲���˵��Ͷ��ϴ����ʽ��躣���ı�Ҫ�ԡ�������
��һ����˾�ķ�չս��
�Գ�����������˾ʼ�ձ��С�Better medicine,Better life����ʹ����Ŭ�������Ϊ���ܲ����й��Ŀ����ҩ��ҵ���������з���ս�Ժ������г������ǹ�˾��չս�Ե�������������˾���ϼ�ǿ�������£�ǿ��Դͷ���º�ת���о�������Ʒ��Ӫ���ʱ���Ӫ���ϣ�Ŭ����չΪһ������ҩ�з�Ϊ���ľ��������Կ�����ҩΪ���IJ�Ʒ�ĸ�����ҩ��ҵ��
��������������ı�Ҫ�ԡ�������
������ĿϵΪ��Ϸ����˶�������ķ�չս�ԣ����ڱ����ι���������ҵ��
ҽ�ƽ�����ҵ�ر�����ҩ�з���ҵ����Ͷ��ʱ�䳤��Ͷ�ʽ���Ͷ�ʷ�����Խϸߵ��ص㡣�����ι���������ҵ��Ŀ�չ��ϵ�����˳�ֿ���ҽ�ƽ�����ҵ���ص㣬���ñ����ι���������ҵ����ؿ���˾ս�Ժ���������ȡ��Ʒ���ߵ�DZ���ƶ����á�����ص�����������������⣬Ŀǰ����������Ҫ��פ����ҵ������Ϊ��������ࡢ���\���ࡢҽҩҽ�����Լ�ҽ����Ϣ�����ռ�ѳ������Լ60%����˺�����Ŀ������б�Ҫ�Ժͺ����ԡ�
����Ͷ���Է��ز��ľ��������ɺ�����Ͷ���Է��ز��ĺ�����
��һ��Ͷ���Է��ز��ľ�������
����2019��12��31�գ���˾Ͷ���Է��ز������ֵΪ57,481.50��Ԫ����˾�ѳ������70,356.68ƽ���ף�2019�깫˾�������Ϊ3,460.97��Ԫ��ռ����Ӫҵ���������Ϊ2.23%��ռ�Ƚ�С��Ŀǰ������ҵ��ҪΪ��������ࡢ���\���ࡢҽҩ�����ࡢҽ�ƽ������Լ�ҽ����Ϣ������ҵ������������£�
1�����·����������·�������ⲿ�֣�ĸ��˾Ͷ���Է��ز���
���·����������·�������ܲ�����δʹ�ó��������к��·���������10,871.99ƽ���ף�����2019�����ȫ�����⣬������100%������·���������82,636.71ƽ���ף�����2019����ѳ���12,557.1ƽ���ף�������15.20%��2019��������빲��465.95��Ԫ��
2��������Ŀ
�㽭����ҽҩ�Ƽ�����˾ӵ�е������ں������ຼ���峣�ֵ�������188�ŵĺ�����Ŀ�����65,749.29ƽ���ף�����2019����ѳ���46,927.59ƽ���ף�������71.37%��2019���������2,995.02��Ԫ��
������ĸ��˾��������Ͷ���Է��ز��ĺ�����
���·����Ϊ��˾���ϳ�����Ϊ��˾����ǰ�ܲ��칫���Ƽ�������ԭ�Ϻϳɡ���ҩ�з��ij��������ڹ�˾��Ʒ����������������������ҩ��Ʒ�������࣬���·�������Ƽ���ԭ��ҩ����������ԶԶ��������ʵ�������ǵ����·��
��ռ�ؽ�40Ķ�Լ���Ӧ�Ļ��������������ܽ��м�������������ܵĿռ�dz����ޡ�
Ϊ�˱�֤��˾������Ӫ����˾��ĸ��˾Ϊʵʩ���壬��������·������Ϊ��˾�ܲ��칫���Ƽ���������ҩ�з��ij�������������·������Ϊ��˾�ĺϳɻ��أ�����ԭ��ҩ�ĺϳɡ�����2019��12��31�գ���˾��������·�����½��˳����������÷������������ʩ����Ͷ����Ӫ������·������δ��ȫͶ����Ӫ��ͨ����������·����������·��������˾�������������������2,500��Ƭ������6,000��Ƭ��������δ��������г�����
ҩƷ��������������Ҫ��ߣ����辭ҩ������պ�GMP��֤��Ͷ�������⣬ҩ�����������Ľ�������һ��ϳ����粻��ǰ���в��ܹ滮��һ���²�Ʒ�з��ɹ���û����صij�������˾��δ�����г������н����ڷdz������ĵ�λ�����Ϊ�˱�֤��������δ��������ģ�ij�������Ϊδ��5-10���ڵ��²�Ʒ��ر����ռ��Ա�ȷ���²�Ʒ�з��ɹ���Ͷ����������˾���������·����ռ�ؽ�147Ķ���������82,636.71ƽ���ס�
���ں��·���������ʱ����磬������ʩ��Ϊ�¾ɣ���������Ҳ��Ϊ��һ������·������Ŀ����Ͷ����Ӫ��˾��Ҫ�������Ƽ����������Ǩ������·����������·�������ֽ��ɺ�������ԭ�Ϻϳɰ�Ǩ������·���������·������δ������������Ϊ��˾��Ӫ�����IJ��䡣��˾��������·�����ͺ��·����Ŀǰ��δʹ�õij������г��⣬Ϊ��˾����һ����������룬�ڱ������γ�Ͷ���Է��ز���δ�����Ź�˾��Ʒ���������ӡ������ߵ������Լ��з����ŵ��������ٳ��������Ŀǰ���ⷽΪ��������ࡢҩƷ�з��ࡢ���\���ࡢҽ����Ϣ������ҵ�����Ϲ�˾�Ķ������ս�Է���
���������δʹ�õij������г�����к����ԡ�
������������Ŀ����Ͷ���Է��ز��ĺ�����
ҽ�ƽ�����ҵ�ر�����ҩ�з���ҵ����Ͷ��ʱ�䳤��Ͷ�ʽ���Ͷ�ʷ�����Խϸߵ��ص㡣�����ι���������ҵ��Ŀ�չ��ϵ�����˳�ֿ���ҽ�ƽ�����ҵ���ص㣬���ñ����ι���������ҵ����ؿ���˾ս�Ժ���������ȡ��Ʒ���ߵ�DZ���ƶ����á�����ص�����������������⣬Ŀǰ����������Ҫ��פ����ҵ
������Ϊ��������ࡢ���\���ࡢҽҩҽ�����Լ�ҽ����Ϣ�����ռ�ѳ������Լ60%�����ϣ�������ĿĿǰϵΪ��Ϸ����˷�չս�ԣ����ڱ����ι���������ҵ������Ͷ���Է��ز����к����ԡ�Ϊ�ӿ��ʽ�������Ӵ�֧�ֹ�˾����ҩ�з�ҵ�������⽫����е��㽭����ҽҩ�Ƽ�����˾100%�Ĺ�Ȩ��������������Ŀ����25,146.35��Ԫת�ø�ʵ�ʿ����˶�����ȫ�ʿعɵ������������¿Ƽ�����˾��
������Ȩת�õı�Ĺ�Ȩ�Ѿ������ʲ���������˾���������ߡ����������֣�2020������0639�š�������ҩҵ�ɷ�����˾���Ȩת���漰���㽭����ҽҩ�Ƽ�����˾�ɶ�ȫ��Ȩ���ֵ������Ŀ�ʲ��������桷�����¼�ơ����ʲ��������桷���������ݡ��ʲ��������桷��������������2020��3��31�գ��㽭����ҽҩ�Ƽ�����˾100%��Ȩ�����ʲ�������ȷ����������ֵΪ25,146.35��Ԫ��������Ȩת�õļ۸�ϵ�ɽ���˫������ǰ�������������ƽ�ȡ���Ը����ƽ�Ļ�����Э��һ��ȷ��������������2020��6��12���ٿ������춭�»���ߴλ��飬����ͨ�������ڳ��۱���ҽҩ�Ƽ�100%��Ȩ�߹��������鰸�����������������¿Ƽ�����˾ǩ����Ч�����ġ������㽭����ҽҩ�Ƽ�����˾��Ȩת��Э�顷�����������Ѿͱ��ν���������ǰ�Ͽ�����ȷͬ��Ķ�����������ν��������ύ�����˹ɶ�������顣
�ġ����������˲����
��һ���˲����
��������������������ȡ�ĺ˲鷽ʽ�����������ڣ�
1����������˶������ĺ�����Ŀ�����·����������·�����������ء������ij��ú�ͬ����������Ȩ֤�顢������Ȩ֤�顢�����˵����춭�»���ߴλ�����顢�������㽭����ҽҩ�Ƽ�����˾��Ȩת��Э�顷�Լ����ʲ��������桷���Է����ˡ��㽭����ҽҩ�Ƽ�����˾�Լ������˿��Ƶ������ӹ�˾�Ƿ���ڷ��ز��������ʽ����˺˲飻
2�����ĺͷ����˷�����Ͷ���Է��ز��Ķ�����������������Ŀ�뱴���ι���������ҵ���ս�Է�չ�ļ�������Ժ�����Ŀ�뱴���ι���������ҵ��Ĺ滮�����̸�˷�������ظ����ˡ�
3�������˹�˾��ս�Է�չ�滮���ܾ�������������ļ���
�������˲����
���˲飬����������Ϊ��
1���㽭����ҽҩ�Ƽ�����˾�����ĺ�����Ŀ������Ϊ�ù�˾�Գ֣�Ŀǰ���ڱ����ι���������ҵ�������ָ���ۼƻ���
2����������������ظ��������֮�գ������˼���ع��ӹ�˾������⳧���ͺ�����Ŀ����Ϊ�����������ء������Ĺ滮��;����ط��ɷ��桢�������ļ��Ĺ涨��
3����������������ظ��������֮�գ������˼���ع��ӹ�˾�����߱����ز��������ʣ������ڷ��ز�������ҵ��������Ŀ���ڱ����ι���������ҵ��ϵΪ��Ϸ����˵ķ�չս�ԣ����·����������·�������ⲿ��ϵ�Է�������δʹ�ó����ĺ���ʹ�ã������˲����ڷ��ز�����ҵ��
���������10��
�������˲���˵�������η��ж��»������ǰ����������˾ʵʩ����ʵʩ�IJ�����Ͷ�ʼ������ҵ��ľ����������˾���һ��ĩ�Ƿ���н��ϴ����ϳ��IJ�����Ͷ�ʣ����������ҵ�����Σ��Ա�Ŀǰ������Ͷ���ܶ��뱾��ļ���ʽ��ģ��˾���ʲ�ˮƽ˵������ļ���ʽ����ı�Ҫ�ԡ�
�뱣������������������˲��������˵����˾�Ƿ���ڱ�������ļ���ʽ�Ͷ������ڼ�����ҵ������Ρ�
�ظ���
һ�����η��ж��»������ǰ����������˾ʵʩ����ʵʩ�IJ�����Ͷ
�ʼ������ҵ��ľ������
��һ���йز�����Ͷ�ʼ������ҵ����϶�����
1��������Ͷ�ʵ��϶�����
�����й�֤���2016��3��4�շ����ġ��������й�˾���ָ����2�š��йز�����Ͷ���϶����ʴ𡷣�������Ͷ�ʳ����ָ��������ȷ�ij��н����Խ����ʲ��Ϳɹ����۽����ʲ����������˿��ί�����Ƶ������⣬�������й�˾Ͷ���ڲ�ҵ�����������ƻ�����Ʒ�ģ�ͬʱ�����������εģ�Ӧ�϶�Ϊ������Ͷ�ʣ���1�����й�˾Ϊ���ϻ��˻���Ͷ���������������ϻ��ˣ������иû��𣨲�Ʒ����ʵ�ʹ���Ȩ�����Ȩ����2�����й�˾�Ի�ȡ�û��𣨲�Ʒ������Ͷ����Ŀ��Ͷ������Ϊ��ҪĿ�ġ������й�֤�����2020��2�·����ġ����м���ʴ𡪹��������淶���й�˾������Ϊ�ļ��Ҫ�����棩�������й�˾����������ʱ������������ҵ�⣬ԭ�������һ��ĩ���ô��ڳ��н��ϴ����ϳ��Ľ����Խ����ʲ��Ϳɹ����۵Ľ����ʲ����������˿��ί�����ƵȲ�����Ͷ�ʵ����Ρ�
�����й�֤�����2020��6�·����ġ�������ҵ���������������棩����������Ͷ�ʵ����Ͱ����������ڣ�����ڣ�Ͷ�ʲ�ҵ���𡢲������𣻲���ʽ�ί�д���Գ������ųֹɱ������Ų���˾���ʻ����ʣ��������沨�����ҷ��սϸߵĽ��ڲ�Ʒ���ǽ�����ҵͶ�ʽ���ҵ��ȡ�������Χ�Ʋ�ҵ���������Ի�ȡ������ԭ�ϻ�����ΪĿ�ĵIJ�ҵͶ�ʣ����չ�������ΪĿ�ĵIJ���Ͷ�ʣ�����չ�ͻ�������ΪĿ�ĵ�ί�д������Ϲ�˾��Ӫҵ��ս�Է�չ�����綨Ϊ������Ͷ�ʡ�
2�������ҵ����϶�����
�����й�֤�����2020��6�·����ġ�������ҵ���������������棩���е���ؽ��ͣ���1�����������С�������ᡢ֤��������½���ҵ��ij��ƻ���Ϊ���ڻ����⣬�������½��ڻ�Ļ�����Ϊ����ڻ����������ҵ������������ڣ��������ޡ���ҵ������С��ҵ��ȡ���2�������˲��ý�ļ���ʽ�ֱ�ӻ�������������ҵ��������������ҵ�������ҵ�����롢����ռ
�Ⱦ�����30%���ҷ���������������ƽ���˹�����1�����η��ж��»������ǰ�����������η���ǰ��Ͷ�����Ͷ�������ҵ��Ľ��������ʡ����ȸ�����ʽ���ʽ�Ͷ�룩Ӧ�ӱ���ļ���ʽ��ܶ��п۳���2����˾��ŵ�ڱ���ļ���ʽ�ʹ�����ǰ��ļ���ʽ�λ36�����ڣ����������������ҵ����ʽ�Ͷ�루�������ʡ����ȸ�����ʽ���ʽ�Ͷ�룩����3���빫˾��Ӫҵ��չ������أ�����ҵ̬���衢��ҵ��չ��������ҵ���ߵ��������ޡ���ҵ��������Ӧ�����ڣ��ݲ���������ڼ���ھ���������Ӧ����������ޡ���ҵ�����Լ���Ӧ�����ڵľ��徭Ӫ���ݡ��������ӯ����Դ���Լ�����ҵ���빫˾��Ӫҵ�����Ҫ��Ʒ֮��Ĺ�ϵ����֤˵����ҵ���Ƿ������ڷ���ʵ�徭�ã��Ƿ�������ҵ��չ����������ҵ������
���������η��ж��»������ǰ����������˾ʵʩ����ʵʩ�IJ�����Ͷ�ʼ������ҵ��ľ������2020��3��3�գ���˾�ٿ������춭�»�����λ�������ͨ���˱��ηǹ������й�Ʊ������ˣ����¼�ơ����ζ��»���顱�����Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ���˾ʵʩ����ʵʩ������Ͷ�ʵľ���������£�
1�������Խ����ʲ�
�Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ���˾�����ڽ����Խ����ʲ�Ͷ�ʵ����Ρ�
2���ɹ����۽����ʲ�
��2019��1��1���𣬹�˾ִ���µĽ��ڹ������״�ִ���գ���ԭ����ɹ����۽����ʲ����Էǽ���Ŀ�ij��е�Ȩ���Թ�ȨͶ�ʣ�ָ��Ϊ�Թ��ʼ�ֵ��������䶯���������ۺ�����Ľ����ʲ����б�Ϊ����Ȩ�湤��Ͷ�ʡ�
�Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ�����Ȩ�湤��Ͷ��ϵͶ�ʺ��ݺ�˼����ҽҩ����˾����������������\������˾�ͺ��ݶ�������Ƽ�����˾����Ϊ��˾����ҵ�ڵ�ս����Ͷ�ʲ��֣������ڲ�����Ͷ�ʣ����ҹ�˾����������£�
| ��� | ��˾���� | ����ʱ�� | ע���ʱ� | �ֹɱ��� | ��Ҫҵ�� | ��Ҫ������Ӫ�� | |
| ֱ�� | ��� | ||||||
| 1 | ���ݺ�˼����ҽҩ����˾ | 2016-08-03 | 1,454.5455��Ԫ����� | 6.25% | - | ����������������ѯ:������Ʒ�����\����ҽ�Ƽ��� | ���� |
| 2 | ��������������\������˾ | 2002-07-11 | 2,883.8996��Ԫ����� | 3.85% | - | ���\����������ҩ���о�����,�ṩ����ת��,������ѯ | ���� |
| 3 | ���ݶ�������Ƽ�����˾ | 2012-12-31 | 4,725.8353��Ԫ����� | 1.33% | - | ����������������ѯ���������ɹ�ת��:���\����ҽҩ������ҽ������Լ������豸��ҽҩ�м��� | ���� |
3�����ڹ�ȨͶ��
�Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ���˾���ڹ�ȨͶ��Ϊ��Capio Biosciences��Inc.������Capio�����ѧ����˾����Ͷ�ʣ���Ͷ��Ϊ��˾��ս����Ͷ�ʣ������ڲ�����Ͷ�ʣ�����������±���
| ��˾���� | ����ʱ�� | ע���ʱ� /ʵ���ʱ� | �ֹɱ��� | ��Ҫҵ�� | ��Ҫ������Ӫ�� | |
| ֱ�� | ��� | |||||
| Capio Biosciences, Inc. | 2015-11-03 | 225����Ԫ | 20.17% | - | ���ѪҺ��ѭ������ϸ����circulating tumor cell, CTC���ļ�⼼�����о��������� | ���� |
4���������˿���
�Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ���˾�����ڽ������˿�������Ρ�
5��ί�д���
�Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ���˾������ί�д�������Ρ�
6��������
�Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ���˾������ί�����Ƶ����Ρ�
7����ҵ���������
�Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ���˾������ʵʩ����ʵʩ�IJ�ҵ�������������Ρ�
8�������ҵ��
�Ա��ζ��»������ǰ�����£�2019��9��3�գ�������������ظ������գ���˾������Ͷ�ʺ���Ͷ�������ҵ������Ρ�
�����������Ա��η�����ض��»������ǰ�������������ظ�����֮�գ���˾δʵʩ����ʵʩ������Ͷ�ʡ�
������˾���һ��ĩ�Ƿ���н��ϴ����ϳ��IJ�����Ͷ�ʣ����������ҵ������
����2019��12��31�գ���˾������Ͷ�ʣ����������ҵ����������£�
1�������Խ����ʲ�
����2019��12��31�գ���˾�����ڽ����Խ����ʲ�Ͷ�ʵ����Ρ�
2���ɹ����۽����ʲ�
��2019��1��1���𣬹�˾ִ���µĽ��ڹ������״�ִ���գ���ԭ����ɹ����۽����ʲ����Էǽ���Ŀ�ij��е�Ȩ���Թ�ȨͶ�ʣ�ָ��Ϊ�Թ��ʼ�ֵ��������䶯���������ۺ�����Ľ����ʲ����б�Ϊ����Ȩ�湤��Ͷ�ʡ�
����2019��12��31�գ�����Ȩ�湤��Ͷ��10,593.42��Ԫ��ռ������ĸ��˾�ɶ����ʲ���4.31%��ϵͶ�ʺ��ݺ�˼����ҽҩ����˾����������������\������˾�ͺ��ݶ�������Ƽ�����˾����Ϊ��˾����ҵ�ڵ�ս����Ͷ�ʲ��֣������ڲ�����Ͷ�ʣ����ҹ�˾����������£�
| ��� | ��˾���� | ����ʱ�� | ע���ʱ� | �ֹɱ��� | ��Ҫҵ�� | ��Ҫ������Ӫ�� | |
| ֱ�� | ��� | ||||||
| 1 | ���ݺ�˼����ҽҩ����˾ | 2016-08-03 | 1,454.5455��Ԫ����� | 6.25% | - | ����������������ѯ:������Ʒ�����\����ҽ�Ƽ��� | ���� |
| 2 | ��������������\������˾ | 2002-07-11 | 2,883.8996��Ԫ����� | 3.85% | - | ���\����������ҩ���о�����,�ṩ����ת��,������ѯ | ���� |
| 3 | ���ݶ�������Ƽ�����˾ | 2012-12-31 | 4,725.8353��Ԫ����� | 1.33% | - | ����������������ѯ���������ɹ�ת��:���\����ҽҩ������ҽ������Լ������豸��ҽҩ�м��� | ���� |
3�����ڹ�ȨͶ��
����2019��12��31�գ���˾���ڹ�ȨͶ��Ϊ��Capio Biosciences��Inc.������Capio�����ѧ����˾����Ͷ�ʣ������ֵΪ1,278.91��Ԫ��ռ������ĸ��˾�ɶ����ʲ���0.52%����Ͷ��Ϊ��˾��ս����Ͷ�ʣ������ڲ�����Ͷ�ʣ�����������±���
| ��˾���� | ����ʱ�� | ע���ʱ� /ʵ���ʱ� | �ֹɱ��� | ��Ҫҵ�� | ��Ҫ������Ӫ�� | |
| ֱ�� | ��� | |||||
| Capio Biosciences, Inc. | 2015-11-03 | 225����Ԫ | 20.17% | - | ���ѪҺ��ѭ������ϸ����circulating tumor cell, CTC���ļ�⼼�����о��������� | ���� |
4���������˿���
����2019��12��31�գ���˾�����ڽ������˿�������Ρ�
5��ί�д���
����2019��12��31�գ���˾������ί�д�������Ρ�
6��������
����2019��12��31�գ���˾������ί�����Ƶ����Ρ�
7����ҵ���������
����2019��12��31�գ���˾������ʵʩ����ʵʩ�IJ�ҵ�������������Ρ�
8�������ҵ��
����2019��12��31�գ���˾������Ͷ�ʺ���Ͷ�������ҵ������Ρ�
��������������2019��12��31�գ���˾�����ڳ��н��ϴ����ϳ��IJ�����Ͷ�ʣ����������ҵ�����Ρ�
�����Ա�Ŀǰ������Ͷ���ܶ��뱾��ļ���ʽ��ģ��˾���ʲ�ˮƽ˵������ļ���ʽ����ı�Ҫ��
����2019��12��31�գ�������ĸ��˾���ʲ�Ϊ246,053.98��Ԫ������ļ���ʽ��ģռ�����������40.72%����˾Ŀǰ��������ʽ��������ȷ��;��ʹ�ð��ţ��������õĻ����ʽ��ҹ�˾�����ڳ��н��ϴ����ϳ��IJ�����Ͷ�ʣ����������ҵ�����Ρ�
��������������ظ������գ���˾�з����߷ḻ��Ŀǰ����С����ҩ�Xʮ����ѽ����ٴ��о������в�Ʒ��ʮ�����Ҫ���Ƿΰ������������ٰ��ȶ���������������˾������ͨ��������ļ���ʽ𣬼Ӵ���ҩ�з�Ͷ�룬��ǿ��ҩ�з����֣��ӿ�������Ŀ�з����̣���ǿ��˾�ۺϾ������Ϳ�����������ʵ�ֹ�˾�Ȳ�������չ��Ϊ�ɶ��������õ�Ͷ�ʻر���ͨ�����й�Ʊ���䲿�������ʽ������ڻ��˾��Ӫ��չ�����ж������ʽ������ѹ����Ҳ�DZ��Ϲ�˾�ɳ�����չ��������Ͷ��������ı�Ҫѡ����ˣ�����ļ���ʽ���б�Ҫ�ԡ�
�ġ���˾�����ڱ�������ļ���ʽ�Ͷ������ڼ�����ҵ�������
���ݹ�˾��ļ���ʽ�����ƶȡ�������˾Ӧ�����շ��������ļ��г�ŵ��ļ���ʽ�Ͷ�ʼƻ�ʹ��ļ���ʽ�ļ���ʽ�Ͷ����Ŀ����Ϊ���н����Խ����ʲ��Ϳɹ����۵Ľ����ʲ����������ˡ�ί�����ƵȲ�����Ͷ�ʣ�����ֱ�ӻ����Ͷ�����������м�֤ȯΪ��Ҫҵ��Ĺ�˾����˾���ý�ļ���ʽ�������Ѻ��ί�д���
����������ı�ļ���ʽ���;��Ͷ�ʡ�������ļ���ʽ�λ��˾���ϸ�ִ�С�ļ���ʽ�����ƶȡ�����ļ���ʽ�ר�����ڱ���ļͶ��Ŀ�������������ļ���ʽ�Ͷ������ڼ�����ҵ����ˣ���˾�����ڱ�������ļ���ʽ�Ͷ������ڼ�����ҵ������Ρ�
�塢���������˲����
��һ���˲����
��������������������ȡ�ĺ˲鷽ʽ�����������ڣ�
1�������������˱������ڵ���Ʊ��桢���ڱ��桢����Ͷ��Э�顢�ո���ƾ֤�������ļ������ϣ�
2���������˸�������Ա�����˷�̸���˽���������δ��������Ͷ�ʵ���ؼƻ����ţ�
3���˲���������ļ���ʽ�ʹ�ð��������
�������˲����
���˲飬����������Ϊ��
1�����η��ж��»������ǰ����������˾������ʵʩ����ʵʩ�IJ�����Ͷ�ʼ������ҵ��������
2����˾���һ��ĩ�����ڳ��н��ϴ����ϳ��IJ�����Ͷ�ʣ����������ҵ�����Σ�
3���Ա�Ŀǰ������Ͷ���ܶ��뱾��ļ���ʽ��ģ��˾���ʲ�ˮƽ������ļ���ʽ������б�Ҫ�ԣ�
4�������˲����ڱ�������ļ���ʽ�Ͷ������ڼ�����ҵ������Ρ�
����ҳ�����ģ�Ϊ����ҩҵ�ɷ�����˾�ԡ�����ҩҵ�ɷ�����˾��ҵ��ǹ�������A�ɹ�Ʊ�����ļ��������֮�ظ����桷֮ǩ��ҳ��
����ҩҵ�ɷ�����˾
2020��6��16��
�����������³�����
�����������Ķ�����ҩҵ�ɷ�����˾���η�������ظ������ȫ�����ݣ��˽ⱨ���漰����ĺ˲���̡�����˾���ں˺ͷ��տ������̣�ȷ�ϱ���˾�������㾡��ԭ�����к˲����������ظ����治������ټ��ء����Գ��������ش���©�����������ļ�����ʵ�ԡ�ȷ�ԡ������ԡ���ʱ�Գе���Ӧ�������Ρ�
���³���____________________
���Ӿ�
����֤ȯ�ɷ�����˾
2020��6��16��
����ҳ�����ģ�Ϊ����֤ȯ�ɷ�����˾�ԡ�����ҩҵ�ɷ�����˾��ҵ��ǹ�������A�ɹ�Ʊ�����ļ��������֮�ظ����桷֮ǩ��ҳ��
| ���������ˣ� | |||||
| �� �� | �� �� |
����֤ȯ�ɷ�����˾
2020��6��16��