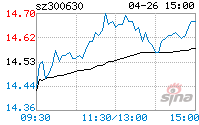
КЃФЯЦеРћжЦвЉЙЩЗнгаЯоЙЋЫОЙигкзЂЩфгУДяЭаУЙЫиЛёЕУгЂЙњвЉЦЗКЭНЁПЕВњЦЗЙмРэОж
ЃЈMHRAЃЉЩЯЪааэПЩЕФЙЋИц
БОЙЋЫОМАЖЪТЛсШЋЬхГЩдББЃжЄаХЯЂХћТЖЕФФкШнецЪЕЁЂзМШЗЁЂЭъећЃЌУЛгаащМйМЧдиЁЂЮѓЕМадГТЪіЛђжиДѓвХТЉЁЃ
КЃФЯЦеРћжЦвЉЙЩЗнгаЯоЙЋЫОЃЈвдЯТМђГЦЁАЦеРћжЦвЉЁБЛђЁАЙЋЫОЁБЃЉгкНќШеЪеЕНгЂЙњвЉЦЗКЭНЁПЕВњЦЗЙмРэОжЃЈMHRAЃЉЧЉЗЂЕФзЂЩфгУДяЭаУЙЫиЕФЩЯЪааэПЩЃЌЯжНЋЯрЙиЧщПіЙЋИцШчЯТЃК
вЛЁЂвЉЦЗЛљБОЧщПі
ЃЈвЛЃЉвЉЦЗУћГЦЃКзЂЩфгУДяЭаУЙЫи
ЃЈЖўЃЉЪЪгІжЂЃКГЩШЫКЭЖљЭЏЛМепЃЈ1 жС 17 ЫъЃЉЕФИДдгадЦЄЗєКЭЦЄЗєзщжЏИаШОЃЛГЩШЫЛМепгЩН№ЛЦЩЋЦЯЬбЧђОњв§Ц№ЕФгвВрИаШОадаФФкФЄбзЃЛГЩШЫМАЖљЭЏЛМепЃЈ1жС 17 ЫъЃЉЕФН№ЛЦЩЋЦЯЬбЧђОњбЊСїИаШОЃЈОњбЊжЂЃЉЁЃ
ЃЈШ§ЃЉМСаЭЃКзЂЩфМС
ЃЈЫФЃЉЙцИёЃК350 mgЃЛ500 mg
ЃЈЮхЃЉЩЯЪааэПЩГжгаШЫЃККЃФЯЦеРћжЦвЉЙЩЗнгаЯоЙЋЫО
ЖўЁЂвЉЦЗЕФЦфЫћЯрЙиЧщПі
ДяЭаУЙЫиЪЧгЩLillyЃЈРёРДЃЉЙЋЫОзюГѕбаОПЃЌCubistжЦвЉЙЋЫОПЊЗЂЕФЛЗжЌыФРрПЙЩњЫиЃЌ2003Фъ9дТ12ШеЃЌУРЙњЪГЦЗвЉЦЗМрЖНЙмРэОжОЙ§ПьЫйЩѓРэГЬађХњзМзЂЩфгУДяЭаУЙЫижЦМСЃЌЩЬЦЗУћЮЊCUBICINЃЌСйДВгУгкжЮСЦИДдгадЦЄЗєМАЦЄЗєзщжЏИаШОгыН№ЛЦЩЋЦЯЬбЧђОњв§Ц№ЕФОњбЊжЂЃЌФПЧАзЂЩфгУДяЭаУЙЫивбдкШЋЧђЙуЗКЩЯЪаЯњЪлЁЃ
ЦеРћжЦвЉЕФзЂЩфгУДяЭаУЙЫиГЩЙІбаЗЂКѓЃЌвбЯрМЬЬсНЛСЫУРЙњЁЂКЩРМЁЂгЂЙњЁЂАФДѓРћбЧКЭжаЙњЕШЖрИіЙњМвКЭЕиЧјЕФЗТжЦвЉЩЯЪаЩъЧыЃЌЪєгкЙВЯпЩњВњЦЗжжЁЃБОЦЗгк2022Фъ8дТЛёЕУУРЙњЪГЦЗвЉЦЗМрЖНЙмРэОжЕФХњзМЃЌ2022Фъ11дТЛёЕУКЩРМвЉЮяЦРМлЮЏдБЛсЕФХњзМЃЌ2022Фъ12дТЛёЕУжаЙњЙњМввЉЦЗМрЖНЙмРэОжЕФХњзМЃЌ2023Фъ1дТ
ЛёЕУАФДѓРћбЧвЉЮяЙмРэОжЕФХњзМЁЃНќШеЃЌЙЋЫОЪеЕНгЂЙњвЉЦЗКЭНЁПЕВњЦЗЙмРэОжЖдБОЦЗЕФЩЯЪааэПЩЃЌетБъжОзХЦеРћжЦвЉОпБИСЫдкгЂЙњЯњЪлзЂЩфгУДяЭаУЙЫиЕФзЪИёЃЌНЋЖдЙЋЫОЭиеЙгЂЙњЪаГЁДјРДЛ§МЋгАЯьЁЃ
Ш§ЁЂЗчЯеЬсЪО
ЙЋЫОИпЖШжиЪгвЉЦЗбаЗЂЁЂЩњВњКЭЯњЪлЁЃдкећИівЉЦЗЩњУќжмЦкЙмРэЙ§ГЬжаЃЌбЯИёзёЪиЙњФкЭтЪаГЁЯрЙиЕФвЉЦЗбаЗЂЁЂЩњВњКЭЯњЪлжЪСПЙмРэЙцЗЖЃЌШЗБЃвЉЦЗжЪСПКЭАВШЋЁЃгЩгквНвЉВњЦЗОпгаММЪѕИДдгЁЂИпЗчЯеЕФЬиЕуЃЌВњЦЗДгбажЦЁЂСйДВЪдбщБЈХњЕНЭЖВњЕФММЪѕИДдгЁЂжмЦкГЄЁЂЛЗНкЖрЃЌдквЉЦЗЛёЕУХњМўКѓЩњВњКЭЯњЪлвВШнвзЪмЕНеўВпКЭЪаГЁвЛаЉВЛШЗЖЈадвђЫиЕФгАЯьЁЃЙЋЫОНЋМАЪБИљОнКѓајНјеЙТФаааХЯЂХћТЖвхЮёЃЌОДЧыЙуДѓЭЖзЪепНїЩїОіВпЃЌзЂвтЗРЗЖЭЖзЪЗчЯеЁЃ
ЫФЁЂБИВщЮФМў
ЃЈвЛЃЉжЄУїЮФМў
ЬиДЫЙЋИцЁЃ
КЃФЯЦеРћжЦвЉЙЩЗнгаЯоЙЋЫОЖ ЪТ Лс2023Фъ7дТ10Ше