КЃФЯЦеРћжЦвЉЙЩЗнгаЯоЙЋЫОЙигкзЂЩфгУЗќСЂПЕпђЛёЕУЮкПЫРМЮРЩњВПЩЯЪааэПЩЕФЙЋИц
БОЙЋЫОМАЖЪТЛсШЋЬхГЩдББЃжЄаХЯЂХћТЖЕФФкШнецЪЕЁЂзМШЗЁЂЭъећЃЌУЛгаащМйМЧдиЁЂЮѓЕМадГТЪіЛђжиДѓвХТЉЁЃ
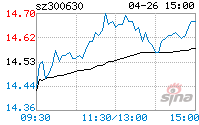
КЃФЯЦеРћжЦвЉЙЩЗнгаЯоЙЋЫОЃЈвдЯТМђГЦЁАЦеРћжЦвЉЁБЛђЁАЙЋЫОЁБЃЉгкНќШеЪеЕНСЫЮкПЫРМЮРЩњВПЧЉЗЂЕФзЂЩфгУЗќСЂПЕпђ200mgЕФЩЯЪааэПЩЃЌЯжНЋЯрЙиЧщПіЙЋИцШчЯТЃК
вЛЁЂвЉЦЗЛљБОЧщПі
ЃЈвЛЃЉвЉЮяУћГЦЃКзЂЩфгУЗќСЂПЕпђ
ЃЈЖўЃЉЪЪгІжЂЃКЗќСЂПЕпђЪЧвЛжжЙуЦзЕФШ§пђРрПЙецОњвЉЃЌжЮСЦЧжЯЎадЧњУЙВЁЃЌЗЧжаадСЃЯИАћМѕЩйЛМепжаЕФФюжщОњбЊжЂЃЌЖдЗњПЕпђФЭвЉЕФФюжщОњв§Ц№ЕФбЯжиЧжЯЎадИаШОЃЈАќРЈПЫШсФюжщОњЃЉЃЌгЩзуЗХЯпВЁОњЪєКЭСЕЖОњЪєв§Ц№ЕФбЯжиИаШОЃЌжївЊгУгкНјеЙадПЩФмЭўаВЩњУќЕФецОњИаШОЛМепЕФжЮСЦЃЌдЄЗРНгЪмвьЛљвђдьбЊИЩЯИАћвЦжВЃЈHSCTЃЉЕФИпЮЃЛМепжаЕФЧжЯЎадецОњИаШОЁЃ
ЃЈШ§ЃЉМСаЭЃКзЂЩфМС
ЃЈЫФЃЉЙцИёЃК200 mg
ЖўЁЂвЉЦЗЕФЦфЫћЯрЙиЧщПіМАКѓајНјеЙ
зЂЩфгУЗќСЂПЕпђгЩЛдШ№ЙЋЫОбаЗЂЃЌгк2002Фъ3дТЛёХЗжовЉЮяЙмРэОжЃЈEMAЃЉХњзМЩЯЪаЃЌ2002Фъ5дТЛёУРЙњЪГЦЗвЉЦЗМрЖНЙмРэОжЃЈFDAЃЉХњзМЩЯЪаЃЌ2004Фъ10дТЛёЙњМввЉЦЗМрЖНЙмРэОжХњзМЩЯЪаЃЌЩЬЦЗУћЮЊVFENDЃЈЭўЗВЃЉЁЃ
ЦеРћжЦвЉЕФзЂЩфгУЗќСЂПЕпђПЊЦєбаЗЂКѓЃЌЗжБ№ЕнНЛСЫУРЙњЁЂХЗУЫЁЂжаЙњЁЂАФДѓРћбЧЁЂаТЮїРМЁЂЮкПЫРМЕШЖрИіЙњМвКЭЕиЧјЕФЗТжЦвЉзЂВсЩъЧыЃЌЪєЙВЯпЩњВњВњЦЗЁЃБОЦЗвбгк2018Фъ11дТЛёЕУУРЙњFDAЕФХњзМВЂгк2019Фъ1дТЭЖЗХУРЙњЪаГЁСїЭЈЃЛгк2019Фъ3дТЛёЕУКЩРМвЉЮяЦРМлЮЏдБЛсЃЈCBGЃЉЕФЩЯЪааэПЩЃЛгк2019Фъ4дТЛёЕУЕТЙњСЊАювЉЮяКЭвНСЦЦїаЕЙмРэОжЃЈBfArMЃЉЕФЩЯЪааэПЩЃЛгк2021Фъ9дТЛёЕУАФДѓРћбЧвЉЮяЙмРэОжЃЈTGAЃЉЕФЩЯЪааэПЩЃЛгк2021Фъ11дТЛёЕУИчЫЙДяРшМгЮРЩњВПЕФ
ЩЯЪааэПЩЃЛгк2022Фъ2дТЛёЕУгЂЙњвЉМрЛњЙЙЃЈMHRAЃЉЧЉЗЂЕФЩЯЪааэПЩЃЛгк2022Фъ5дТЛёЕУжаЙњвЉЦЗМрЖНЙмРэОжЧЉЗЂЕФзЂВсХњМўЃЌЪгЭЌЭЈЙ§ЗТжЦвЉвЛжТадЦРМлЃЛ2022Фъ7дТЛёЕУаТЮїРМвЉЦЗЙмРэОжЕФЩЯЪааэПЩЁЃНќШеЃЌЙЋЫОЪеЕНЮкПЫРМЮРЩњВПЕФЩЯЪааэПЩЃЌБъжОзХЦеРћжЦвЉОпБИСЫдкЮкПЫРМЯњЪлзЂЩфгУЗќСЂПЕпђЕФзЪИёЃЌНЋЖдЙЋЫОЭиеЙЮкПЫРМЪаГЁДјРДЛ§МЋгАЯьЁЃ
Ш§ЁЂЗчЯеЬсЪО
ЙЋЫОИпЖШжиЪгвЉЦЗбаЗЂЃЌВЂбЯИёПижЦвЉЦЗбаЗЂЁЂжЦдьМАЯњЪлЛЗНкЕФжЪСПМААВШЋЁЃгЩгквНвЉВњЦЗОпгаИпПЦММЁЂИпЗчЯеЁЂИпИНМгжЕЕФЬиЕуЃЌВЛНівЉЦЗЕФЧАЦкбаЗЂвдМАВњЦЗДгбажЦЁЂСйДВЪдбщБЈХњЕНЭЖВњЕФжмЦкГЄЁЂЛЗНкЖрЃЌЖјЧввЉЦЗЛёЕУХњМўКѓЩњВњКЭЯњЪлвВШнвзЪмЕНвЛаЉВЛШЗЖЈадвђЫиЕФгАЯьЁЃЙЋЫОНЋМАЪБИљОнКѓајНјеЙТФаааХЯЂХћТЖвхЮёЃЌОДЧыЙуДѓЭЖзЪепНїЩїОіВпЃЌзЂвтЗРЗЖЭЖзЪЗчЯеЁЃ
ЫФЁЂБИВщЮФМў
ЃЈвЛЃЉжЄУїЮФМў
ЬиДЫЙЋИцЁЃ
КЃФЯЦеРћжЦвЉЙЩЗнгаЯоЙЋЫО
Ж ЪТ Лс2023Фъ6дТ5Ше