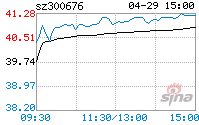
ЩюлкЛЊДѓЛљвђЙЩЗнгаЯоЙЋЫОЙигкШЋзЪзгЙЋЫОЩъБЈвНСЦЦїаЕзЂВсЛёЕУЪмРэЕФЙЋИц
БОЙЋЫОМАЖЪТЛсШЋЬхГЩдББЃжЄаХЯЂХћТЖЕФФкШнецЪЕЁЂзМШЗЁЂЭъећЃЌУЛгаащМйМЧдиЁЂЮѓЕМадГТЪіЛђжиДѓвХТЉЁЃ
вЛЁЂЧщПіИХЪі
ЩюлкЛЊДѓЛљвђЙЩЗнгаЯоЙЋЫОЃЈвдЯТМђГЦЁАЙЋЫОЁБЃЉШЋзЪзгЙЋЫОЛЊДѓЩњЮяПЦММЃЈЮфККЃЉгаЯоЙЋЫОЃЈвдЯТМђГЦЁАЮфККЩњЮяПЦММЁБЃЉНќШеЪеЕНЙњМввЉЦЗМрЖНЙмРэОжЃЈвдЯТМђГЦЁАЙњМввЉМрОжЁБЃЉЯТЗЂЕФЁЖЪмРэЭЈжЊЪщЁЗЃЌОпЬхЧщПіШчЯТЃК
| ађКХ | ВњЦЗУћГЦ | зЂВсЗжРр | дЄЦкСйДВгУЭО |
| 1 | вХДЋадЖњСћЛљвђМьВтЪдМСКаЃЈСЊКЯЬНеыУЊЖЈОлКЯВтађЗЈЃЉ | IIIРр | гУгкЬхЭтЖЈадМьВтИЩбЊЦЌбљБОжаШЫЛљвђзщDNAЕФ4ИівХДЋадЖњСћЛљвђЕФ20ИіЭЛБфЮЛЕуЃЌМьВтНсЙћЬсЙЉ20ИіЮЛЕуЕФЭЛБфРраЭЁЃ |
ЩЯЪіВњЦЗФПЧАЫљДІЕФЩѓХњНзЖЮЮЊЃКзЂВсЩъЧыЪмРэЃЌКѓајЫљашЕФЩѓХњСїГЬжївЊЮЊММЪѕЩѓЦРЁЂааеўЩѓХњЁЂжЦжЄЁЃ
ЖўЁЂЖдЙЋЫОЕФгАЯьМАЗчЯеЬсЪО
дЄЗРКЭМѕЩйГіЩњШБЯнЪЧЬсИпГіЩњШЫПкЫижЪЁЂЭЦНјНЁПЕжаЙњНЈЩшЕФживЊОйДыЁЃЙњМвЮРЩњНЁПЕЮЏдБЛсгк2018Фъ9дТЗЂВМЕФЁЖШЋЙњГіЩњШБЯнзлКЯЗРжЮЗНАИЁЗЃЈЙњЮРАьИОгзЗЂЁВ2018ЁГ19КХЃЉжажИГіЁАГіЩњШБЯнЗРжЮЗўЮёФмСІгыШКжкШевцдіГЄЕФгХЩњашЧѓШдгаНЯДѓВюОрЁБЃЌЖњСћЕШбЯжиГіЩњШБЯнЩаЮДЕУЕНгааЇПижЦЃЌашвЊНјвЛВНМгЧПЗРПиЁЃ
вХДЋвђЫиЪЧЕМжТЖњСћЕФжївЊдвђЃЌвХДЋадЖњСћЛљвђМьВтЪЧЯШЬьадЖњСћВЁвђеяЖЯЃЌдЄЗРГйЗЂадвЉЮяадЖњСћЕФживЊЗНЗЈЃЌЭЌЪБвВЪЧжИЕМПЦбЇЛщг§ЃЌНЕЕЭЖњСћГіЩњШБЯнЕФживЊЪжЖЮЃЌдкМВВЁЗРПиЁЂВЁвђеяЖЯвдМАЗчЯедЄВтЗНУцгаживЊЕФвтвхЁЃвХДЋадЖњСћЛљвђМьВтЪдМСКаЃЈСЊКЯЬНеыУЊЖЈОлКЯВтађЗЈЃЉЩъБЈвНСЦЦїаЕзЂВсЖдЙЋЫОЩњг§НЁПЕвЕЮёгаЛ§МЋгАЯьЁЃФПЧАИУЪдМСКаЕФЩѓХњНјГЬНіДІгкзЂВсЩъЧыЪмРэНзЖЮЃЌФП
ЧАЖдЙЋЫООгЊвЕМЈВЛЙЙГЩжБНггАЯьЁЃ
ИљОнЙњМвЯрЙизЂВсЗЈЙцЙцЖЈЃЌБОДЮЩъБЈзЂВсЛёЕУЪмРэКѓЃЌНЋгЩЙњМввЉМрОжвРЗЈНјааЦРЩѓЗНФмЛёЕУвНСЦЦїаЕзЂВсжЄЃЌКѓајЯрЙиЩѓЦРЙЄзїЫљашЕФЪБМфКЭНсЙћОљОпгавЛЖЈЕФВЛШЗЖЈадЃЌвђДЫЃЌЙЋЫОЩаЮоЗЈдЄВтЦфЖдЙЋЫОЮДРДвЕМЈЕФгАЯьЃЌЙЋЫОНЋИљОнБОДЮЩъБЈзЂВсЕФНјеЙЧщПіМАЪБАДЙцЖЈТФаааХЯЂХћТЖвхЮёЁЃОДЧыЙуДѓЭЖзЪепНїЩїОіВпЃЌзЂвтЭЖзЪЗчЯеЁЃ
ЬиДЫЙЋИцЁЃ
ЩюлкЛЊДѓЛљвђЙЩЗнгаЯоЙЋЫОЖЪТЛс
2019Фъ2дТ1Ше